
【题目】在2A(g)+B(g)![]() 3C(g)+4D(g)反应中,表示该反应的反应速率最快的是
3C(g)+4D(g)反应中,表示该反应的反应速率最快的是
A.v(A)=0.5 mol·L1·min 1B.v(B)=0.1 mol·L1·s1
C.v(C)=0.8 mol·L1·min 1D.v(D)=1 mol·L1·min 1
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】合成NH3所需的H2可由煤与H2O反应制得,其中有一步反应为:CO(g)+H2O(g)![]() CO2(g)+H2(g) △H>O,欲提高CO转化率可采用的方法可能有①降低温度②增大压强③使用催化剂④增大CO的浓度⑤增大水蒸气的浓度,其中正确的组合是( )
CO2(g)+H2(g) △H>O,欲提高CO转化率可采用的方法可能有①降低温度②增大压强③使用催化剂④增大CO的浓度⑤增大水蒸气的浓度,其中正确的组合是( )
A. ①②③B. ④⑤C. ①⑤D. ⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《本草图经》有“白矾多人药用”。白矾[KAl(SO4)2·12H2O]又称明矾.钾铝矾、钾明矾等,是一种重要的化学试剂。下列说法正确的是( )
A.含白矾的药物不宜与胃药奧美拉唑碳酸氢钠胶囊同时服用
B.0.1molL-1白矾溶液完全水解生成Al(OH)3胶粒数小于6.02×1022
C.向含0.1mol白矾的溶液中滴入Ba(OH)2溶液,若SO42-和Al3+全部转化为BaSO4和Al(OH)3沉淀,则此时生成沉淀的质量最大
D.室温下,0.1molL-1白矾溶液中水电离出c(H+)小于10-7mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用蒸馏水稀释0. 1mol/L的CH3COOH溶液时,始终保持增大趋势的是
A. c(CH3COOH)B. c(H+)C. c(CH3COO-)D. c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室利用如图装置探究SO2还原CuO,并进一步检测产物含量。已知Cu2O+2H+=Cu+Cu2++H2O。回答下列相关问题:
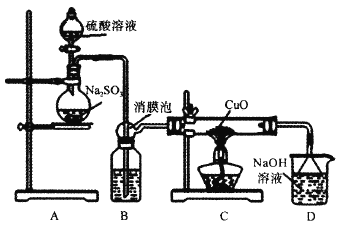
Ⅰ.SO2还原CuO的探究
(1)装置B中宜放入的试剂为___,消膜泡的作用是__。
(2)使用98%的H2SO4溶液制备SO2的速率明显小于使用65%的H2SO4溶液制备SO2,原因是__。
(3)充分反应后,黑色固体变为红色。取C中适量的产物,加水后溶液显蓝色并有红色沉淀物,取红色沉淀物滴加盐酸,溶液又呈蓝色并仍有少量红色不溶物,由此可以得出SO2与CuO反应的方程式为__。
Ⅱ.生成物中CuSO4含量检测
(4)用“碘量法”测定产物中CuSO4含量。取mg固体溶解于水配制为250mL溶液,取20.00mL溶液滴加几滴稀硫酸,再加入过量KI溶液,以淀粉为指示剂用Na2S2O3标准溶液滴定,相关化学反应为2Cu2++4I-=2CuI↓+I2,I2+I-![]() I3-,I2+2S2O32-=S4O62-+2I-。
I3-,I2+2S2O32-=S4O62-+2I-。
①Na2S2O3标准溶液易变质,滴定前需要标定。配制该溶液时需要的玻璃仪器有烧杯、___、玻璃棒和试剂瓶。
②若消耗0.1000mol/LNa2S2O3标准溶液VmL,则产物中CuSO4质量分数为____(写表达式)。
③CuI沉淀物对I3-具有强的吸附能力,由此会造成CuSO4质量分数测定值____(填“偏大”或“偏小”)。为减少实验误差,滴定过程中,常常在接近终点时加入KSCN,使CuI转化为溶解度更小的CuSCN,该沉淀物对I3-吸附能力极弱,KSCN加入太早,I2的浓度较大,I2会将SCN-氧化生成SO42-和ICN,该反应的离子方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方程式书写正确的是
A.溴乙烷发生消去反应:![]()
B.向![]() 溶液中加入过量氨水:
溶液中加入过量氨水:![]()
C.向![]() 溶液中加入过量
溶液中加入过量![]() 溶液:
溶液:![]()
D.向含![]() 和KOH均为0.1 mol的混合溶液中通人标准状况下4.48 L
和KOH均为0.1 mol的混合溶液中通人标准状况下4.48 L![]() 气体:
气体:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.冰的密度小于水,是因为冰中水分子的氢键导致分子间出现较大空隙
B.碘晶体是分子晶体,加热升华过程中只需克服原子间作用力
C.某物质在熔融态时能导电,则该物质一定是离子化合物
D.在![]() 、
、![]() 晶体中,阳离子与阴离子个数比均为
晶体中,阳离子与阴离子个数比均为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,![]() 的
的![]() 和
和![]() 的
的![]() 两种酸溶液,起始时的体积均为
两种酸溶液,起始时的体积均为![]() ,分别向两溶液中加水进行稀释,稀释后溶液体积为V,所得曲线如图所示。下列说法正确的是
,分别向两溶液中加水进行稀释,稀释后溶液体积为V,所得曲线如图所示。下列说法正确的是
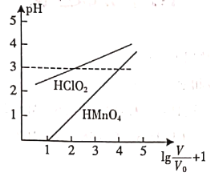
A.在![]() 时,
时,![]() 溶液满足
溶液满足![]()
B.当稀释至pH均为3时,溶液中![]()
C.稀释前分别用![]() 的NaOH溶液中和,消耗的NaOH溶液体积:
的NaOH溶液中和,消耗的NaOH溶液体积:![]()
D.常温下,浓度均为![]() 的
的![]() 和
和![]() 溶液的
溶液的![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.现有pH=2的醋酸溶液甲和pH=2的盐酸乙,请根据下列操作回答问题:
(1)取10 mL的甲溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中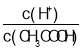 的比值将____________(填“增大”、“减小”或“无法确定”)。
的比值将____________(填“增大”、“减小”或“无法确定”)。
(2)相同条件下,取等体积的甲、乙两溶液,各稀释100倍。稀释后的溶液,其pH大小关系为:pH甲________pH乙(填“大于”、“小于”或“等于”)。
(3)各取25 mL的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和至pH=7,则消耗的NaOH溶液的体积大小关系为: V甲_____V乙(填“大于”、“小于”或“等于”)。
Ⅱ.有一学生在实验室测某溶液的pH。实验时,他先用蒸馏水润湿pH试纸,然后用洁净干燥的玻璃棒蘸取试样进行检测。
(1)该学生的操作是______________(填“正确的”或“不正确的”)。
(2)若用此法分别测定c (H+)相等的盐酸和醋酸溶液的pH,误差较大的是___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com