
【题目】环戊烯是生产精细化工产品的重要中间体,其制备涉及的反应如下:
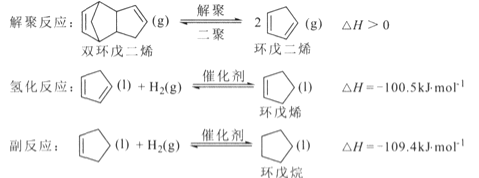
回答下列问题:
(l)反应![]() 的△H= _________ kJ/mol 。
的△H= _________ kJ/mol 。
(2)解聚反应在刚性容器中进行。
①其他条件不变,有利于提高双环戊二烯平衡转化率的条件是 ____ (填标号).
A.升高温度 B.降低温度 C.增大压强 D.减小压强
②实际生产中常通入水蒸气以降低双环戊二烯的沸点。某温度下,通入总压为l00kPa的双环戊二烯和水蒸气,达到平衡后总压为160kPa,双环戊二烯的转化率为8 0%,则 pH2O=___kpa,平衡常数Kp=______kPa (Kp为以分压表示的平衡常数)
(3) 一定条件下,将环戊二烯溶于有机溶剂中进行氢化反应,反应过程中保持氢气压力不变,测得环戊烯和环戊烷的产率(以环戊二烯为原料计)随时间变化如下图所示。

①将环戊二烯溶于有机溶剂中可减少二聚反应的发生,原因是____,
②最佳的反应时间为__h。活化能较大的是__(填“氢化反应”或“副反应”)。
(4)已知氢化反应平衡常数为1.6 × 1012,副反应的平衡常数为2.0×10l2。在恒温恒容下,环戊二烯与氢气按物质的量之比为1:1进行反应,则环戊二烯的含量随时间变化趋势是____(不考虑环戊二烯的二聚反应)。
【答案】-209.9 AD 25 960 降低环戊二烯浓度,减小二聚速率;稀释有利于平衡向解聚方向移动 4 副反应 先变小后变大(最后不变)
【解析】
(1)已知![]() ,
,
![]() ,根据盖斯定律,由氢化反应+副反应得反应
,根据盖斯定律,由氢化反应+副反应得反应![]() △H=-100.5kJ/mol-109.4kJ/mol=-209.9kJ/mol;
△H=-100.5kJ/mol-109.4kJ/mol=-209.9kJ/mol;
(2)①提高双环戊二烯平衡转化率则平衡正向移动;
A.升高温度,平衡向吸热反应的正反应方向移动,选项A符合;
B.降低温度,平衡向放热反应的逆反应方向移动,选项B不符合;
C.增大压强,平衡向气体体积缩小的逆反应方向移动,选项C不符合;
D.减小压强,平衡向气体体积增大的正反应方向移动,选项D符合;
答案选AD;
②实际生产中常通入水蒸气以降低双环戊二烯的沸点。某温度下,通入总压为l00kPa的双环戊二烯和水蒸气,达到平衡后总压为160kPa,则增压60kPa,双环戊二烯的转化率为8 0%,则反应前双环戊二烯的分压为![]() ,则 pH2O=l00kPa-75kPa=25kPa,平衡时双环戊二烯、环戊二烯的平衡分压分别为15kPa、120kPa,平衡常数Kp=
,则 pH2O=l00kPa-75kPa=25kPa,平衡时双环戊二烯、环戊二烯的平衡分压分别为15kPa、120kPa,平衡常数Kp=![]() =960kPa;
=960kPa;
(3)①将环戊二烯溶于有机溶剂中可减少二聚反应的发生,原因是降低环戊二烯浓度,减小二聚速率;稀释有利于平衡向解聚方向移动;
②根据图中信息可知,4h时环戊烯的产率最大,故最佳的反应时间为4h。根据各反应的焓变以及环戊烯和环戊烷产率随时间的变化曲线可知,活化能较大的是副反应;
(4)已知氢化反应平衡常数为1.6 ×1012,副反应的平衡常数为2.0×1012。在恒温恒容下,环戊二烯与氢气按物质的量之比为1:1进行反应,开始一段时间,氢化反应的活化能较小,氢化反应比副反应快,环戊二烯的含量随时间的推移变小;一段时间后,由于副反应的平衡常数大于氢化反应的平衡常数,副反应进行的程度大、放热多,使氢化反应逆向进行,环戊二烯的含量随时间推移又变大,直至最后不变。


科目:高中化学 来源: 题型:
【题目】金属蚀刻加工过程中,常用盐酸对其表面氧化物进行清洗,会产生酸洗废水。 pH在1.5左右的某酸洗废水中含铁元素质量分数约3%,其他金属元素如铜、镍、锌、 铬浓度较低,工业上综合利用酸洗废水可制备三氯化铁。制备过程如下:

相关金属离子生成氢氧化物沉淀的pH如下表所示:

回答下列问题:
(1)“中和”时发生反应的化学方程式为__________________,调节pH至________范围,有利于后续制备得纯度较高的产品。
(2)酸溶处理中和后的滤渣,使铁元素浸出。滤渣和工业盐酸反应时,不同反应温度下 铁浸出率随时间变化如图(a)所示,可知酸溶的最佳温度为_______________。按照不同的固液比(滤渣和工业盐酸的投入体积比)进行反应时,铁浸出率随时间变化如 图(b)所示,实际生产中固液比选择1.5:1的原因是___________。

(3)氧化时,可选氯酸钠或过氧化氢为氧化剂,若100L“酸溶”所得溶液中Fe 2+含量为1.2molL1,则需投入的氧化剂过氧化氢的质量为_____________。
(4)氧化时,除可外加氧化剂外,也可采用惰性电极电解的方法,此时阴极的电极反应式为____,电解总反应的离子方程式是 ___。
(5)将得到的FeCl3溶液在HCl气氛中_________、过滤、洗涤、干燥得FeCl36H2O晶体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)铅蓄电池(原电池)工作时,总反应为Pb +PbO2+2H2SO4→2PbSO4 +2H2O 由此可以判断:
A.原电池的电极材料:①正极为____,②负极为___。
B.工作后,蓄电池里电解质溶液的pH___(填“变大”“变小”或“不变”),理由是____。
(2)如图所示,水槽中试管内有一枚铁钉,放置数天观察:

a.若试管内液面上升,则原溶液是___性,发生_____腐蚀,电极反应,正极为_____。
b.若试管内液面下降,则原溶液呈____性,发生____腐蚀,电极反应:负极为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在t℃时,稀硫酸和盐酸混合液中,c(H+)=10-amol·L-1,c(OH-)=10-bmol·L-1,已知a+b=12,向20mL该混合酸溶液中逐滴加入pH=11Ba(OH)2溶液,生成BaSO4的量如图所示,当加入60mL Ba(OH)2溶液时,C点溶液的pH=6(体积变化忽略不计),试计算:
(1)t℃时,Kw=___,最初混合酸中c(SO42-)=___,c(Cl-)=____。
(2)A点pH=_____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T K时,向2.0L恒容密闭容器中充入0.10molCOCl2,发生反应 ![]() ,经过一段时间后反应达到平衡。反应过程中测得的部分数据见下表,下列说法正确的是
,经过一段时间后反应达到平衡。反应过程中测得的部分数据见下表,下列说法正确的是
t/s | 0 | 2 | 4 | 6 | 8 |
n(Cl2)/mol | 0 | 0.030 | 0.039 | 0.040 | 0.040 |
A. 反应在前2s的平均速率![]() mol·L-1·s-1
mol·L-1·s-1
B. 保持其他条件不变,升高温度,若新平衡时c(C12)=0.038mol·L-1,则反应的△H<0
C. 平衡后向上述容器中再充入0.10molCOCl2,平衡正向移动,COCl2的转化率增大
D. T K时该反应的化学平衡常数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下如图,关闭活塞,在左右两室(体积相同)各充入一定量H2和Cl2,且恰好使两容器内气体密度相同,打开活塞,点燃使H2与Cl2充分反应生成氯化氢气体:H2+Cl2=2HCl,恢复到原温度后,下列判断正确的是
A. 开始时左右两室分子数相同
B. 最终容器内无H2存在
C. 反应前后H2室压强相同
D. 最终容器内密度与原来相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素R、X、Y、Z的原子序数依次增大,由这些元素组成的物质之间的转化关系如图所示,其中c、d为单质,a、b、g为二元化合物。b是10电子分子,g是18电子分子。下列说法正确的是

A. 同温同浓度的e和f溶液,后者pH较大
B. 含X、R、Z三种元素的化合物只有一种
C. 0.1mol的d与足量的e溶液反应转移电子数约为 1.204×1023
D. e和f含化学键类型相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Mn2O3是一种重要的工业原料,在电磁和有机合成等领域应用广泛。某学习小组在实验室用CH4还原MnO2制备Mn2O3,并测定产品纯度。请回答下列问题:
Ⅰ.制备(实验装置如图所示)

已知:Al4C3+12H2O==4Al(OH)3+3CH4↑。
(1)仪器a的名称为______________________
(2)用稀醋酸代替水的优点有________________________________________
(3)连接好实验装置,检验装置的气密性并加入相应试剂。向烧瓶中滴加稀醋酸之后,在点燃酒精灯之前应进行的操作是__________________________________
(4)仪器b中同时生成两种能参与大气循环的物质,该反应的化学方程式为______________
(5)指出上述实验装置有一处明显的缺陷____________________________
Ⅱ.测定产品中Mn2O3的纯度(只考虑产品中混有少量未参与反应的MnO2)
ⅰ.实验结束后,取仪器b中所得固体7.19g,加入足量硫酸酸化的KI溶液,使固体中锰元素全部转化为Mn2+;
ⅱ.将所得溶液稀释至500mL;
ⅲ.取25.00mL稀释后的溶液,滴加几滴淀粉溶液,用0.200molL-1的Na2S2O3标准溶液滴定,达到滴定终点时,消耗25.00mLNa2S2O3标准溶液。(已知:I2+2 Na2S2O3==Na2S4O6+2NaI)
(1)步骤ⅰ中发生反应的离子方程式为________________________________________
(2)滴定终点的标志是__________________________________________________
(3)所取固体中Mn2O3的质量分数为___________________(计算结果精确到0.1%)
(4)下列操作使测定结果偏高的是______________
A.滴定前平视,滴定终点俯视读数
B.盛放Na2S2O3标准溶液的滴定管未用标准液润洗
C.硫酸酸化的KI溶液在空气中静置时间过长
D.滴定前正常,滴定后滴定管尖嘴内有气泡
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com