
【题目】如图所示。请回答:

(1)若C为稀H2SO4溶液,电流表指针发生偏转,B电极材料为Zn,A极材料为铜,该装置能量转换形式____, A为____极,此电池所发生的反应化学方程式为_____,反应进行一段时间后溶液C中c(H+)将_____(填“变大” “变小”或“基本不变”)。溶液中的SO42-移向____极(填“A”或“B”)
(2)若C为CuSO4溶液,B电极材料为Fe,A极材料为石墨。则B为_____极,B极上电极反应属于____(填“氧化反应”或“还原反应”)。B电极上发生的电极反应式为______,A极产生的现象是_____;若AB两电极质量都为50.0g且反应过程中有0.2mol的电子发生转移,理论上AB两电极质量差为____g。
【答案】化学能转化为电能 正 H2SO4+ Zn==H2↑+ZnSO4 减小 B 负 氧化反应 Fe-2e-==Fe2+ 有红色物质析出 12.0
【解析】
(1)锌比铜活泼,则锌作负极,原电池反应是锌与稀硫酸置换氢气的反应,正极反应是氢离子得电子生成氢气,负极上是金属铁发生失去电子的氧化反应,结合原电池的工作原理分析作答;
(2)若C为CuSO4溶液,B电极材料为Fe,A极材料为石墨,则总反应为铁与硫酸铜发生自发的氧化还原反应。原电池中,B电极为负极,发生失电子的氧化反应,A电极为正极,发生得电子的还原反应,结合原电池的工作原理及电化学计算中电子转移数守恒作答;
(1)锌比铜活泼,则该装置为锌作负极,铜做正极的原电池,化学能转化为电能;A极材料为铜,即A为正极,则该原电池反应是锌与稀硫酸置换氢气的反应, H2SO4+ Zn==H2↑+ZnSO4;依据总反应可知溶液中氢离子放电,导致溶液中氢离子浓度减小;原电池中阴离子移向负极,则溶液中的SO42-移向B极,
故答案为:正;H2SO4+ Zn==H2↑+ZnSO4;减小;B;
(2)依据上述分析易知:B电极为原电池的负极,发生发生失电子的氧化反应,其电极反应式为:Fe-2e-==Fe2+;A极铜离子得电子转化为铜单质,其电极反应式为:Cu2++2e-=Cu,故现象为:有红色物质析出;反应过程中有0.2mol的电子发生转移,则消耗的铁的质量为m(Fe)= ![]() =5.6g,生成的铜的质量为m(Cu)=
=5.6g,生成的铜的质量为m(Cu)= ![]() =6.4g,则两极的质量差为m(Fe)+ m(Cu)=5.6g+6.4g=12.0g,故答案为:负;氧化反应;Fe-2e-==Fe2+;有红色物质析出;12.0;
=6.4g,则两极的质量差为m(Fe)+ m(Cu)=5.6g+6.4g=12.0g,故答案为:负;氧化反应;Fe-2e-==Fe2+;有红色物质析出;12.0;


 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案科目:高中化学 来源: 题型:
【题目】工业上常利用含硫废水生产 Na2S2O3·5H2O,实验室可用如图装置(略去部分夹持仪器)模拟生产过程
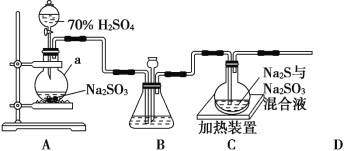
(1)仪器a的名称是__________,A中发生的化学反应方程为_______________________;
(2)实验中,为使 SO2 缓慢进入装置C,采用的操作______________,装置C中制备反应结束的现象___________________;
(3)装置 C 中的溶液一般需控制在碱性环境,否则产品发黄,用离子方程式表示其原因为 ___________________;
(4)为减少装置C中可能出现的Na2SO4杂质,在不改变原有装置的基础上应采取的操作是__________________;
(5)装置 D 用于处理尾气,可选用的最合理装置(夹持仪器已略去)为_____(填序号)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钾、氟及锌的相关化合物用途非常广泛。回答下列问题:
(1)基态锌原子的价电子排布式为___________;K、F、Zn的电负性从大到小的顺序为___________。
(2)Zn与Ca位于同一周期且最外层电子数相等,钙的熔点与沸点均比锌高,其原因是_______________。
(3)OF2分子的几何构型为___________,中心原子的杂化类型为___________。
(4)KOH 与O3反应可得到KO3(臭氧化钾),KO3 中除σ键外,还存在___________;与O3-互为等电子体的分子为___________ (任 写一种 )。
(5)K、F、Zn组成的一种晶体结构如图所示,其晶胞参数为a=0.4058 nm。

①晶胞中Zn2+的配位数为___________个。
②晶胞中紧邻的两个F-间的距离为_______________________(列出算式即可)nm。
③该晶体的密度为___________(列出算式即可,用NA表示阿伏加德罗常数的数值)g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以硫铁矿(FeS2的质量分数为60%)为原料制备氯化铁晶体(FeCl3·6H2O,270.5g·moˉ1)的工艺流程如图所示。

请回答下列问题:
(1)为加快焙烧反应的化学反应速率,可采取的措施为_____、_____。(任写两条)
(2)焙烧后得到的Fe2O3在酸溶过程中发生反应的离子方程式为________。
(3)过滤操作用到的玻璃仪器有烧杯、_______、______。
(4)焙烧过程中产生的SO2可用过量的氨水进行吸收,所得溶液中溶质的名称为_______。
(5)先向氯化铁溶液中加适量盐酸的目的是______,再______、______、过滤、洗涤,最终得到氯化铁晶体。
(6)若取1kg硫铁矿经过上述流程(铁元素在整个流程中损失率为4%),则可得氯化铁晶体的质量为_______(保留一位小数)kg。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用已知浓度的盐酸滴定未知浓度的NaOH溶液时,下列操作中不正确的是
A.酸式滴定管用蒸馏水洗净后,必须用已知浓度的盐酸润洗
B.锥形瓶用蒸馏水洗净后,用NaOH溶液润洗后再加入待测液
C.滴定时,必须逐出滴定管下口的气泡
D.读数时,视线与滴定管内液体的凹液面最低处保持水平
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究NO2、NO、CO等污染物的处理对建设美丽中国具有重要意义。
(1)利用甲烷催化还原NOx:
CH4(g)+4NO2(g) ===4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1
CH4(g)+4NO(g) ===2N2(g)+CO2(g)+2H2O(g) ΔH2=-1160 kJ·mol-1
①甲烷直接将NO2还原为N2的热化学方程式为________________________________。
②将CH4和NO2充入密闭容器中发生上述反应,该反应达到平衡后,为了提高反应速率的同时提高NO2的转化率,可采取的措施有__________(写一点即可)。
③利用原电池反应可实现NO2的无害化,总反应为6NO2+8NH3===7N2+12H2O,电解质溶液为NaOH溶液,工作一段时间后,该电池正极区附近溶液pH________(填“增大”、“减小”或“不变”),负极的电极反应式为___________________。
(2)光气(COCl2)在塑料、制革、制药等工业中有许多用途。工业上常利用废气CO2通过反应:C(s)+CO2(g)![]() 2CO(g) ΔH>0,制取合成光气的原料气CO。在体积可变的恒压(p总)密闭容器中充入1mol CO2 与足量的碳发生上述反应,在平衡时体系中气体体积分数与温度的关系如图所示:
2CO(g) ΔH>0,制取合成光气的原料气CO。在体积可变的恒压(p总)密闭容器中充入1mol CO2 与足量的碳发生上述反应,在平衡时体系中气体体积分数与温度的关系如图所示:
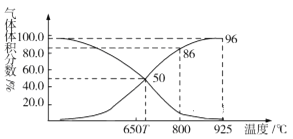
①T℃时,在容器中若充入稀有气体,平衡______移动(填“正向”“逆向”或“不”,下同);若充入等体积的CO2和CO,平衡________移动。
②CO体积分数为40%时,CO2的转化率为_______。
③已知:气体分压(p分)=气体总压×体积分数。800℃时用平衡分压代替平衡浓度表示平衡常数Kp=______(用含p总的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两个恒容的密闭容器中进行下列两个可逆反应:
甲:C(s)+H2O(g)![]() CO(g)+H2(g)
CO(g)+H2(g)
乙:CO(g)+H2O(g)![]() CO2(g)+H2(g)
CO2(g)+H2(g)
现有下列状态:①混合气体平均相对分子质量不再改变
②恒温时,气体压强不再改变 ③各气体组成浓度相等
④反应体系中温度保持不变 ⑤断裂氢氧键速率是断裂氢氢键速率的2倍 ⑥混合气体密度不变 ⑦单位时间内,消耗水蒸气质量与生成氢气质量比为9∶1
其中能表明甲、乙容器中反应都达到平衡状态的是( )
A. ①②⑤ B. ③④⑥ C. ⑥⑦ D. ④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W代表四种短周期元素,有关它们的部分结构信息及性质信息如表所示。
元素 | 部分结构信息 | 部分性质信息 |
X | X的单质由双原子分子构成 | X的氢化物水溶液呈碱性 |
Y | Y原子的最外层电子数是其内层电子数的两倍 | Y能形成多种气态氢化物 |
Z | Z原子有三个电子层 | 含有Z元素的化合物的焰色反应呈黄色 |
W | W原子的最外层电子数等于(2n+1)(n为原子核外电子层数) | W和Z能按1∶1的原子个数比形成离子化合物 |
请按要求回答下列问题:
(1)W在元素周期表中的位置是______。
(2)X简单气态氢化物的分子式为______。(用化学式表示)
(3)X、Y、W三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序是______。(用化学式表示)
(4)Z单质在W单质中发生反应的实验现象是______。
(5)写出W的单质与二氧化硫的混合气体通入水中所发生反应的离子方程式:______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com