
【题目】下列基态原子或离子的电子排布式(图)正确的是______(填序号,下同),违反能量最低原理的是______,违反洪特规则的是______,违反泡利原理的是______.
①![]() :
:![]()
②![]() :
:![]()
③P: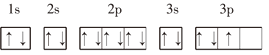
④Cr:![]()
⑤Fe:![]()
⑥![]() :
:![]()
⑦O: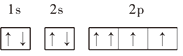
【答案】①⑤⑥ ② ③④ ⑦
【解析】
根据构造原理,利用核外电子排布的三个原理:能量最低原理、泡利原理、洪特规则可对各项作出判断。
①Ca的电子排布式为:1s22s22p63s23p64s2,失去4s能级上的2个电子变成具有稀有气体电子层结构的Ca2+:1s22s22p63s23p6,离子的电子排布式书写正确;
②②离子的电子排布违反了能量最低原理,能量:2p<3p,F-核外电子排布应表示为:1s22s22p6;
③P的3p能级上的3个电子没有独占1个轨道,违反了洪特规则,正确的电子排布图为: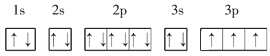
④Cr的价电子构型应为:3d54s1,3d轨道半充满状态更稳定,此为洪特规则特例,所以④违反了洪特规则;
⑤Fe原子序数为26,电子排布式为:1s22s22p63s23p63d64s2,书写正确;
⑥Mg的电子排布式为:1s22s22p63s2,失去3s能级上的2个电子变成具有稀有气体电子层结构的Mg2+:1s22s22p6,离子的电子排布式书写正确;
⑦O电子排布图2p能级的1个轨道上的一对电子自旋方向相同,违反了泡利原理,应表示为:![]() ;
;
总之,基态原子或离子的电子排布式(图)正确的是①⑤⑥,违反能量最低原理的是②,违反洪特规则的是③④,违反泡利原理的是⑦。答案为:①⑤⑥;②;③④;⑦。


 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】有机化合物在自然界中数目非常庞大,对此你认为下列解释不合理的是( )
A.碳原子能与其他原子形成四个共价键
B.有机化合物存在同分异构现象
C.碳是非金属元素
D.碳原子能与![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 等多种非金属原子形成共价化合物,且原子连接方式多样
等多种非金属原子形成共价化合物,且原子连接方式多样
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或有关化学用语的使用正确的是( )
A.在基态多电子原子中,p轨道电子的能量一定高于s轨道电子的能量
B.Fe原子的外围电子排布图为![]()
C.氧的电负性比氮大,故氧元素的第一电离能比氮元素的第一电离能大
D.铜原子的外围电子排布式为3d94s2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.原子核外电子排布式为![]() 的原子与原子核外电子排布式为
的原子与原子核外电子排布式为![]() 的原子对应元素的化学性质相似
的原子对应元素的化学性质相似
B.![]() 的最外层电子排布式为
的最外层电子排布式为![]()
C.基态铜原子外围电子排布图为![]()
D.基态碳原子最外层电子排布图为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组用合金铝、铁、铜的废弃合金为原料制取硝酸铜晶体和氢氧化铝,并测定硝酸铜晶体的结晶水含量和氢氧化铝的纯度,设计的主要流程如下:
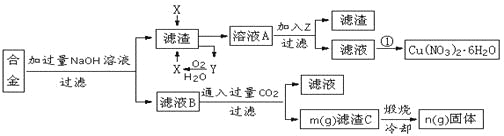
已知:
Fe2+沉淀的pH范围为7.0~9.0;Fe3+沉淀的pH范围为1.9~3.2;Cu2+沉淀的pH范围为4.7~6.7
回答下列问题:
(1)写出合金中加入NaOH溶液后所发生的离子反应方程式_______________________。试剂X的名称为______________。
(2)加入Z的作用是调节溶液的pH,pH范围应为_____;下列可作为试剂Z的是_______。
a.铜粉 b.氨水 c.氧化铜 d.硫酸铜
(3)实验操作①依次是_________、_________、过滤洗涤即可得硝酸铜晶体。
(4)测定硝酸铜晶体的结晶水含量,下列方案中肯定不可行的是______。(选填编号)
a.称量样品→加热→冷却→称量CuO
b.称量样品→加热→冷却→称量Cu(NO3)2
c.称量样品→加热→用已知质量的无水氯化钙吸收水蒸气并称量
d.称量样品→加过量已知量的NaOH溶液→选用酚酞指示剂用标准盐酸滴定
(5)根据流程图内数据计算:滤渣C中氢氧化铝的质量分数为______________________。(用m、n的代数式表示)
(6)按该流程的操作步骤,氢氧化铝质量分数的测定结果偏高的可能性是最大的,原因有_______________________________;____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含硫化合物在生产、生活中有广泛应用,其吸收和处理也十分重要。回答下列问题:
1.SO2具有还原性,写出将SO2气体通入 FeCl3溶液中的离子方程式_________,并标出电子转移的数目及方向。_____________________________________________________________
2.在Na2SO3溶液中滴加酚酞,溶液变红色,若在该溶液中滴入过量的BaCl2溶液,现象是_________,请结合离子方程式,运用平衡原理进行解释_____________________。
3.等体积等物质的量浓度的 NaClO溶液与Na2SO3溶液混合后,溶液显______性。此时溶液中浓度相等的微粒是___________________________________________。
4.已知:H2S:Ki1=1.3×10-7Ki2=7.1×10-15 H2CO3:Ki1=4.3×10-7Ki2=5.6×10-11
含H2S尾气用足量的Na2CO3溶液来吸收。写出离子反应方程式。____________
常温时,等体积等浓度的Na2S和Na2CO3溶液的离子总数:N前___N后(填“>”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业制硫酸工艺的催化氧化反应原理是:2SO2(g)+O2(g)![]() 2SO3(g)ΔH<0,起始以相同的物质的量进行投料,测得SO2在不同温度下的平衡转化率与压强的关系如图所示。下列说法正确的是( )
2SO3(g)ΔH<0,起始以相同的物质的量进行投料,测得SO2在不同温度下的平衡转化率与压强的关系如图所示。下列说法正确的是( )
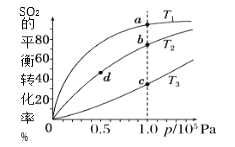
A.温度:T1>T2>T3
B.正反应速率:υ(a)>υ(c)、υ(b)>υ(d)
C.平均摩尔质量:M(a)>M(c)、M(b)>M(d)
D.平衡常数:K(a)>K(c)、K(b)>K(d)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过学习,同学们对宏观辨识与微观探析,变化观念与平衡思想等学科素养有了进一步的认识和理解。请根据所学知识回答下列问题:
(1)FeCl3溶液呈________性(填“酸”、“中”或“碱”),原因是__________________(用离子方程式表示);若把FeCl3溶液蒸干,灼烧,最后得到固体产物是 ____________,原因是________________________________________________。
(2)将1L 0.2 mol·L-1HA溶液与1L 0.1 mol·L-1NaOH溶液等体积混合(混合后溶液体积变化忽略不计),测得混合溶液中c(Na+)>c(A-),则混合溶液中c(HA)+c(A-)_____0.1 mol·L-1(填“>”、“<”或“=”)。
(3)浓度均为0.1 mol/L的四种溶液①氯化铵溶液、②碳酸氢铵溶液、③氨水、④硫酸氢铵中,NH4+浓度由大到小的顺序为_______________________________。
(4)铅蓄电池是典型的可充电型电池,电池总反应式为:Pb+PbO2+4H++2SO42-![]() 2PbSO4+2H2O。放电时,负极的电极反应式是__________________________;充电时,当外电路通过1 mol电子时,理论上正极板的质量减少________________g。
2PbSO4+2H2O。放电时,负极的电极反应式是__________________________;充电时,当外电路通过1 mol电子时,理论上正极板的质量减少________________g。
(5)已知:常温下,Ksp[Mg(OH)2]=1.8×10-11,Ksp[Fe(OH)3]=4×10-38。
①常温下,某酸性MgCl2溶液中含有少量的FeCl3 ,为了得到纯净的MgCl2·2H2O晶体,应加入________(填化学式),调节溶液的pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=________mol·L-1。
②常温下,若将0.01 mol·L-1 MgCl2溶液与________ mol·L-1 NaOH溶液等体积混合时有沉淀生成。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸的产量是衡量一个国家化工水平的标志。2004年我国催化剂硫酸产量即已位居世界第一。![]() 是工业制硫酸的重要反应。在催化加热条件下,向恒容密闭容器中充入
是工业制硫酸的重要反应。在催化加热条件下,向恒容密闭容器中充入![]() 和
和![]() ,测得
,测得![]() 浓度(c)随时间(t)的变化关系如图所示。
浓度(c)随时间(t)的变化关系如图所示。
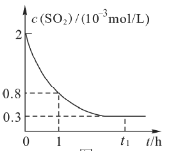
【1】在0~1h(小时)内,用![]() 浓度变化表示该反应的平均速率是____________
浓度变化表示该反应的平均速率是____________
A.![]() B.
B.![]()
C.![]() D.
D.![]()
【2】为加快该反应的速率,下列措施可行的是___________
A.降低温度B.使用更高效的催化剂
C.减小![]() 的浓度D.减小
的浓度D.减小![]() 的浓度,
的浓度,
【3】关于![]() 时刻的反应体系,下列说法正确的是____________
时刻的反应体系,下列说法正确的是____________
A.反应完全停止B.![]() 已完全转化为
已完全转化为![]()
C.反应未达到平衡状态D.![]() 的浓度均不再变化
的浓度均不再变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com