
【题目】Na2S2O3是重要的化工原料,易溶于水,在中性或碱性环境中稳定. Ⅰ.制备Na2S2O35H2O
反应原理:Na2SO3(aq)+S(s) ![]() Na2S2O3(aq)
Na2S2O3(aq)
实验步骤:
①称取15g Na2SO3加入圆底烧瓶中,再加入80mL蒸馏水.另取5g研细的硫粉,用3mL乙醇润湿,加入上述溶液中.
②安装实验装置(如图所示,部分夹持装置略去),水浴加热,微沸60分钟.
③趁热过滤,将滤液水浴加热浓缩,冷却析出Na2S2O35H2O,经过滤、洗涤、干燥,得到产品.
回答问题: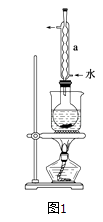
(1)硫粉在反应前用乙醇润湿的目的是 .
(2)仪器a的名称是 , 其作用是 .
(3)产品中除了有未反应的Na2SO3外,最可能存在的无机杂质是 . 检验是否存在该杂质的方法是 .
(4)该实验一般控制在碱性环境下进行,否则产品发黄,用离子反应方程式表示其原因: .
(5)Ⅱ.测定产品纯度 准确称取W g产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.100 0molL﹣1碘的标准溶液滴定.
反应原理为2S2O ![]() +I2═S4O
+I2═S4O ![]() +2I﹣
+2I﹣
滴定至终点时,溶液颜色的变化:
(6)测定起始和终点的液面位置如图2,则消耗碘的标准溶液体积为mL.产品的纯度为(设Na2S2O35H2O相对分子质量为M) . 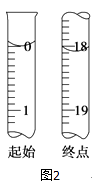
(7)Ⅲ.Na2S2O3的应用 Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO ![]() ,常用作脱氯剂,该反应的离子方程式为
,常用作脱氯剂,该反应的离子方程式为
【答案】
(1)使硫粉易于分散到溶液中
(2)冷凝管;冷凝回流
(3)Na2SO4;取少量产品溶于过量稀盐酸,过滤,向滤液中加BaCl2溶液,若有白色沉淀,则产品中含有Na2SO4
(4)S2O32 ̄+2H+=S↓+SO2↑+H2O
(5)由无色变为蓝色
(6)18.10; ![]() ×100%
×100%
(7)S2O32 ̄+4Cl2+5H2O=2SO42 ̄+8Cl ̄+10H+
【解析】解:(1)硫粉难溶于水微溶于乙醇,所以硫粉在反应前用乙醇湿润是使硫粉易于分散到溶液中,
所以答案是:使硫粉易于分散到溶液中;(2)根据题中图示装置图可知,仪器a为冷凝管,该实验中冷凝管具有冷凝回流的作用,
所以答案是:冷凝管;冷凝回流;(3)S2O32具有还原性,能够被氧气氧化成硫酸根离子,所以可能存在的杂质是硫酸钠;检验硫酸钠的方法为:取少量产品溶于过量稀盐酸,过滤,向滤液中加BaCl2溶液,若有白色沉淀,则产品中含有Na2SO4,
所以答案是:Na2SO4;取少量产品溶于过量稀盐酸,过滤,向滤液中加BaCl2溶液,若有白色沉淀,则产品中含有Na2SO4; (4)S2O32与氢离子发生氧化还原反应生成淡黄色硫单质,反应的离子方程式为:S2O32+2H+=S↓+SO2↑+H2O,
所以答案是:S2O32+2H+=S↓+SO2↑+H2O;(5)滴定结束后,碘单质使淀粉变蓝,所以滴定终点时溶液颜色变化为:由无色变为蓝色,
所以答案是:由无色变为蓝色;(6)根据图示的滴定管中液面可知,滴定管中初始读数为0,滴定终点液面读数为18.10mL,所以消耗碘的标准溶液体积为18.10mL;
根据反应2S2O32﹣+I2═S4O62﹣+2I﹣可知,n(S2O32﹣)=2n(I2),所以W g产品中含有Na2S2O35H2O质量为:0.1000 molL﹣1×18.10×10﹣3L×2×M=3.620×10﹣3Mg,则产品的纯度为: ![]() ×100%=
×100%= ![]() ×100%,
×100%,
所以答案是:18.10; ![]() ×100%;(7)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO42﹣,根据化合价升降相等配平后的离子方程式为:S2O32+4Cl2+5H2O=2SO42+8Cl+10H+,
×100%;(7)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO42﹣,根据化合价升降相等配平后的离子方程式为:S2O32+4Cl2+5H2O=2SO42+8Cl+10H+,
所以答案是:S2O32+4Cl2+5H2O=2SO42+8Cl+10H+.


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:
【题目】某有机物结构简式为 ![]() ,下列叙述错误的是( )
,下列叙述错误的是( )
A.1mol该有机物在加热和催化剂作用下,最多能和4 mol H2反应
B.该有机物能使溴水褪色,也能使酸性KMnO4溶液褪色
C.该有机物遇硝酸银溶液产生白色沉淀
D.该有机物在一定条件下能发生消去反应和取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如右图所示,由此确定,原溶液中含有的阳离子是:
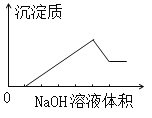
A. Mg2+、Al3+、Fe2+ B. H+、Mg2+、Al3+
C. H+、Ba2+、Al3+ D. 只有Mg2+、Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对于“摩尔”的说法和理解正确的是( )
A. 摩尔是国际科学界建议采用的一种物理量
B. 摩尔可以把微观粒子与可称量物质联系起来
C. 摩尔是物质的量的单位,简称摩,符号为mol
D. 国际上规定,0.012kg碳原子所含有的碳原子数目为1摩
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在生产生活中,我们会遇到各种各样的化学反应。请按要求回答下列问题:
(1)焊接钢铁时常用的焊药为氯化铵,其作用是消除焊接处的铁锈。发生的反应体系中共有六种物质:NH4Cl、N2、Fe2O3、Fe、FeCl3 和 X。
①根据题意,可判断出X是_____________(写化学式)
②写出并配平该反应的化学方程式,并用双线桥标出电子转移的方向和数目:______。
(2)铝元素是自然界中含量最多的的金属元素,应用广泛。金属铝既能与酸反应又能与强碱反应,请写出铝与强碱反应的离子方程式__________________________________________ 。
(3)Na2O2可用作呼吸面具的供氧剂, 发生反应的化学方程式为__________________________。
(4)“水玻璃”长期暴露在空气中会变质,这是因为“水玻璃”与空气中少量二氧化碳接触,生成了乳白色的凝胶状沉淀的缘故。写出反应的离子方程式_________________________________。
(5)小苏打可作胃药,请写出其中和胃酸时的离子方程式______________________ 。
(6)在反应 3BrF3+5H2O = HBrO3+Br2+9HF+O2 中,被氧化的元素是____________,当有5 mol水反应时,由H2O还原的BrF3为______________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境污染已成为人类社会面临的重大问题,各种污染数不胜数。导致下列污染的主要原因与高分子化合物有关的是( )
A. 酸雨 B. 光化学烟雾
C. 温室效应 D. 白色污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某些电镀厂的酸性废水中常含有一定量的CrO42﹣和Cr2O72﹣ , 它们会对人类及生态系统产生很大的伤害,必须进行处理.常用的处理方法有两种
方法1:还原沉淀法,其中第①步存在平衡步存在平衡:2CrO42﹣(黄色)+2H+Cr2O72﹣(橙色)+H2O
(1)若平衡体系的pH=12,该溶液显 .
(2)写出第③步的离子反应方程式: .
(3)第②步中,用6mol的FeSO47H2O可还原molCr2O72﹣离子.
(4)第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3() Cr3+(aq)+3OH﹣(aq)
常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)c3(OH﹣)=10﹣32 , 要使c(Cr3+)降至10﹣5mol/L,溶液的pH应调至 .
方法2:电解法:该法用Fe做电极电解含Cr2O72﹣的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3沉淀.
(5)写出阳极的电极反应式 .
(6)在阴极附近溶液pH升高的原因是(用电极反应解释)
(7)用电镀法在铁制品上镀上一层锌,则阴极上的电极反应式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com