
����Ŀ��˫��ˮ��84����Һ���ճ������г��õ���������
��1��84����Һ����Ҫ�ɷ���NaClO)��Һ�ʼ��ԣ������ӷ���ʽ��ʾ��ԭ��_____________________��
��2��˫��ˮ��84����Һ���ʧȥ�������ã���������ɫ��ζ���壬�ڸ÷�Ӧ����������____________��
��3����ҵ�ϣ��Ʊ�84����Һ��ԭ���ǣ��Զ��Ե缫��ⱥ���Ȼ�����Һ�����������������ɵ��ռ���Һ���ա����������ĵ缫��ӦʽΪ_________________________��д���ܷ�Ӧ�Ļ�ѧ����ʽ______________��
��4��ʵ���ҷֱ���KMnO4��H2O2��KClO3�Ʊ�O2�����õ���������O2ʱ������Ӧ��ת�Ƶ��ӵ���Ŀ֮��Ϊ______________��
��5��˫��ˮ�Ƕ�Ԫ���ᣬ298 Kʱ��Ka1��1.6��1012��Ka2��1.0��1025����298 Kʱ��0.1 mol��L1˫��ˮ��Һ��pH��________________������֪��lg2��0.3��
��6����V2O5��������ϡ����õ�250mL(VO2)2SO4��Һ��ȡ25��00mL����Һ����ƿ�У���0��1000 mol��L-1H2C2O4����Һ���еζ����ﵽ�ζ��յ�ʱ���ı���Һ�����Ϊ20��00mL����֪�ζ�������H2C2O4������ΪCO2��VO2+(��ɫ)����ԭΪVO2+(��ɫ)��
�ٸõζ�ʵ�鲻��Ҫ�������ָʾ�����ﵽ�ζ��յ��������___________________��
��(VO2)2SO4��Һ�����ʵ����ʵ���Ũ��Ϊ___________________��
�۴ﵽ�ζ��յ�ʱ�����ӵζ��ܶ�����ʹ���_________(�ƫ�ߡ�����ƫ�͡�����Ӱ�족)��
���𰸡�ClO��H2O![]() HClO��OH NaClO 2H2O��2e��2OH��H2�� NaCl��H2O
HClO��OH NaClO 2H2O��2e��2OH��H2�� NaCl��H2O![]() NaClO��H2�� 2:1:2 6.4 ��Һ�ɻ�ɫ��Ϊ��ɫ���Ұ���Ӳ���ɫ 0.080mol��L-1 ƫ��
NaClO��H2�� 2:1:2 6.4 ��Һ�ɻ�ɫ��Ϊ��ɫ���Ұ���Ӳ���ɫ 0.080mol��L-1 ƫ��
��������
��1�������������ˮ�����ɴ���������������ӣ���Һ�ʼ��ԣ�
��2��˫��ˮ�У�1����Ԫ�ر������������������������
��3������ˮ������������ӵõ�������������������Ȼ�����Һ���ɴ������ƺ�������
��4��������Ԫ�صĻ��ϼ۱仯��ϵ��ӵ�ʧ�غ�������
��5����Ԫ����ֲ����룬��Ҫ�Ե�һ��Ϊ������ϵ���ƽ�ⳣ�����㣻
��6��������VO2+����ɫ������ԭΪVO2+����ɫ��ָʾ���յ㣻
�ڽ�Ϸ�Ӧ�����ӷ���ʽ�������ʵ�����Ũ��c=n/V��
�۴ﵽ�ζ��յ�ʱ�����ӵζ��ܶ�������ȡ����Һ������ݴ��жϡ�
��1�����ڴ���ˮ�ⷴӦClO��H2O![]() HClO��OH�����84����Һ����Ҫ�ɷ���NaClO����Һ�ʼ��ԣ�
HClO��OH�����84����Һ����Ҫ�ɷ���NaClO����Һ�ʼ��ԣ�
��2��˫��ˮ��84����Һ���ʧȥ�������ã���������ɫ��ζ���壬���ɵ�������������˫��ˮ��84����Һ��Ϸ���������ԭ��Ӧ����O2��ˮ���Ȼ��ƣ���Ԫ�ػ��ϼ۽��ͣ��õ����ӣ��ڸ÷�Ӧ����������NaClO��
��3����ҵ���Ʊ�84����Һ��ԭ���ǣ��Զ��Ե缫��ⱥ���Ȼ�����Һ�����������������ɵ��ռ���Һ���գ�����������ԭ��Ӧ����缫��ӦʽΪ2H2O��2e��2OH��H2�����ܷ�ӦΪNaCl��H2O![]() NaClO��H2����
NaClO��H2����
��4��ʵ���ҷֱ���KMnO4��H2O2��KClO3�Ʊ�O2����Ӧ����Ԫ�ػ��ϼ۷ֱ�ӣ�2�����ߵ�0�ۡ���1�����ߵ�0�ۡ���2�����ߵ�0�ۣ����Ե��õ���������O2ʱ������Ӧ��ת�Ƶ��ӵ���Ŀ֮��Ϊ2:1:2��
��5��˫��ˮ�Ƕ�Ԫ���ᣬ������뷽��ʽΪ��H2O2![]() H++HO2����HO2��
H++HO2����HO2��![]() H++O22���������Ե�һ������Ϊ������c��H+����c��Ka1��0.4��10��6�����298Kʱ0.1molL��1˫��ˮ��Һ��pH=��lg0.4��10��6=6��lg0.4=6.4��
H++O22���������Ե�һ������Ϊ������c��H+����c��Ka1��0.4��10��6�����298Kʱ0.1molL��1˫��ˮ��Һ��pH=��lg0.4��10��6=6��lg0.4=6.4��
��6����VO2+(��ɫ)����ԭΪVO2+(��ɫ)���õζ�ʵ�鲻��Ҫ�������ָʾ������˴ﵽ�ζ��յ�������ǣ��������һ����Һ�ɻ�ɫ��Ϊ��ɫ�Ұ�����ڲ���ɫ��
�ڽ�V2O5��������ϡ����õ�250mL(VO2)2SO4��Һ��ȡ25��00mL����Һ����ƿ�У���0��1000 mol��L-1H2C2O4����Һ���еζ����ﵽ�ζ��յ�ʱ���ı���Һ�����Ϊ20.00mL����֪�ζ�������H2C2O4������ΪCO2��VO2+(��ɫ)����ԭΪVO2+(��ɫ)����Ӧ�����ӷ���ʽΪ��
H2C2O4+2H++2VO2+=2VO2++2CO2��+2H2O
1 2
0.002mol n
���n=0.004mol
250mL��Һ�к�VO2+���ʵ���=250/25��0.004mol=0.04mol��(VO2)2SO4���ʵ���=0.02mol����ҺŨ��=0.02mol��0.25L=0.080mol/L��
�۴ﵽ�ζ��յ�ʱ�����ӵζ��ܶ�������ȡ����Һ���ƫ��c�����⣩=c(��)V(��)/V(����)���ⶨ���ƫ�ߡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ��mA(g)��nB(g) ![]() pC(g)���ﵽƽ��������¶�ʱ��B��ת���ʱ����Сѹǿʱ�������ϵ��C������������С����
pC(g)���ﵽƽ��������¶�ʱ��B��ת���ʱ����Сѹǿʱ�������ϵ��C������������С����
(1)�÷�Ӧ���淴ӦΪ______(��������������������)��Ӧ����m��n______(����>������������<��)p��
(2)��ѹʹ�����������ʱ��A����������________��(��������������С����������������ͬ)
(3)���ݻ��������B����A��ת����__________��B��ת����________��
(4)�������¶ȣ���ƽ��ʱB��C��Ũ��֮��![]() ��________��
��________��
(5)�����������ƽ��ʱ��������������ʵ���______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������۲�����װ�ã�����˵���������
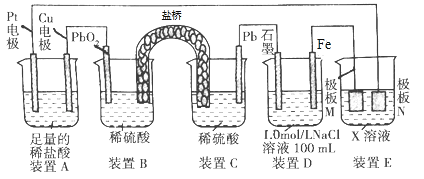
A. װ��B��PbO2�Ϸ����ĵ缫��Ӧ����ʽΪPbO2+4H++SO42-+2e����PbSO4+2H2O
B. װ��A���ܷ�Ӧ�����ӷ���ʽΪCu+2H+![]() Cu2++H2��
Cu2++H2��
C. ����װ��D������0.2 mol Fe(OH)3��������ˮ�����ʵ�����Ϊ0.5 mol
D. ��װ��E��Ŀ������Cu�����϶�������N�IJ���ΪCu
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ѧϰ���о���ѧ����Ҫ�������������ʵķ���������ǣ� ��
A.�����ơ���ʯ�ҡ���������ڼ�
B.CO2��SO2��SO3����������������
C.�����ᡢ�����ᡢ��������ں�����
D.NH4Cl��NH4NO3��CO��NH2��2���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ����Ƴ�����ĤH2Sȼ�ϵ����ʵ��������H2S������Դ�����������õ�����������ĤH2Sȼ�ϵ�صĽṹʾ��ͼ��ͼ��ʾ������˵������ȷ���ǣ� ��
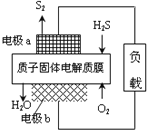
A. �缫aΪ��صĸ���
B. �缫b�Ϸ����ĵ缫��ӦΪ��O2+4H++4e-�T2H2O
C. ��·��ÿ����2mol���ӣ�����������22.4L H2S
D. ÿ34g H2S���뷴Ӧ����2mol H+������Ĥ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z���ֽ�����X��Y���ԭ��أ�X�Ǹ�������Y����Z����������Һ�У�Y������Z�����������˳����
A.X >Y>ZB.Z>Y>X
C.X>Z>YD.Y>X>Z
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ҵ�ǹ�ҵ��������Ҫ֧����
��1����֪��¯��������Ҫ��ӦΪ��
��Fe2O3(s)+3CO(g)��2Fe(s)+3CO2(g) ��H=��25 kJ��mol��1
��3Fe2O3(s)+CO(g)��2Fe3O4(s)+CO2(g) ��H=��47 kJ��mol��1
��Fe3O4(s)+CO(g)��3FeO(s)+CO2(g) ��H=+19 kJ��mol��1
д��FeO(s)��CO��ԭ����Fe(s)��CO2���Ȼ�ѧ����ʽ��________________��
��2�����º��������½��з�ӦFe2O3(s)+3CO(g)![]() 2Fe(s)+3CO2(g)�����и�����˵���÷�Ӧ�Ѵﵽƽ��״̬����_______(��д�����ĸ)��
2Fe(s)+3CO2(g)�����и�����˵���÷�Ӧ�Ѵﵽƽ��״̬����_______(��д�����ĸ)��
a��v(CO)��=v(CO2)�� b��CO��CO2 ��Ũ��֮��Ϊ1��1
c��������ѹǿ���ֲ��� d�����������ܶȱ��ֲ���
��3��ToCʱ����ӦFe2O3(s)+3CO(g)![]() 2Fe(s)+3CO2(g)��ƽ�ⳣ��ΪK=27����1L���ܱ������зֱ��±���ʾ�������ʣ�ά��ToC��Ӧһ��ʱ��ﵽƽ�⣬�ס���������CO��ƽ��ת����֮��=_________��
2Fe(s)+3CO2(g)��ƽ�ⳣ��ΪK=27����1L���ܱ������зֱ��±���ʾ�������ʣ�ά��ToC��Ӧһ��ʱ��ﵽƽ�⣬�ס���������CO��ƽ��ת����֮��=_________��
Fe2O3 | CO | Fe | CO2 | |
������ | 1.0 mol | 1.0 mol | 1.0 mol | 1.0 mol |
������ | 1.0 mol | 2.0 mol | 1.0 mol | 1.0 mol |
��4������Ϊ�ϳɼ״����йػ�ѧ����ʽ��
��2H2(g)+CO(g) ![]() CH3OH(g)
CH3OH(g)
��H2(g)+CO2(g) ![]() H2O(g)+CO(g)
H2O(g)+CO(g)
��3H2(g)+CO2(g) ![]() CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
ij�¶��£�����������Ӧ��ƽ�ⳣ����ֵ�ֱ�Ϊ2.5��2.0��K3����K3ֵΪ_______��
��5�����ǵ�˫ģ�綯����ʹ�ø�����ع��硣������ص��ܷ�ӦΪ��3Zn(OH)2+2Fe(OH)3+4KOH![]() 3Zn+2K2FeO4+8H2O������ʱ��������ӦʽΪ__________��
3Zn+2K2FeO4+8H2O������ʱ��������ӦʽΪ__________��
��6������β���к���CO���������տ����ںϳɼ״���2H2(g)+CO(g)![]() CH3OH(g) ��H=��90.1 kJ��mol��1��ToC���÷�Ӧ��Kp=6.0��10-3kPa-2����ƽ���ѹ����ƽ��Ũ������ƽ�ⳣ������ѹ= ��ѹ�����ʵ��������������¶��µ�ij�����У�����ʼ����2molH2��1molCO��ƽ��ʱ�״���ƽ���ѹp(CH3OH)=24.0kPa����ƽ��ʱ���������CH3OH���������ԼΪ________���ðٷ�����ʾ��С�������1λ����
CH3OH(g) ��H=��90.1 kJ��mol��1��ToC���÷�Ӧ��Kp=6.0��10-3kPa-2����ƽ���ѹ����ƽ��Ũ������ƽ�ⳣ������ѹ= ��ѹ�����ʵ��������������¶��µ�ij�����У�����ʼ����2molH2��1molCO��ƽ��ʱ�״���ƽ���ѹp(CH3OH)=24.0kPa����ƽ��ʱ���������CH3OH���������ԼΪ________���ðٷ�����ʾ��С�������1λ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������C9H10O2������Ϊ��Ϣ��������������һ����ɫ��Һ�壬������ˮ������ˮ����ζ������������ˮ�㾫�����쾫�ͣ���������ʳƷ��ҵ�У�Ҳ�������л��ϳ��м��壬�ܼ��ȡ����Ʊ�����Ϊ��
��֪��
���� | ��Է������� | ��ɫ��״̬ | �е�(��) | �ܶ�(g��cm-3) |
������ | 122 | ��ɫƬ״���� | 249 | 1.2659 |
���������� | 150 | ��ɫ����Һ�� | 212.6 | 1.05 |
�Ҵ� | 46 | ��ɫ����Һ�� | 78.3 | 0.7893 |
������ | 84 | ��ɫ����Һ�� | 80.8 | 0.7318 |
��������100���Ѹ��������
ʵ�鲽�����£�
����Բ����ƿ�м���12.20 g�����ᣬ25 mL 95%���Ҵ�����������20 mL�������Լ�4 mLŨ���ᣬ��Ͼ��Ȳ������ʯ������ͼ��ʾװ�������������¶���65��70����Ȼ���2 h�����÷�ˮ�����Ϸ����ȥ��Ӧ���ɵ�ˮ��������������Ҵ���
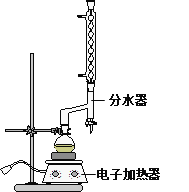
�ڷ�Ӧ�������������ų���ˮ����Һ��ر��������������ȣ�����ˮ�����ռ�����Һ�岻���������ӣ�ֹͣ���ȡ�
�۽���ƿ�ڷ�ӦҺ����ʢ������ˮ���ձ��У���������Na2CO3����Һ�������ԡ��÷�Һ©���ֳ��л��㣬ˮ����25 mL������ȡ��Һ��Ȼ��ϲ����л��㣬�����Ȼ��ƣ����ã����ˣ�����Һ�����������������Ѻͻ�����������£�����210��213�����֡�
�ܼ���ϸ�ò�Ʒ���Ϊ12.86 mL��
�ش��������⣺
��1���ڸ�ʵ���У�Բ����ƿ���ݻ����ʺϵ���_________��������ȷѡ��ǰ����ĸ����
A��25 mL B��50 mL C��100 mL D��250 mL
��2���������ʹ�÷�ˮ�����Ϸ����ȥˮ��Ŀ����_____________________��
��3���������Ӧ������ֵ��¶���____________��
A��65��70�� B��78��80�� C��85��90�� D��215��220��
��4������ۼ���Na2CO3��������______________________����Na2CO3���벻�㣬��֮������ʱ��������ƿ�пɼ����������ɣ������������ԭ����____________��
��5�����ڲ�����е���ȡ��Һ����������ȷ����__________��
A��ˮ��Һ�м������ѣ�ת������Һ©���У����ϲ���������Һ©����ת������������ҡ
B����ҡ���κ����Һ©���ϿڵIJ���������
C����������ҡ���������ֳַ�Һ©�����ô�Һ��ֲ�
D���ų�Һ��ʱ��Ӧ���Ͽڲ������������ϵİ��۶�©�����ϵ�С��
��6�����㱾ʵ��IJ���Ϊ_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ʷ����У�ǰ�߰������ߵ���
A.�����������B.����������
C.��Һ�� ����D.��Һ�� ��ɢϵ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com