
【题目】某市场销售的食用精制盐包装袋上有如下说明:
产品标准 | GB5461 |
产品等级 | 一级 |
配 料 | 食盐、碘酸钾、抗结剂 |
碘含量(以I计) | 20~50mg/kg |
分装时期 | |
分装企业 |
(1)碘酸钾与碘化钾在酸性条件下发生反应的化学方程式为:_______________________。
(2)上述反应生成的I2可用四氯化碳检验。向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。Na2SO3稀溶液与I2反应的离子方程式是 ____________________________。
(3)已知:I2+2S2O32-=2I-+S4O62-。某学生测定食用精制盐的碘含量,其步骤为:
a. 准确称取wg食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol·L-1的Na2S2O3溶液10.0mL,恰好反应完全。
①判断c中反应恰好完全依据的现象是_______________________。
②b中反应所产生的I2的物质的量是____________mol。
③根据以上实验和包装袋说明,所测精制盐的碘含量是__________________ mg/kg。(以含w的代数式表示)
【答案】KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2OI2+SO32-+H2O=2I-+SO42-+2H+滴最后一滴溶液,由蓝色恰好变为无色,且半分钟内不变色1.0×10-5423/w
【解析】
(1)碘酸钾中碘元素由+5价降为0价,碘化钾中碘元素由-1价升高为0价,根据化合价升降法配平方程式为KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O;
(2)Na2SO3溶液与I2反应生成硫酸钠和氢碘酸,反应的离子方程式是I2+SO32-+H2O=2I-+SO42-+2H+;
(3)①以淀粉做指示剂的时候,当I2反应完后,恰好完全反应,所以溶液由蓝色变为无色。故判断c中反应恰好完全依据的现象是滴最后一滴溶液,由蓝色恰好变为无色,且半分钟内不变色;②反应后生成I2的物质的量为![]() ;精制盐的含碘量为
;精制盐的含碘量为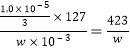 。
。


科目:高中化学 来源: 题型:
【题目】短周期五种元素A、B、C、D、E的原子序数依次增大。A、B、C的单质在常温下都呈气态,C原子最外层电子数是电子层数的3倍,C和E位于同主族。1molDAx与足量的A2C反应生成44.8L(标准状况)G气体。A、B的单质依次为G、T,在密闭容器中充入一定量的G、T,一定条件下发生反应G+T→W(未配平),测得各物质的浓度如表所示。
物质 | T | G | W |
10min时,c/(mol/L) | 0.5 | 0.8 | 0.2 |
20min时,c/(mol/L) | 0.3 | 0.2 | 0.6 |
回答下列问题:
(1)A、B、C能组成既含离子键又含共价键的化合物,该化合物的化学式为_________。
(2)B、C、D、E的简单离子中,离子半径由大到小排序为__________。(用离子符号表示)
(3)J、L是由A、B、C、E四种元素组成的两种常见酸式盐,J、L混合可产生有刺激性气味的气体,写出这两种溶液发生反应的离子方程式_______;J、L中能使酸性高锰酸钾溶液退色的是_______(填化学式)。
(4)B2A4-C2碱性燃料电池放电效率高。该电池放电时生成B2和A2C,正极反应式为_____;电池工作一段时间后,电解质溶液的pH_____(填“增大”“减小”或“不变”)。
(5)由A、B、C、D四种元素组成的单质、化合物在一定条件下的转化关系(部分条件和产物已省略)如图所示,已知M耐高温。
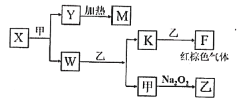
①X的电子式为______;W的结构式为________。
②已知W与乙反应生成K和甲是某重要化工生产步骤之一,提高其反应速率的方法除增大反应物浓度、增大压强外,还有______、______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝广泛应用于电子陶瓷等工业领域。在一定条件下,AlN可通过以下反应合成:Al2O3+N2+3C![]() 2AlN+3CO。有关该反应下列叙述正确的是
2AlN+3CO。有关该反应下列叙述正确的是
A. 上述反应中,N2是还原剂,Al2O3是氧化剂
B. 上述反应中,每生成1 mol AlN需转移3 mol电子
C. AlN中氮的化合价为+3
D. AlN的摩尔质量为41 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】判断下列过程的ΔH和ΔS,用“> 0”或“< 0”来表示
化学方程式 | ΔH | ΔS |
H2O(l)→H2O(g) | _________ | ________ |
CaCO3(s) == CaO (s) + CO2(g) | _______ | _______ |
NaOH(s)== Na+(aq)+OH-(aq) | _______ | ________ |
N2(g)+3H2(g) | ______ | ________ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质的叙述正确的是( )
A.液态HCl不导电,所以HCl是非电解质
B.熔融NaCl可以导电,所以NaCl是电解质
C.液态Cl2不导电,所以Cl2是非电解质
D.SO2的水溶液能够导电,所以SO2是电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇能发生如下反应:
①CH3CH2OH+3O2![]() 2CO2+3H2O;
2CO2+3H2O;
②2Cu+O2 ![]() 2CuO,CH3CH2OH+CuO
2CuO,CH3CH2OH+CuO![]() CH3CHO+H2O+Cu。
CH3CHO+H2O+Cu。
由以上反应不能得出的结论是
A. 由反应①②可知,条件不同,乙醇与O2反应的产物不同
B. 由反应②可知,Cu是乙醇氧化生成乙醛的催化剂
C. 由反应①可知,乙醇燃烧时,碳碳键、碳氢键、氢氧键均断裂
D. 由反应②可知,乙醇氧化为乙醛时,只断开氢氧键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列根据反应原理设计的应用,不正确的是
A. CO32-+H2O![]() HCO3-+OH-:用热的纯碱溶液清洗油污
HCO3-+OH-:用热的纯碱溶液清洗油污
B. A13++3H2O![]() Al(OH)3(胶体)+3H+:明矾净水
Al(OH)3(胶体)+3H+:明矾净水
C. TiCl4+(x+2)H2O(过量)![]() TiO2·xH2O↓+4HCl:制备TiO2纳米粉
TiO2·xH2O↓+4HCl:制备TiO2纳米粉
D. SnCl2+H2O![]() Sn( OH)Cl↓+HCl配制氯化亚锡溶液时加入氢氧化钠溶液
Sn( OH)Cl↓+HCl配制氯化亚锡溶液时加入氢氧化钠溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用锌和稀硫酸反应制取氢气。在2mol/L的足量稀硫酸跟一定量的锌片反应制取氢气的实验中,为加快反应速率,又不影响生成氢气的总量,可以采用的方法是( )
A.适当升高温度B.加入几滴硫酸铜溶液
C.再加入少量浓硝酸D.加入适量的氯化钠溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com