
【题目】利用下列装置(部分仪器已省略),能顺利完成对应实验的是
A.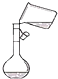 向容量瓶中转移
向容量瓶中转移
B.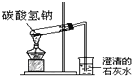 碳酸氢钠受热分解
碳酸氢钠受热分解
C.![]() 制氢氧化亚铁
制氢氧化亚铁
D.![]() 分离花生油和水
分离花生油和水
【答案】D
【解析】
A.根据移液时通过玻璃棒引流进行分析;
B.根据试管加热固体的方法进行分析;
C.根据制氢氧化亚铁的方法进行分析;
D.根据萃取、分液的方法来解答。
![]() 为了防止溶液洒到瓶外,移液时应通过玻璃棒引流,A错误;
为了防止溶液洒到瓶外,移液时应通过玻璃棒引流,A错误;
B.加热碳酸氢钠有水生成,倒流会引起试管炸裂,所以加热固体药品时底部要高于试管口,防止生成的水蒸气冷却后倒流而炸裂试管,B错误;
C.氢氧化亚铁不稳定,易被氧化生成氢氧化铁,所以制取氢氧化亚铁时要隔绝空气,胶头滴管要伸入液面下,C错误;
D.互不相溶的液体采用分液方法分离,漏斗的下端紧贴烧杯内壁,下层液体从下端放出,上层液体从上口倒出,花生油和水不互溶,可以采用分液方法分离,D正确;
故合理选项是D。


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖授予约翰·古德伊纳夫、斯坦利·惠廷厄姆和吉野彰三位科学家,以表彰他们在锂电池领域所做出的巨大贡献。请回答下列问题:
(1)LiCoO2、LiFePO4常用作锂离子电池的正极材料。基态Co原子核外电子排布式为___,基态磷原子中,电子占据的最高能层符号为___;该能层能量最高的电子云在空间有___个伸展方向,原子轨道呈___形。
(2)[Co(NO3-)4]2-中Co2+的配位数为4,配体中N的杂化方式为__,该配离子中各元素的第一电离能由小到大的顺序为___(填元素符号),1mol该配离子中含σ键数目为___NA。
(3)LiFePO4属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如图所示:
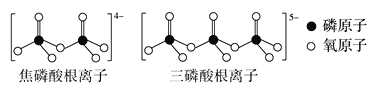
这类磷酸根离子的化学式可用通式表示为___(用n代表P原子数)。
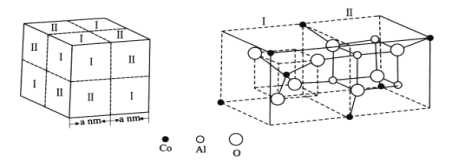
(4)钴蓝晶体结构如图,该立方晶胞由4个I型和4个Ⅱ型小立方体构成,其化学式为___,晶体中Al3+占据O2-形成的___(填“四面体空隙”或“八面体空隙”)。NA为阿伏加德罗常数的值,钴蓝晶体的密度为___g·cm-3(列计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物W(C16H14O2)用作调香剂、高分子材料合成的中间体等,制备W的一种合成路线如下:
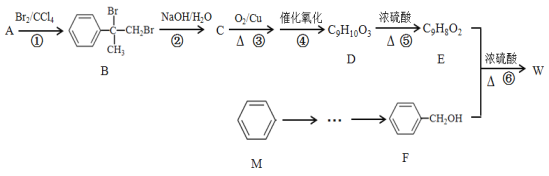
已知: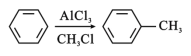
请回答下列问题:
(1)F的化学名称是_______,⑤的反应类型是_______。
(2)E中含有的官能团是_______(写名称),E在一定条件下聚合生成高分子化合物,该高分子化合物的结构简式为_______。
(3)E + F→W反应的化学方程式为_______。
(4)与A含有相同官能团且含有苯环的同分异构体还有_______种(不含立体异构),其中核磁共振氢谱为六组峰,且峰面积之比为1∶1∶2∶2∶2∶2的结构简式为____。
(5)参照有机物W的上述合成路线,写出以M和CH3Cl为原料制备F的合成路线(无机试剂任选)_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,在H2CO3溶液中逐滴加入NaOH溶液,溶液中H2CO3、HCO3-和CO32-的物种分布分数![]() (X)=
(X)=![]() 与pH的关系如图所示:
与pH的关系如图所示:

下列说法正确的是
A. 反应HCO3-![]() H++CO32-的lgK=-6.4
H++CO32-的lgK=-6.4
B. pH═8的溶液中:c(Na+)>c(HCO3-)
C. NaHCO3溶液中滴入少量盐酸至溶液显中性:c(Na+)═c(Cl-)
D. 向pH=6.4的溶液中滴加NaOH溶液至pH=8,主要发生的离子反应:HCO3-+OH-═CO32-+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用铂电极电解CuSO4和KNO3的混合液500mL,经过一段时间后,两极均得到标况下11.2L气体,则原混合液中CuSO4的物质的量浓度为
A.0.5mol·L-B.0.8mol·L-1
C.1.0mol·L-1D.1.5mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.标准状况下,11.2LNH3和HCl的混合气体中的分子数为0.5NA
B.0.1molC2H6O分子中含有C—H键的数目为0.5NA
C.0.1molCl2通入适量水中,转移的电子数为0.1NA
D.17gH2O2与17gH2S所含的电子数均为9NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,通电5min后,第③极增重2.16g,同时在A池中收集到标准状况下的气体224mL,A池中混合液的体积为200mL(电解前后体积视为不变),求通电前A池中原混合溶液Cu2+的浓度。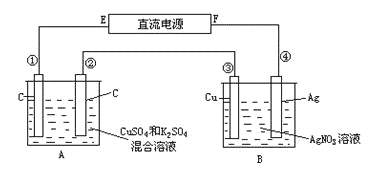
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示戊烷燃烧热的热化学方程式正确的是( )
A. C5H12(l)+8O2(g)![]() 5CO2(g) +6H2O(l) ΔH=-3 540 kJ·mol-1
5CO2(g) +6H2O(l) ΔH=-3 540 kJ·mol-1
B. C5H12(l)+8O2(g)![]() 5CO2(g)+6H2O(g) ΔH=-3 540 kJ·mol-1
5CO2(g)+6H2O(g) ΔH=-3 540 kJ·mol-1
C. C5H12(l)+8O2(g)![]() 5CO2(g)+6H2O(g) ΔH=+3 540 kJ·mol-1
5CO2(g)+6H2O(g) ΔH=+3 540 kJ·mol-1
D. C5H12(l)+8O2(g)![]() 5CO2(g)+6H2O(l) ΔH=+3 540 kJ·mol-1
5CO2(g)+6H2O(l) ΔH=+3 540 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟化铬可用作毛织品防蛀剂、卤化催化剂、大理石硬化及着色剂。以铬云母矿石(含4.5%Cr2O3,还含Fe2O3、FeO、MgO、SiO2)为原料制备氟化铬的工艺流程如下。
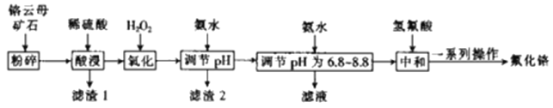
下表列出了相关金属离子生成氢氧化物沉淀的pH:
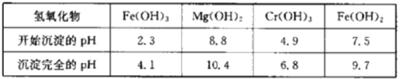
请回答下列问题:
(1)Fe2O3、MgO、FeO、SiO2中属于碱性氧化物的有___种。
(2)将铬云母矿石粉碎的目的是___。
(3)滤渣1主要成分的用途是___。(写一种)
(4)Cr2O3与稀硫酸反应的化学方程式为___。
(5)第一次滴加氨水调节pH范围为___。
(6)第二次滴加氨水调节pH为6.8~8.8的目的是___,Cr(OH)3与Al(OH)3一样具有两性,若第二次滴加的氨水改为NaOH溶液,生成的Cr(OH)3会部分溶解,写出Cr(OH)3溶解的离子方程式:___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com