


 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、ω(
| ||
D、ω(
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HClO4?H++ClO4- |
| B、H2CO3?2H++CO32- |
| C、HCO3-+H2O?CO32-+H3O+ |
| D、NH3?H2O═NH4++OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
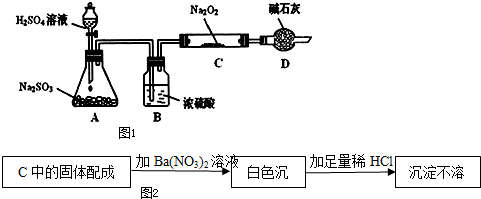
 某实验小组欲探究Na2CO3和NaHCO3的性质,发现实验室里盛放两种固体的试剂瓶丢失了标签.于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究.
某实验小组欲探究Na2CO3和NaHCO3的性质,发现实验室里盛放两种固体的试剂瓶丢失了标签.于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究.| 实验方案 | 预测现象 | 预测依据 |
| 操作1:向2mL Na2CO3溶液中滴加1mL 0.5mol?L-1CaCl2溶液 | 有白色沉淀 | Na2CO3溶液中的CO32-浓度较大,能与CaCl2发生反应 |
| 操作2:向2mL NaHCO3溶液中滴加1mL 0.5mol?L-1CaCl2溶液 | 无白色沉淀 | NaHCO3溶液中的CO32-浓度很小,不能与CaCl2反应. |
查看答案和解析>>
科目:高中化学 来源: 题型:
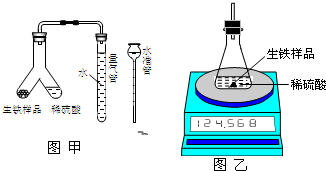 为测定某生铁(假设仅含Fe和C)粉末状样品中铁的质量分数,某化学研究性学习小组设计有关方案进行如下实验.
为测定某生铁(假设仅含Fe和C)粉末状样品中铁的质量分数,某化学研究性学习小组设计有关方案进行如下实验.| 反应前:整套装置+ 稀硫酸质量/g | 反应前: 生铁样品质量/g | 反应后:整套装置+ 锥形瓶中剩余物的质量/g |
| a | m | b |
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 加入生铁样品的质量/g | 1.43 | 2.86 | 8.58 |
| 生成气体的体积/L(标准状况) | 0.56 | 1.12 | 2.24 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、③④⑤⑥ | B、②③④⑥ |
| C、①③④⑤ | D、①③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、Mg2+的结构示意图: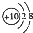 |
B、Na2S的电子式: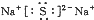 |
| C、氨气的空间结构:三角形 |
| D、乙烯的结构简式:(CH2)2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com