
【题目】下图中 A、B、C、D 分别是三种烃的分子结构,请回答下列问题:
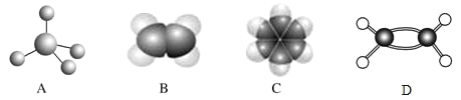
(1)上图中 D 是有机物分子的_____模型;
(2)烃 A 及其同系物的分子式符合通式_____(碳原子个数用 n 表示),当 n=6 时的同分异构体数目为_____(填数字)种;
(3)上述三种有机物烃中,所有原子均共平面的是_________(填有机物的名称);
(4)下列关于烃 C 的叙述正确的是_____(填序号)。
A.分子式为 C6H6,它不能使酸性 KMnO4 溶液褪色,属于饱和烃
B.从分子结构看,C 分子中含有碳碳双键,属于烯烃
C.烃 C 的同系物二甲苯(C8H10)有三种不同的结构,均属于芳香烃
D.烃 C 中加入溴水,充分振荡,静置,下层无色
(5)分别写出 B 使溴水褪色、C 的溴代反应的化学方程式____________、_____________,并指明反应类型:________________、______________
(6)C 的同系物甲苯与足量氢气加成后的产物(甲基环己烷)的一氯代物有_____种。
【答案】球棍 CnH2n+2(n≥1) 5 乙烯、苯 CD CH2=CH2+Br2→CH2Br—CH2Br ![]() +Br2
+Br2![]()
![]() +HBr 加成反应 取代反应 5
+HBr 加成反应 取代反应 5
【解析】
根据图示,A为甲烷分子的球棍模型,B为乙烯分子的比例模型,C为苯分子的球棍模型,D为乙烯分子的球棍模型,根据以上有机物的结构与性质分析解答下列问题。
(1)根据分析D为乙烯分子的球棍模型;
(2) A为甲烷,及其同系物属于烷烃,烷烃的分子式通式CnH2n+2(n≥1);当 n=6 时,该烃的分子式为C6H14的烷烃,己烷的同分异构体分别为:主链为6个碳原子时CH3CH2CH2CH2CH2CH3;主链为5个碳原子时:(CH3)2CHCH2CH2CH3、CH3CH2CH(CH3)CH2CH3;主链为4个碳原子时:(CH3)2CHCH(CH3)2、(CH3)3CCH2CH3,共有5种;
(3)上述三种有机物烃中,A为甲烷是正四面体结构,所有原子不在同一平面,B为乙烯,是平面结构,所有原子在同一平面,C为苯,是平面结构,所有原子在同一平面,则所有原子均共平面的是乙烯、苯;
(4) C为苯,苯分子结构中,不含碳碳单键和双键,是一种介于单键与双键之间的一种特殊键,在一定条件下能发生加成反应、取代反应、氧化反应,但不能使酸性高锰酸钾溶液褪色;
A.苯分子式为 C6H6,它不能使酸性 KMnO4 溶液褪色,能发生加成反应,则属于不饱和烃,故A错误;
B.苯分子结构中,不含碳碳单键和双键,是一种介于单键与双键之间的一种特殊键,属于芳香烃,故B错误;
C.苯分子的结构为平面的正六边形,两个甲基在苯环上有邻间对三个位置结构,分别为邻二甲苯、间二甲苯、对二甲苯,含有苯环的烃类均属于芳香烃,故C正确;
D.苯与溴水不反应,由于溴水中的溴单质在苯中的溶解度较大,故向溴水中加入苯,充分混合振荡静置后,溴单质会转移至溶解度较大的苯中,由于苯的密度比水小,且不溶于水, 溶液分层,上层是苯层,由于溶解溴单质为橙色,下层为水层,几乎无色,故D正确;
答案选CD;
(5)乙烯结构中含有碳碳双键,和溴水发生加成反应,使溴水褪色,方程式为CH2=CH2+Br2→CH2Br—CH2Br;苯和溴单质在溴化铁作催化剂的作用下发生取代反应,生成溴苯和溴化氢,化学方程式为![]() +Br2
+Br2![]()
![]() +HBr;
+HBr;
(6)苯的同系物甲苯与足量氢气加成后的产物(甲基环己烷)由一个甲基和六元环构成,甲基环己烷中有5种不同环境的氢原子,如图所示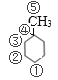 ,则其一氯代物由5种。
,则其一氯代物由5种。


 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:
【题目】在探究影响化学反应速率的因素时,将H2C2O4溶液滴入KMnO4酸性溶液中,一段时间后,溶液突然变成无色,发生反应:KMnO4+H2C2O4+H2SO4![]() K2SO4+MnSO4+CO2+H2O(没有配平)。下列有关说法错误的是
K2SO4+MnSO4+CO2+H2O(没有配平)。下列有关说法错误的是
A. H2C2O4中C的化合价为+3
B. 每生成22.4 L(标况)CO2,转移电子2 mol
C. 该反应中,氧化剂与还原剂物质的量之比为2 :5
D. 溶液突然褪色的原因是产物MnSO4对该反应有催化作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池装置如图所示,电池总反应为 2Ag + Cl2 = 2AgCl。已知阳离子交换膜只允许阳离子通过,阴离子不能通过,离子交换过程中溶液电荷守恒。下列说法正确的是
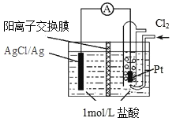
A.正极反应式为 AgCl + e—= Ag + Cl—
B.放电时,交换膜右侧溶液中有大量白色沉淀生成
C.若用 NaCl 溶液代替盐酸,则电池总反应随之改变
D.当外电路中转移 0.1mol e—时,阳离子交换膜左侧溶液中约减少0.2mol 离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有![]() (a).
(a). ![]() (b).
(b). ![]() (c)的分式均为C5H6,下列有关叙述正确的是
(c)的分式均为C5H6,下列有关叙述正确的是
A. 符合分子式为C5H6的同分异构体只有a、b、c三种
B. a、b、c的一氯代物都只有三种
C. a、b、c都能使溴的CCl4溶液褪色,且褪色原理相同
D. a、b、c分子中的5个碳原子一定都处于同一个平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸乙酯是无色具有水果香味的液体,沸点为 77.2 ℃,实验室某次制取乙酸乙酯用冰醋酸、乙醇、浓硫酸、饱和碳酸钠溶液以及极易与乙醇结合的氯化钙溶液。主要装置如下图所示:
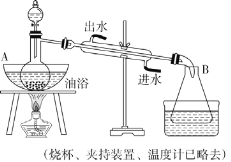
实验步骤:
①先向 A 中的蒸馏烧瓶中注入少量乙醇和浓硫酸后摇匀,再将剩下的所有乙醇和冰醋酸注入分液漏斗里待用。
②加热油浴保温。
③将分液漏斗中的液体缓缓滴入蒸馏烧瓶里,
调节加入速率,使蒸出酯的速率与进料速率大体相等,直到加料完成。
④保持油浴温度一段时间,至不再有液体馏出后,停止加热。
⑤取下 B 中的锥形瓶,将一定量饱和 Na2CO3 溶液分批少量多次地加到馏出液里,边加边振荡,至无气泡产生为止。
⑥将⑤的液体混合物用分液漏斗分液,弃去水层。
⑦将饱和 CaCl2 溶液(适量)加入分液漏斗中,振荡一段时间后静置,放出水层(废液)。
⑧分液漏斗里得到的是初步提纯的乙酸乙酯粗品。
(1)实验中浓硫酸的主要作用是_____。
(2)用饱和 Na2CO3 溶液洗涤粗酯的目的是_____。用饱和 CaCl2溶液洗涤粗酯的目的是_____。
(3)在步骤⑧所得的粗酯里还含有的杂质是_____。
(4)写出本实验制取乙酸乙酯的化学方程式:_____。
(5)若用 46g 乙醇与 30g 醋酸反应,如果实际产率是理论产率的 65%,试计算可得到的乙酸乙酯的质量为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着时代的发展,绿色环保理念越来越受到大家的认同,变废为宝是我们每一位公民应该养成的意识。某同学尝试用废旧的铝制易拉罐作为原材料、采用“氢氧化铝法”制取明矾晶体并进行一系列的性质探究。
制取明矾晶体主要涉及到以下四个步骤:
第一步:铝制品的溶解。取一定量铝制品,置于250mL锥形瓶中,加入一定浓度和体积的强碱溶液,水浴加热(约93℃),待反应完全后(不再有氢气生成),趁热减压抽滤,收集滤液于250mL烧杯中;
第二步:氢氧化铝沉淀的生成。将滤液重新置于水浴锅中,用3 mol/L H2SO4调节滤液pH至8~9,得到不溶性白色絮凝状Al(OH)3,减压抽滤得到沉淀;
第三步:硫酸铝溶液的生成。将沉淀转移至250mL烧杯中,边加热边滴入一定浓度和体积的H2SO4溶液;
第四步:硫酸铝钾溶液的形成。待沉淀全部溶解后加入一定量的固体K2SO4,将得到的饱和澄清溶液冷却降温直至晶体全部析出,减压抽滤、洗涤、抽干,获得产品明矾晶体[KAl(SO4)2·12H2O,M=474g/mol]。
回答下列问题:
(1)第一步铝的溶解过程中涉及到的主要反应的离子方程式为__________________________
(2)为了加快铝制品的溶解,应该对铝制品进行怎样的预处理:________________________
(3)第四步操作中,为了保证产品的纯度,同时又减少产品的损失,应选择下列溶液中的___(填选项字母)进行洗涤,实验效果最佳。
A.乙醇 B.饱和K2SO4溶液 C.蒸馏水 D.1:1乙醇水溶液
(4)为了测定所得明矾晶体的纯度,进行如下实验操作:准确称取明矾晶体试样4.0g于烧杯中,加入50mL 1mol/L盐酸进行溶解,将上述溶液转移至100mL容量瓶中,稀释至刻度线,摇匀;移取25.00 mL溶液干250 mL锥形瓶中,加入30 mL 0.10mol/L EDTA-2Na标准溶液,再滴加几滴2D二甲酚橙,此时溶液呈黄色;经过后续一系列操作,最终用0.20 mol/L锌标准溶液滴定至溶液由黄色变为紫红色,达到滴定终点时,共消耗5.00 mL锌标准溶液。滴定原理为H2Y2-+Al3+→AlY-+2H+,H2Y2-(过量)+Zn2+→ZnY2-+2H+(注:H2Y2-表示EDTA-2Na标准溶液离子)。则所得明矾晶体的纯度为_________%。
(5)明矾除了可以用作人们熟悉的净水剂之外,还常用作部分食品的膨松剂,例如油条(饼)的制作过程需要加入一定量的明矾,请简述明矾在面食制作过程作膨松剂的原理:_______
(6)为了探究明矾晶体的结晶水数目及分解产物,在N2气流中进行热分解实验,得到明矾晶体的热分解曲线如图所示(TG%代表的是分解后剩余固体质量占样品原始质量的百分率,失重百分率=![]() ×100%):
×100%):
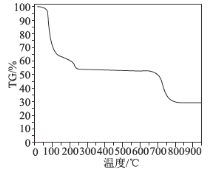
根据TG曲线出现的平台及失重百分率,30~270℃范围内,失重率约为45.57%,680~810℃范围内,失重百分率约为25.31%,总失重率约为70.88%,请分别写出所涉及到30~270℃、680~810℃温度范围内这两个阶段的热分解方程式:___________、_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数,下列说法正确的是( )
A.6.2g白磷分子(P4)中含P-P键数为0.05NA
B.1mol CH3+含电子数为8NA
C.标准状况下,22.4LSO3中含原子数为4NA
D.常温常压下,11.2LCO2气体通过足量Na2O2充分反应,转移电子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】液态化合物AB会发生微弱的自身电离,电离方程式为AB![]() A++B-,在不同温度下其平衡常数为K(25 ℃)=1.0×10-14,K(35 ℃)=2.1×10-14。则下列叙述正确的是 ( )。
A++B-,在不同温度下其平衡常数为K(25 ℃)=1.0×10-14,K(35 ℃)=2.1×10-14。则下列叙述正确的是 ( )。
A.c(A+)随温度升高而降低
B.在35 ℃时,c(A+)>c(B-)
C.AB的电离程度(25 ℃)>(35 ℃)
D.AB的电离是吸热过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D四种短周期元素,A分别与B、C、D结合生成甲、乙、丙三种化合物,且甲、乙、丙三分子中含有的质子数都为10,C、D结合生成化合物丁。有关元素的单质和甲、乙、丙、丁四种化合物的转化关系如下图所示:
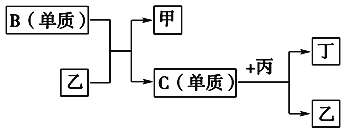
(1)写出B+乙―→甲+C的化学反应方程式______________________________________。
(2)根据以上条件可以确定A、B、C、D四种元素中的三种,不能被确定的第四种元素是________(填写序号)。
①A ②B ③C ④D
(3)依据下列条件可以进一步确定上述第四种元素:
①甲与丙以及乙与丙均能够发生反应,②甲、丙都是无色、有刺激性气味的物质。
据此,请回答下列问题:
写出上述第四种元素在周期表中的位置________________。写出C+丙―→乙+丁的化学反应方程式_________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com