
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЖдБШБЅКЭСДЬўЁЂВЛБЅКЭСДЬўЕФНсЙЙКЭаджЪЃЌБНЕФЖРЬиаджЪОпЬхРДЫЕЪЧ(ЁЁЁЁ)
A.ФббѕЛЏЁЂвзМгГЩЁЂФбШЁДњ
B.ФббѕЛЏЁЂФмМгГЩЁЂвзШЁДњ
C.взбѕЛЏЁЂвзМгГЩЁЂФбШЁДњ
D.взбѕЛЏЁЂвзМгГЩЁЂФбШЁДњ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
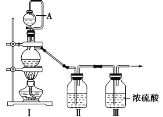
ЁОЬтФПЁПAЪЧгЩЕМШШВФСЯжЦГЩЕФУмБеШнЦїЃЌBЪЧвЛФЭЛЏбЇИЏЪДЧввзгкДЋШШЕФЦјЧђЃЎЙиБеK2ЃЌНЋЕШСПЧвЩйСПЕФNO2ЭЈЙ§K1ЁЂK3ЗжБ№ГфШыAЁЂBжаЃЌЗДгІЦ№ЪМЪБЃЌAЁЂBЕФЬхЛ§ЯрЭЌЃЎ(вбжЊЃК2NO2(g) ![]() N2O4(g)ЁЁІЄHЃМ0)
N2O4(g)ЁЁІЄHЃМ0)
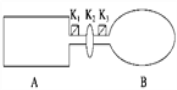
ЃЈ1ЃЉвЛЖЮЪБМфКѓЃЌЗДгІДяЕНЦНКтЃЌДЫЪБAЁЂBжаЩњГЩN2O4ЕФЫйТЪЪЧvA______vB(ЬюЁАЃОЁБЁЂЁАЃМЁБЛђЁАЃНЁБ)ЃЛШєДђПЊЛюШћK2ЃЌЦјЧђBНЋ______(ЬюЁАБфДѓЁБЁЂЁАБфаЁЁБЛђЁАВЛБфЁБ)ЃЎ
ЃЈ2ЃЉЙиБеЛюШћK2ЃЌШєдкAЁЂBжадйГфШыгыГѕЪМСПЯрЕШЕФNO2ЃЌдђДяЕНЦНКтЪБЃЌNO2ЕФзЊЛЏТЪІСAНЋ________(ЬюЁАдіДѓЁБЁЂЁАМѕаЁЁБЛђЁАВЛБфЁБ)ЃЛШєЗжБ№ЭЈШыЕШСПЕФФЪЦјЃЌдђДяЕНЦНКтЪБЃЌAжаNO2ЕФзЊЛЏТЪНЋ________ЃЌBжаNO2ЕФзЊЛЏТЪНЋ______(ЬюЁАБфДѓЁБЁЂЁАБфаЁЁБЛђЁАВЛБфЁБ)ЃЎ
ЃЈ3ЃЉЪвЮТЯТЃЌШєAЁЂBЖМБЃГжЬхЛ§ВЛБфЃЌНЋAЬзЩЯвЛИіОјШШВуЃЌBгыЭтНчПЩвдНјааШШДЋЕнЃЌдђДяЕНЦНКтЪБЃЌ______жаЕФбеЩЋНЯЩюЃЎ
ЃЈ4ЃЉШєдкШнЦїAжаГфШы4.6 gЕФNO2ЃЌДяЕНЦНКтКѓШнЦїФкЛьКЯЦјЬхЕФЦНОљЯрЖдЗжзгжЪСПЮЊ57.5ЃЌдђЦНКтЪБN2O4ЕФЮяжЪЕФСПЮЊ___________________ЃЎ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПШчЭМЕуЕЮАхЩЯЫФИіШмвКМфЗДгІЖдгІЕФРызгЗНГЬЪНЪщаДе§ШЗЕФЪЧ
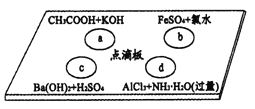
A. aЗДгІЃКHЃЋЃЋOHЃ![]() H2O
H2O
B. bЗДгІЃКFe2ЃЋЃЋCl2![]() Fe3ЃЋЃЋ2ClЃ
Fe3ЃЋЃЋ2ClЃ
C. cЗДгІЃКBa2ЃЋЃЋ![]() ЃЋHЃЋЃЋOHЃ
ЃЋHЃЋЃЋOHЃ![]() BaSO4Ё§ЃЋH2O
BaSO4Ё§ЃЋH2O
D. dЗДгІЃКAl3ЃЋЃЋ3NH3ЁЄH2OЃНAlЃЈOHЃЉ3Ё§ЃЋ3![]()
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСадзгађЪ§ЕФдЊЫиЃЌБЫДЫжЎМфФмаЮГЩРызгМќЕФЪЧЃЈ ЃЉ
A. 1КЭ16 B. 6КЭ8 C. 9КЭ11 D. 1КЭ17
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯжгаAЁЂBЁЂCЁЂDЁЂEЁЂFСљжжЖЬжмЦкжїзхдЊЫиЃЌдзгађЪ§вРДЮдіДѓЁЃвбжЊAЕФЦјЬЌЧтЛЏЮяФмгыЦфзюИпМлбѕЛЏЮяЕФЫЎЛЏЮяЗДгІЕУЕНвЛжжРызгЛЏКЯЮяЃЌBЕФвЛжжЕЅжЪОпгаЩБОњЯћЖОЕФзїгУЃЌCЃЋКЭD3+ЕФЕчзгВуНсЙЙЯрЭЌЃЌEЕФжїзхађЪ§ЪЧЦфжмЦкађЪ§ЕФ2БЖЁЃ
ЃЈ1ЃЉFдкдЊЫижмЦкБэжаЕФЮЛжУЪЧ__________________ЁЃ
ЃЈ2ЃЉЩЯЪідЊЫиаЮГЩЕФМђЕЅРызгжаЃЌАыОЖзюДѓЕФЪЧ____________(ЬюРызгЗћКХ)ЁЃ
ЃЈ3ЃЉгЩЩЯЪідЊЫижаЕФвЛжжЛђМИжжзщГЩЕФЮяжЪМзПЩвдЗЂЩњШчЯТЗДгІЃК

ЂйШєБћОпгаЦЏАзадЃЌдђМзКЭЫЎЗДгІЕФРызгЗНГЬЪНЮЊ__________________________ЁЃ
ЂкШєввЕФЫЎШмвКЪЧЧПМюадШмвКЃЌЮяжЪБћЮЊBЕФвЛжжЕЅжЪЃЌдђМзжаКЌгаЕФЛЏбЇМќЕФРраЭЮЊ________ЃЌDЕФЕЅжЪгыввЕФЫЎШмвКЗДгІЕФРызгЗНГЬЪНЮЊ_________________ЁЃ
ЂлШєМзЮЊDКЭEаЮГЩЕФЖўдЊЛЏКЯЮяЃЌЮяжЪБћЪЧЦјЬхЃЌдђБћЕФНсЙЙЪНЮЊ___________ЃЛЮяжЪввЮЊАзЩЋГСЕэЃЌЦфЛЏбЇЪНЮЊ______________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЙЄвЕКЯГЩАБЕФЗДгІШчЯТЃК3H2+N2![]() 2NH3ЁЃФГЮТЖШЯТЃЌдкШнЛ§КуЖЈЮЊ2.0 LЕФУмБеШнЦїжаГфШы2.0 mol N2КЭ2.0 mol H2ЃЌвЛЖЮЪБМфКѓЗДгІДяЦНКтзДЬЌЃЌЪЕбщЪ§ОнШчЯТБэЫљЪОЃК
2NH3ЁЃФГЮТЖШЯТЃЌдкШнЛ§КуЖЈЮЊ2.0 LЕФУмБеШнЦїжаГфШы2.0 mol N2КЭ2.0 mol H2ЃЌвЛЖЮЪБМфКѓЗДгІДяЦНКтзДЬЌЃЌЪЕбщЪ§ОнШчЯТБэЫљЪОЃК
t/s | 0 | 50 | 150 | 250 | 350 |
n(NH3)/mol | 0 | 0.24 | 0.36 | 0.40 | 0.40 |
(1)0ЁЋ50 sФкЕФЦНОљЗДгІЫйТЪ v(N2)ЃН_______________ЁЃ
(2)250 sЪБЃЌH2ЕФзЊЛЏТЪЮЊ_______________ЁЃ
(3)вбжЊNЁдNЕФМќФмЮЊ946 kJЁЄmol-1ЃЌHЃHЕФМќФмЮЊ436 kJЁЄmol-1ЃЌNЃHЕФМќФмЮЊ391 kJЁЄmol-1ЃЌдђЩњГЩ1 mol NH3Й§ГЬжаЕФШШСПБфЛЏЮЊ_______kJЁЃЯТЭМФме§ШЗБэЪОИУЗДгІжаФмСПБфЛЏЕФЪЧ_____ЃЈЬюзжФИЃЉЁЃ
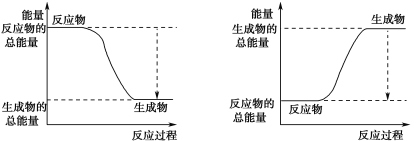
A B
(4)ЮЊМгПьЗДгІЫйТЪЃЌПЩвдВЩШЁЕФДыЪЉ______________ЁЃ
aЃЎНЕЕЭЮТЖШ bЃЎдіДѓбЙЧП cЃЎКуШнЪБГфШыHeЦј
dЃЎКубЙЪБГфШыHeЦј eЃЎМАЪБЗжРыГіNH3
(5)ЯТСаЫЕЗЈДэЮѓЕФЪЧ____________ЁЃ
aЃЎЪЙгУДпЛЏМСЪЧЮЊСЫМгПьЗДгІЫйТЪЃЌЬсИпЩњВњаЇТЪ
bЃЎЩЯЪіЬѕМўЯТЃЌN2ВЛПЩФм100%зЊЛЏЮЊNH3
cЃЎдквЛЖЈЬѕМўЯТЃЌКЯГЩАБЗДгІгавЛЖЈЕФЯоЖШ
dЃЎ250ЁЋ350 sЪБЃЌЩњГЩЮяХЈЖШБЃГжВЛБфЃЌЗДгІЭЃжЙ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЪЕбщЪввдПеЦјКЭУОЮЊдСЯжЦБИ Mg3N2 ЕФзАжУШчЭМЫљЪОЃЈМаГжКЭМгШШзАжУТдШЅЃЉЃК
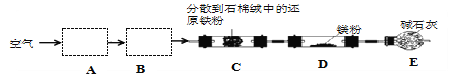
ЯТСаЫЕЗЈе§ШЗЕФЪЧЃЈ ЃЉ
A. зАжУ AЁЂB жаПЩвРДЮМгШыХЈСђЫсЁЂNaOH ШмвК
B. ШєШЅЕєзАжУ CЃЌЖдВњЦЗДПЖШЮогАЯь
C. ЪЕбщЪБгІЯШМгШШ CЃЌЭЈШывЛЖЮЪБМфПеЦјКѓдйМгШШD
D. E жаМюЪЏЛвЕФзїгУЪЧЮќЪеЮВЦј
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПбЧЯѕѕЃТШЃЈNOClЃЌШлЕуЃКЃ64.5 ЁцЃЌЗаЕуЃКЃ5.5 ЁцЃЉЪЧвЛжжЛЦЩЋЦјЬхЃЌгіЫЎвзЗДгІЩњГЩвЛжжЮобѕЫсКЭСНжжЕЊЕФГЃМћбѕЛЏЮяЁЃбЧЯѕѕЃТШгІгУЙуЗКЃЌПЩгУгкКЯГЩЧхНрМСЁЂДЅУНМСМАжаМфЬхЕШЁЃЪЕбщЪвПЩгЩТШЦјгывЛбѕЛЏЕЊдкГЃЮТГЃбЙЯТКЯГЩЁЃ
ЃЈ1ЃЉМззщЭЌбЇФтжЦБИдСЯЦјNOКЭCl2ЃЌжЦБИзАжУШчЭМЫљЪОЃЌЮЊжЦБИДПОЛИЩдяЕФЦјЬхЃЌВЙГфгвБэжаШБЩйЕФвЉЦЗЁЃ
зАжУЂё | зАжУЂђ | ||
еєСѓЩеЦПжа | AвЧЦїжа | ||
жЦБИДПОЛЕФCl2 | MnO2 | Ђй______ | Ђк______ |
жЦБИДПОЛЕФNO | Cu | Ђл______ | Ђм______ |
ЃЈ2ЃЉввзщЭЌбЇЖдМззщЭЌбЇжЦШЁNOЕФзАжУТдМгИФСМЃЌНсКЯМззщжЦЕУЕФCl2ЙВЭЌжЦБИNOClЃЌзАжУШчЭМЫљЪОЃК
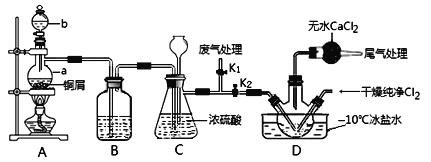
ЂйвЧЦїbЕФУћГЦЮЊ________________ЁЃ
ЂкзщзАКУЪЕбщзАжУКѓгІЯШ______________ЃЌШЛКѓвРДЮзАШывЉЦЗЁЃДЫЪЕбщЙиМќВйзїгаСНЕуЃКвЛЪЧНЋCl2ГфТњDзАжУЕФШ§ОБЦПжаЃЛЖўЪЧAжаЗДгІПЊЪМЪБвЊЯШЙиБеK2ЃЌДђПЊK1ЃЌД§NOГфТњзАжУКѓдйЙиБеK1ЃЌДђПЊK2ЁЃетСНВНВйзїжаГфТњЕФФПЕФЖМЪЧ__________________________________________________ЁЃ
ЂлШєCзАжУжабЙЧПЙ§ДѓЃЌПЩвдЙлВьЕНЕФЯжЯѓЪЧ_________________________ЁЃ
ЂмзАжУDжаБљбЮЫЎЕФзїгУЪЧ__________________ЁЃ
ЃЈ3ЃЉбЧЯѕѕЃТШЃЈNOClЃЉДПЖШЕФВтЖЈЃКНЋЫљЕУбЧЯѕѕЃТШЃЈNOClЃЉВњЦЗ13.10gШмгкЫЎЃЌХфжЦГЩ250mLШмвКЃЛШЁГі25.00mLЃЌвдK2CrO4ШмвКЮЊжИЪОМСЃЌгУ0.8molЁЄL-1AgNO3БъзМШмвКЕЮЖЈжСжеЕуЃЌЯћКФБъзМШмвКЕФЬхЛ§ЮЊ 22.50mLЁЃЃЈвбжЊЃКAg2CrO4ЮЊзЉКьЩЋЙЬЬхЃЉ
ЂйбЧЯѕѕЃТШЃЈNOClЃЉгыЫЎЗДгІЕФЛЏбЇЗНГЬЪНЮЊ_________________________ЁЃ
ЂкбЧЯѕѕЃТШЃЈNOClЃЉЕФжЪСПЗжЪ§ЮЊ______________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСазАжУжаФмаЮГЩдЕчГиЕФЪЧ(ЁЁЁЁ)

A. ЂйЂлЂнB. ЂкЂмЂоC. ЂйЂнЂоD. ЂкЂлЂм
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвбжЊЛЏбЇЗДгІЂй:Fe(s)+CO2(g)![]() FeO(s)+CO(g),ЦфЛЏбЇЦНКтГЃЪ§ЮЊK1;ЛЏбЇЗДгІЂк:Fe(s)+H2O(g)
FeO(s)+CO(g),ЦфЛЏбЇЦНКтГЃЪ§ЮЊK1;ЛЏбЇЗДгІЂк:Fe(s)+H2O(g)![]() FeO(s)+H2(g),ЦфЛЏбЇЦНКтГЃЪ§ЮЊK2,дкЮТЖШ973 KКЭ1173 KЕФЧщПіЯТ,K1ЁЂK2ЕФжЕЗжБ№ШчЯТ:
FeO(s)+H2(g),ЦфЛЏбЇЦНКтГЃЪ§ЮЊK2,дкЮТЖШ973 KКЭ1173 KЕФЧщПіЯТ,K1ЁЂK2ЕФжЕЗжБ№ШчЯТ:
ЮТЖШ | K1 | K2 |
973 K | 1.47 | 2.38 |
1 173 K | 2.15 | 1.67 |
(1)ЭЈЙ§БэИёжаЕФЪ§жЕПЩвдЭЦЖЯ:ЗДгІЂйЪЧ_______(ЬюЁАЮќШШЁБЛђЁАЗХШШЁБ)ЗДгІЁЃ
(2)ЯжгаЗДгІЂл:CO2(g)+H2(g)![]() CO(g)+H2O(g),ЧыФуаДГіИУЗДгІЕФЦНКтГЃЪ§K3ЕФБэДяЪН:K3=______ЁЃ
CO(g)+H2O(g),ЧыФуаДГіИУЗДгІЕФЦНКтГЃЪ§K3ЕФБэДяЪН:K3=______ЁЃ
(3)ИљОнЗДгІЂйгыЂкПЩЭЦЕМГіK1ЁЂK2гыK3жЎМфЕФЙиЯЕЪНЮЊ__________,ОнДЫЙиЯЕЪНМАЩЯБэЪ§Он,ФмЭЦЖЯГіЗДгІЂлЪЧ________(ЬюЁАЮќШШЁБЛђЁАЗХШШЁБ)ЗДгІЁЃ
(4)вЊЪЙЗДгІЂлдквЛЖЈЬѕМўЯТНЈСЂЕФЦНКтЯђе§ЗДгІЗНЯђвЦЖЏ,ПЩВЩШЁЕФДыЪЉга______ ЁЂ_____ (ЬюаДзжФИађКХ)ЁЃ
A.ЫѕаЁЗДгІШнЦїЕФШнЛ§ B.РЉДѓЗДгІШнЦїЕФШнЛ§
C.Щ§ИпЮТЖШ D.ЪЙгУКЯЪЪЕФДпЛЏМС
E.ЩшЗЈМѕаЁЦНКтЬхЯЕжаЕФCOЕФХЈЖШ
(5)ЭММзЁЂввЗжБ№БэЪОЗДгІЂлдкt1ЪБПЬДяЕНЦНКт,дкt2ЪБПЬвђИФБфФГИіЬѕМўЖјЗЂЩњБфЛЏЕФЧщПі:
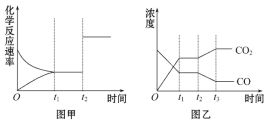
ЂйЭММзжаt2ЪБПЬЗЂЩњИФБфЕФЬѕМўЪЧ__________ЁЃ
ЂкЭМввжаt2ЪБПЬЗЂЩњИФБфЕФЬѕМўЪЧ__________ЁЃ
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com