
科目: 来源: 题型:
【题目】将![]() 和
和![]() 以
以![]() (体积比)分别通入到体积为2L的恒容密闭容器中进行反应:
(体积比)分别通入到体积为2L的恒容密闭容器中进行反应:![]() ,得到如下三组数据,其中实验①、②没有使用催化剂。下列说法不正确的是( )
,得到如下三组数据,其中实验①、②没有使用催化剂。下列说法不正确的是( )
实验 | 温度/℃ | 起始 | 平衡 | 达平衡所需时间/min |
① | 500 | 5.00 | 2.00 | 40 |
② | 800 | 3.00 | 1.00 | 15 |
③ | 500 | 3.00 | 1.20 | 9 |
A. 实验①中,在![]() 内,以
内,以![]() 表示的反应速率大于
表示的反应速率大于![]()
B. 比较实验①和②,不能说明浓度对反应速率的影响
C. 比较实验①和②,不能说明反应速率随温度升高而增大
D. 比较实验②和③,说明实验③使用了催化剂
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法不正确的是( )
A. 干冰升华和液氯气化时,都只需克服分子间作用力
B. 硫酸氢钠晶体溶于水,需要克服离子键和共价键
C. ![]() 和
和![]() 中,每个原子的最外层都具有8电子稳定结构
中,每个原子的最外层都具有8电子稳定结构
D. 石墨转化为金刚石时,既有共价键的断裂,又有共价键的形成
查看答案和解析>>
科目: 来源: 题型:
【题目】如图示中,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物。它们的焰色反应均为黄色。
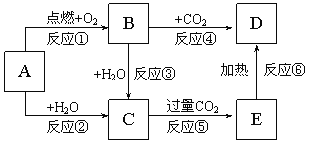
请填写下列空白:
(1)写出化学式:A_______、B______、 C_______。
(2)以上反应中属于氧化还原反应的有_______。(填写编号)
(3)写出A→C反应的离子方程式_______;E→D的化学方程式_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验方案中,能达到相应实验目的的是
选项 | A | B | C | D |
目的 | 证明乙醇发生消去反应 | 证明乙炔可使溴水褪色 | 实验室制备乙酸乙酯 | 实验室制备氨气 |
实验方案 |
|
|
|
|
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】现有FeCl3、AlCl3的混合溶液100mL,逐滴加入NaOH溶液,生成沉淀的物质的量随加入的NaOH的物质的量的关系如图,请计算出FeCl3、AlCl3的物质的量浓度各为_____ ______
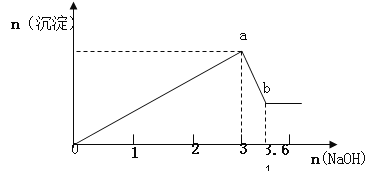
查看答案和解析>>
科目: 来源: 题型:
【题目】A是一种红棕色金属氧化物,B、G是金属单质,F是一种难溶于水的白色化合物,受热后容易发生分解。
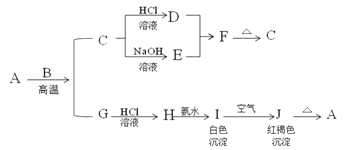
(1)写出下列物质的化学式:A:___ E:___ F:___ H:__。
(2)按要求写方程式:
①H与氨水反应的离子方程式:___。
②B与氢氧化钠溶液反应的离子方程式:___。
③I在空气中转化为J的化学方程式:___。
查看答案和解析>>
科目: 来源: 题型:
【题目】某中学化学课外兴趣小组通过实验探究Fe2+、Fe3+的性质。回答下列问题:
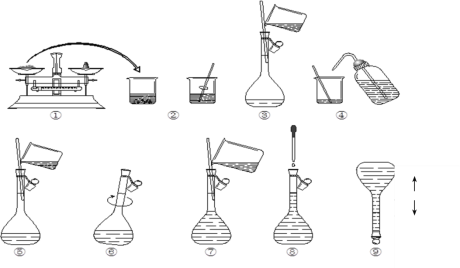
(1)本次实验中共需要1mol/LFeCl2溶液100 mL,配制时涉及到如下操作:
①步骤③中玻璃棒的作用是__;
②在配制溶液过程中步骤⑦所进行的操作是___(填“洗涤”、“转移”、“定容”);该步中视线应与溶液凹液面的最低处保持___。
③下列操作会使所配溶液物质的量浓度偏低的是___。
A.溶解后小烧杯、玻璃棒没有洗涤
B.所用容量瓶中,已有少量蒸馏水
C.定容、加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度线
(2)取2mLFeCl2溶液于试管中,加入几滴氯水,再加入1滴KSCN溶液,观察到的现象为__,说明Cl2可将Fe2+氧化成Fe3+。FeCl2溶液与氯水反应的离子方程式为___,此时将所取FeCl2溶液完全反应需__molCl2。
(3)在(2)溶液中加入过量的铁粉,溶液变成___色;发生反应的离子方程式为__,此时溶液中所含铁元素的微粒的物质的量为__mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列解释事实的化学用语不正确的是
A.铝制餐具不宜长期存放酸性食物:2Al+6H+=2Al3++3H2↑
B.用NaHCO3溶液除去CO2中的HCl气体:HCO3-+H+=CO2↑ +H2O
C.口罩中无纺布纤维聚丙烯的合成:nCH3CH=CH2![]()
![]()
D.硬塑料中酚醛树脂的合成: 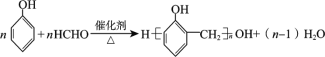
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室制备并收集干燥、纯净氯气的装置如图所示:

(1)写出实验室制备Cl2的化学方程式:___。
(2)写出指定试剂的名称,C__,D__。
(3)C的作用是__,D的作用是__,F的作用是___。
(4)检验氯气是否收集满的操作:___。
(5)实验室除了可用二氧化锰和浓盐酸反应制取氯气外,还可以用其他很多方法制取氯气,其中用高锰酸钾和浓盐酸反应制备氯气的化学方程式可表示为:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,其中该反应中HCl的作用是___,若反应产生0.5mol Cl2,则消耗的氧化剂的物质的量为___mol,反应转移的电子数是___。
查看答案和解析>>
科目: 来源: 题型:
【题目】将铁粉和铝粉的混合物逐渐加入100mL的稀硝酸中,其产生的有关离子浓度与加入铁粉和铝粉的混合物的质量的关系如下图所示:
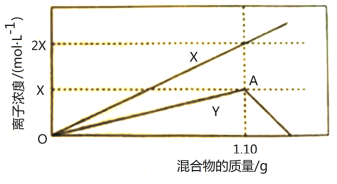
若反应过程中生成的气体为NO,溶液的体积变化忽略不计。请回答下列问题:
(1)X表示的变化离子是_______________(填离子符号)。
(2)OA段发生反应的离子方程式是___________________________________。
(3)稀硝酸溶解1.10g铁粉和铝粉后溶液还能继续溶解混合物的原因是________________
(4)该硝酸的浓度是_____________mol·L-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com