
科目: 来源: 题型:
【题目】![]() 作为加碘剂的食盐在保存过程中,由于空气中氧气的作用,容易引起碘的损失。
作为加碘剂的食盐在保存过程中,由于空气中氧气的作用,容易引起碘的损失。![]() 溶于
溶于![]() 溶液能发生
溶液能发生![]() 的反应,在低温条件下,可制得
的反应,在低温条件下,可制得![]() 。下列说法不正确的是( )
。下列说法不正确的是( )
A.其他条件相同的情况下,![]() 在
在![]() 溶液中的溶解度大于在水中的溶解度
溶液中的溶解度大于在水中的溶解度
B.向![]() 溶液中加入淀粉溶液,溶液变蓝色
溶液中加入淀粉溶液,溶液变蓝色
C.![]() 代替
代替![]() 作为加碘剂,可以减少碘的损失
作为加碘剂,可以减少碘的损失
D.由于还原性![]() ,加入
,加入![]() 可以提高加碘盐(添加
可以提高加碘盐(添加![]() )的稳定性
)的稳定性
查看答案和解析>>
科目: 来源: 题型:
【题目】已知![]() ,25℃时,
,25℃时,![]() 的
的![]() 。该温度下用
。该温度下用![]() 溶液滴定
溶液滴定![]() 溶液的滴定曲线如图所示。下列说法不正确的是( )
溶液的滴定曲线如图所示。下列说法不正确的是( )
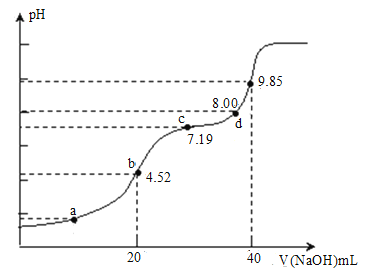
A.若a点溶液c(![]() )=c(H2SO3),则a点对应的
)=c(H2SO3),则a点对应的![]()
B.若选择b为反应终点,宜选择甲基橙为指示剂
C.c点对应的溶液2c(Na+)=3c(![]() )
)
D.d点对应的溶液c(Na+)>c(![]() )>c(
)>c(![]() )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
查看答案和解析>>
科目: 来源: 题型:
【题目】化学就在我们身边,它与我们的日常生活密切相关,按要求回答以下问题:
(1)缺铁性贫血患者应补充Fe2+,通常以硫酸亚铁的形式补充,而硫酸铁无这种药效。当用硫酸亚铁制成药片时外表包有一层特殊的糖衣,这层糖衣的作用是_________________.
(2)硅酸盐常可写成氧化物形式,钾长石(K2Al2Si6O16)写成氧化物的形式为____________.
(3)漂粉精中有效成分的化学式为_________________.
(4)“硅材料”是无机非金属材料的主角,其中广泛应用的光导纤维成分是_____________________
(5)陶瓷、水泥和玻璃是常用的传统的无机非金属材料,其中生产普通玻璃的主要原料有_________,氢氧化钠溶液不能用玻璃塞的原因是(化学方程式)_________________.
(6)向浑浊的水中加入明矾KAl(SO4)212H2O后,水可得到净化.写出明矾在水中的电离方程式_______,往明矾溶液中逐滴加入Ba(OH)2溶液直至Al3+恰好沉淀完全,发生反应的离子方程式为_________________ .
(7)饮用水中的NO3-对人类健康产生危害,为了降低饮用水中NO3-的浓度,可以在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为:10Al+6NaNO3+4NaOH═10NaAlO2+3N2↑+2H2O.
请回答下列问题:
①在化学方程式上用单线桥标出该反应中电子转移的方向和数目:_________________.
②上述反应中若生成标况下3.36L N2,则转移的电子数目为:_________________.
查看答案和解析>>
科目: 来源: 题型:
【题目】准确称取6.0 g铝土矿样品(主要成分为Al2O3,含Fe2O3杂质),加入100 mL稀硫酸中,充分反应后向滤液中加入10 mol·L-1NaOH溶液,产生沉淀的质量和加入NaOH溶液体积之间的关系如图所示。则所用硫酸物质的量浓度为( )

A. 3.50 mol·L-1
B. 1.75 mol·L-1
C. 0.85 mol·L-1
D. 无法确定
查看答案和解析>>
科目: 来源: 题型:
【题目】在下列溶液中,各组离子一定能够大量共存的是 ( )
A.使酚酞试液变红的溶液:Na+、Cl-、SO42-、Fe3+
B.使紫色石蕊试液变红的溶液:Fe3+、Mg2+、NO![]() 、Cl-
、Cl-
C.某无色的溶液:K+、Ba2+、Cl-、MnO4-
D.碳酸氢钠溶液:K+、SO42-、Cl-、OH-
查看答案和解析>>
科目: 来源: 题型:
【题目】将20g两种金属的混合物投入足量的稀硫酸中,反应完全后得到标准状况下H2 11.2L,则该混合物的组成可能是( )
A. Na和Fe B. Mg和Cu C. Al和Mg D. Zn和Fe
查看答案和解析>>
科目: 来源: 题型:
【题目】研究化学反应中能量变化,能更好地利用化学反应为生产和生活服务。
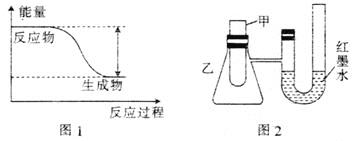
(1)反应Fe+H2SO4=FeSO4+H2↑的能量变化如图1所示。
①该反应为 __________(填“吸热”或“放热”)反应。
②为了探究化学能与热能的转化,某实验小组设计了图2实验装置,在甲试管里先加入适量铁片,再加入稀硫酸,U形管中可观察到的现象是__________。
③若要使该反应的反应速率加快,下列措施可行的是__________(填字母)。
A.铁片改为铁粉 B.稀硫酸改为98%的浓硫酸 C.升高温度
(2)若将上述反应设计成原电池,装置如图3所示。
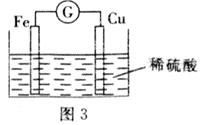
①铜为 __________(填“正”或“负”)极;负极的电极反应式为______。
②若该电池反应过程中共转移0.3 mol电子,则生成的H2在标准状况下的体积是__________L。
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数,下列有关说法正确的是( )
A. 100mL12mol/L浓盐酸与足量的MnO2加热充分反应生成Cl2分子数为0. 3 NA
B. 80gSO3在标准状况下所占体积约为22.4L
C. 向FeI2溶液中通入适量Cl2,当有1 mol Fe2+被氧化时,转移的电子的数目为NA
D. 5.4g铝粉与足量的氢氧化钠溶液充分反应生成H2分子数为0. 3 NA
查看答案和解析>>
科目: 来源: 题型:
【题目】利用废旧镀锌铁皮可制备磁性Fe3O4胶体粒子及副产物ZnO,制备流程如下图所示
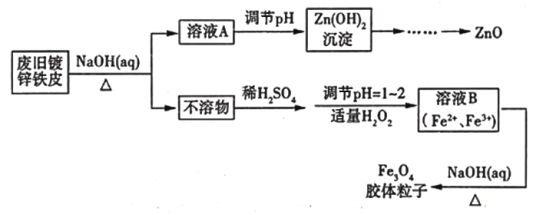
(1)从流程图可知,Zn、Fe中能与NaOH溶液反应的是_______________________。
(2)向不溶物中加入稀硫酸发生反应的离子方程式是____________________________________。
(3)加入适量H2O2的目的是__________________________________。
(4)如何证明已生成了Fe3O4胶体?_____________________________________________________。
(5)流程中所需的硫酸溶液由焦硫酸(H2SO4·SO3)溶于水配制而成,其中的SO3都转化为硫酸,若将445g焦硫酸溶于水配成4.00L硫酸,该硫酸的物质的量浓度为__________________mol/L。
(6)稀硫酸也可以用浓硫酸和水配制。已知4 mol/L的硫酸溶液密度为ρ1g/cm3,2 mol/L的硫酸溶液密度为ρ2g/cm3。100g物质的量浓度为4 mol/L的硫酸溶液与___________mL水混合,使硫酸的物质的量浓度减小到2 mol/L(用含ρ1、ρ2的式子表示)
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示___________,K值大小与温度的关系是:温度升高,K值_________(填一定增大、一定减小、或可能增大也可能减小)。
(2)对于可逆反应CO(g) +H2O(g) ![]() CO2(g)+H2(g) △H<0在850℃时,KC=1 该反应的平衡常数K的表达式为K=______;若温度为900℃,达到平衡后KC_____1 (填“>“<”=)
CO2(g)+H2(g) △H<0在850℃时,KC=1 该反应的平衡常数K的表达式为K=______;若温度为900℃,达到平衡后KC_____1 (填“>“<”=)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com