
科目: 来源: 题型:
【题目】某溶液中可能含有K+、Ba2+、NH4+、SO42-、CO32-、Cl-中的几种离子:
①取V mL的溶液滴加足量的 BaCl2 溶液,过滤,得到4.30g白色沉淀,往白色沉淀中加入足量的盐酸,沉淀部分溶解,余下2.33g沉淀未溶解;往滤液中滴加足量的AgNO3溶液,生成白色沉淀0.45mol。
②另取原溶液 V mL 与足量的 NaOH固体共热,生成气体 1.12 L(标准状况下)。
根据以上实验,回答下列问题:
(1)溶液中一定存在的阴离子有_____________
(2)溶液中不能确定存在的离子有 _____
(3)实验②发生反应的离子方程式为_____
查看答案和解析>>
科目: 来源: 题型:
【题目】氢气与氧气生成水的反应是氢能源应用的重要途径。下列有关说法正确的是
A. 一定温度下,反应2H2(g)+O2(g) ![]() 2H2O(g)能自发进行,该反应的ΔH<0
2H2O(g)能自发进行,该反应的ΔH<0
B. 氢氧燃料电池的负极反应为O2+2H2O+4e![]() 4OH
4OH
C. 常温常压下,氢氧燃料电池放电过程中消耗11.2 L H2,转移电子的数目为6.02×1023
D. 反应2H2(g)+O2(g) ![]() 2H2O(g)的ΔH可通过下式估算:
2H2O(g)的ΔH可通过下式估算:
查看答案和解析>>
科目: 来源: 题型:
【题目】现有金属单质 A、B 和气体甲、乙、丙以及物质 C、D、E、F,它们之间能发生如下反应。(图中有些反应的产物和反应条件没有标出)
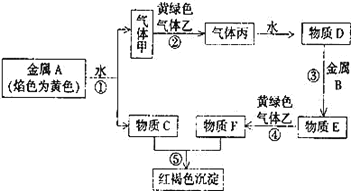
请回答下列问题:
(1) A 的化学式为_____,F 的化学式为_____;
(2) 写出 C 溶液与 Al 反应的离子方程式_____。
(3) 写出 C 溶液与黄绿色气体乙反应的化学方程式_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】镍钴锰三元材料是近年来开发的一类新型锂离子电池正极材料,具有容量高、循环稳定性好、成本适中等重要优点。镍钴锰三元材料中Ni为主要活泼元素,通常可以表示为:LiNiaCobMncO2,其中a+b+c=1,可简写为LiAO2。充电时总反应为LiAO2 + nC = Li1-xAO2 + LixCn(0<x<1),工作原理如下图所示,则以下说法正确的是( )

A. 放电时Ni元素最先失去电子
B. 放电时电子从a电极由导线移向b电极
C. 充电时的阳极反应式为LiAO2 - xe-= Li1-xAO2 + xLi+
D. 充电时转移1mol电子,理论上阴极材料质量增加7g
查看答案和解析>>
科目: 来源: 题型:
【题目】一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)![]() 2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示:
2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示:

已知:气体分压(P分)=气体总压(P总)×体积分数。下列说法正确的是
A. 550℃时,若充入惰性气体,正,逆 均减小,平衡不移动
B. 650℃时,反应达平衡后CO2的转化率为25.0%
C. T℃时,若充入等体积的CO2和CO,平衡向逆反应方向移动
D. 925℃时,用平衡分压代替平衡浓度表示的化学平衡常数KP=24.0P总
查看答案和解析>>
科目: 来源: 题型:
【题目】在呼吸面具和潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验仪器,用图中的实验装置进行实验,证明过氧化钠可作供氧剂。

(1)A 是制取 CO2 的装置,可选用的试剂_____(填序号)
①碳酸钙固体与稀硫酸 ②碳酸钠固体与稀盐酸 ③碳酸氢钠固体与氢氧化钠溶液
写出对应的离子方程式_________________。
(2)填写表中空格:
仪器 | 加入试剂 | 加入该试剂的目的 |
B | 饱和 NaHCO3 溶液 | ____________ |
C | ____________ | 与 CO2 和水反应产生 O2 |
D | NaOH 溶液 | ____________ |
(3)写出过氧化钠与二氧化碳反应的化学方程式_____。
(4)用_____检验 F 中收集到的气体,现象是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】在容积为2.00 L的容器中,通入一定量的N2O4,发生反应N2O4(g)2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:

(1)反应的ΔH________0(填“大于”或“小于”);100 ℃时,体系中各物质浓度随时间变化如上图所示。在0~60 s时段,反应的平衡常数K1为________。
(2)100 ℃时达平衡后,将反应容器的容积增大一倍,平衡向________(填“正反应”或“逆反应”)方向移动,达到新的平衡后N2O4的浓度范围是___________________
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示是分离混合物时常用的仪器,回答下列问题:
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]() E.
E. 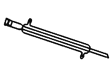
(1)写出仪器 C、E 的名称_____ 、_____。
(2)分离以下混合物应该主要选用上述什么仪器(填字母符号)a.粗盐和泥沙:____b.花生油和水:____
(3)下列实验与物质微粒大小无直接关系的是_____
A.过滤 B.渗析
B.渗析 C.萃取
C.萃取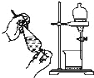 D.丁达尔效应
D.丁达尔效应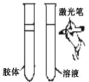
查看答案和解析>>
科目: 来源: 题型:
【题目】将镁铝合金溶于100mL稀硝酸中,产生1.12LNO气体(标准状况),向反应后的溶液中加入NaOH溶液,产生沉淀与加入氢氧化钠体积(mL)情况如图所示。下列说法不正确的是( )

A.原溶液中c(HNO3)=1.8mol/LB.沉淀最大质量为4.08g
C.n(Mg):n(Al)=1:1D.氢氧化钠溶液浓度为3mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:废液中含+6 价铬的化合物毒性较大污染性强,常用 NaHSO3 将废液中的Cr2O72-还原成 Cr3+。请配平该反应的离子方程式:_____ Cr2O72-+_____HSO3-+____H+ = ____Cr3++_____SO42-+_____H2O
并用双线桥标出电子转移的方向和数目____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com