
科目: 来源: 题型:
【题目】把温度为![]() ,浓度为
,浓度为![]() 和
和![]() 的碱溶液各50mL混合
的碱溶液各50mL混合![]() 设溶液的密度均为
设溶液的密度均为![]() ,比热容为
,比热容为![]() ,轻轻搅动。测得酸碱混合液的温度变化数据如下:
,轻轻搅动。测得酸碱混合液的温度变化数据如下:
反应物 | 起始温度 | 终止温度 |
| 20 |
|
| 20 |
|
则反应![]() 的焓变约为(单位:
的焓变约为(单位:![]() )
)
A.![]() B.
B.![]()
C.![]() D.缺少数据,无法计算
D.缺少数据,无法计算
查看答案和解析>>
科目: 来源: 题型:
【题目】炽热的炉膛内有反应:![]() 往炉膛内通入水蒸气时,有如下反应:
往炉膛内通入水蒸气时,有如下反应:![]() ,
,![]() ,
,![]() ,其能量变化示意图如下,
,其能量变化示意图如下,

已知CO的燃烧热为![]() 。下列有关说法正确的是
。下列有关说法正确的是![]()
A.![]()
B.![]() 的燃烧热为
的燃烧热为![]()
C.在反应![]() 中,反应物总键能大于生成物总键能
中,反应物总键能大于生成物总键能
D.往炽热的炉膛内通入水蒸气可节省燃料
查看答案和解析>>
科目: 来源: 题型:
【题目】FeBr2是一种黄绿色固体,某学习小组制备并探究它的还原性。
I.制备FeBr2固体
实验室用如图所示装置制取溴化亚铁。其中A为CO2发生装置,D和d中均盛有液溴,E为外套电炉丝的不锈钢管,e是两个耐高温的瓷皿,其中盛有细铁粉。
实验开始时,先将干燥、纯净的CO2气流通入D中,再将铁粉加热至600-700℃,E管中铁粉开始反应。不断将d中液溴滴入温度为100-120℃的D中,经过一段时间的连续反应,在不锈钢管内产生黄绿色鳞片状溴化亚铁。
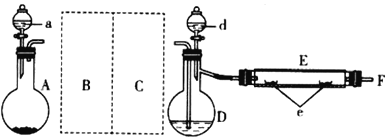
(1)若在A中盛固体CaCO3,a中盛有6mol/L的盐酸。为使导入D中的CO2为干燥纯净的气体,图中C处的洗气瓶中装有浓硫酸,则B中为___,若进入E装置中的CO2未干燥,则可能发生的副反应的化学方程式为___。
(2)E管中的反应开始前通入CO2的主要作用是___;E管中的反应开始后持续通入CO2的主要作用是___。
II.探究FeBr2的还原性
(3)现实验需要90mL0.2mol/LFeBr2溶液,取上述反应制得的FeBr2固体配制该溶液,所需仪器除烧杯、量筒、玻璃棒、胶头滴管外,还需要的玻璃仪器是___。
(4)已知:Cl2的CCl4溶液呈黄绿色,Br2的CCl4溶液呈橙红色。Cl2既能氧化Br-,也能氧化Fe2+。取10mL上述FeBr2溶液,向其中滴加几滴新制的氯水,振荡后溶液呈黄色。取少量反应后的溶液加入KSCN溶液,溶液变为血红色。另取少量反应后的溶液加入CCl4,振荡后,下层为无色液体。以上实验结论表明还原性:Fe2+___Br-(填“>”或“<”)。
(5)若向30mL步骤(3)的FeBr2溶液中通入标准状况下179.2mL的Cl2,取少量反应后的溶液加入CCl4,振荡后下层液体呈___色,写出该反应的离子方程式___。
查看答案和解析>>
科目: 来源: 题型:
【题目】钢铁是目前应用最广泛的金属材料,了解钢铁腐蚀的原因与防护方法具有重要意义,对钢铁制品进行抗腐蚀处理,可适当延长其使用寿命。
(1)抗腐蚀处理前,生产中常用盐酸来除铁锈。现将一表面生锈的铁件放入盐酸中,当铁锈除尽后,溶液中发生的化合反应的化学方程式为__________________。
(2)利用如图装置,可以模拟铁的电化学防护。
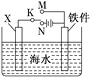
①若X为碳棒,为减缓铁件的腐蚀,开关K应置于________________处。
②若X为锌,开关K置于M处,该电化学防护法称为__________。
(3)图中若X为粗铜,容器中海水替换为硫酸铜溶液,开关K置于N处,一段时间后,当铁件质量增加3.2 g时,X电极溶解的铜的质量____3.2 g(填“<”“>”或“=”)。
(4)图中若X为铜,容器中海水替换为FeCl3溶液,开关K置于M处,铜电极发生的反应是______________________,若将开关K置于N处,发生的总反应是_______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下列图示所得出的结论正确的是
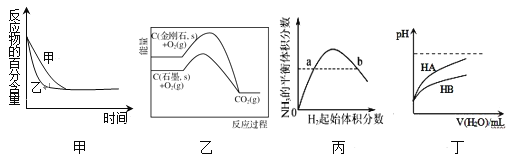
A.图甲表示压强对可逆反应2A(g)+2B(g)![]() 3C(g)+D(s)的影响,乙的压强比甲的压强大
3C(g)+D(s)的影响,乙的压强比甲的压强大
B.图乙是金刚石与石墨分别氧化生成CO2的能量关系曲线,说明石墨转化为金刚石的反应的ΔH>0
C.图丙表示一定条件下的合成氨反应中,NH3的平衡体积分数随H2起始体积分数(N2的起始量恒定)的变化,图中a点N2的转化率大于b点
D.图丁表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则相同条件下NaA溶液的pH大于同浓度的NaB溶液的pH
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上可以利用废气中的CO2为原料制取甲醇,其反应方程式为:CO2+3H2![]() CH3OH+H2O。请回答下列问题:
CH3OH+H2O。请回答下列问题:
(1)已知常温常压下下列反应的能量变化如图1所示:
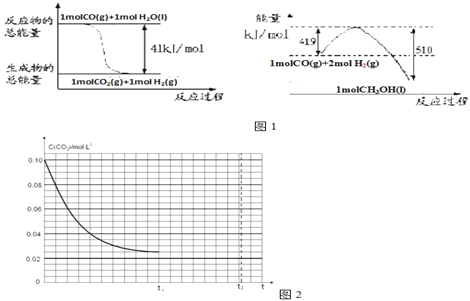
写出由二氧化碳和氢气制备甲醇的热化学方程式______________________________,该反应的△S_______0(填“>”或“<”或“=”),在________情况下有利于该反应自发进行(填“低温”或“高温”)。
(2)如果上述反应方程式的平衡常数K值变大,则该反应_________(选填编号)。
A.一定向正反应方向移动 B.在平衡移动时正反应速率先增大后减小
C.一定向逆反应方向移动 D.在平衡移动时逆反应速率先减小后增大
(3)若反应容器的容积为2.0L,CO2和H2的起始浓度分别为0.10 mol·L-1和0.30 mol·L-1。
①若反应时间为4.0min,容器内气体的密度减少了2.0g/L,则在这段时间内CO2的平均反应速率为__________。
②若反应在t1时达到平衡,过程中c(CO2)随时间t变化趋势曲线如图2所示.保持其他条件不变,t1时将容器体积压缩到1L,请画出t1后c(CO2)随时间t变化趋势曲线(t2达到新的平衡)______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】液氨作为一种潜在的清洁汽车燃料,它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势。请回答下列问题:
Ⅰ.已知反应N2(g)+3H2(g)![]() 2NH3(g)的活化能Ea1=akJ/mol,相关化学键键能数据如下:
2NH3(g)的活化能Ea1=akJ/mol,相关化学键键能数据如下:
化学键 | H-H | N≡N | N-H |
键能/kJ·mol-1 | 436 | 946 | 391 |
(1)反应2NH3(g)![]() N2(g)+3H2(g)的活化能Ea2=______kJ/mol(用含a的代数式表示);
N2(g)+3H2(g)的活化能Ea2=______kJ/mol(用含a的代数式表示);
(2)已知:
① 4NH3(g)+3O2(g)=2N2(g)+6H2O(l) △H1
② 4NH3(g)+5O2(g)=4NO(g)+6H2O(l) △H2
③ 4NH3(g)+6NO(g)=5N2(g)+6H2O(l) △H3
则△H1、△H2、△H3三者之间的关系为:△H3= ______________ ;
Ⅱ.利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,工作原理如图所示。
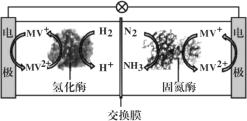
(3)负极的电极反应式为_______________;
(4)当电路中通过3mol电子时,可产生氨气的体积(标况下)为_______L;正极区中n(H+)______(填“增加”、“减少”或“不变”);
(5)该装置在高温下不能正常工作,原因是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】在有机合成中,常需要将官能团消除或增加 ,按要求完成下列各题。
乙烯→乙二醇:CH2=CH2 ![]() CH2Br—CH2Br
CH2Br—CH2Br ![]() HOCH2CH2OH
HOCH2CH2OH
溴乙烷→乙醇:CH3CH2Br ![]() CH2=CH2
CH2=CH2![]() CH3CH2OH
CH3CH2OH
(1)①的化学方程式_______________________________________ 反应类型________________
(2)②的化学方程式__________________________________________反应类型_______________
(3)③的化学方程式_______________________________________反应类型_______________
(4)④的化学方程式_______________________________________反应类型__________________
查看答案和解析>>
科目: 来源: 题型:
【题目】请回答下列问题:
(1)根据题意选择以下四种物质的字母序号填空
A:Si B:Na2SiO3 C:Ca(ClO)2 D:KAl(SO4)2·12H2O
①漂白粉的有效成分是___。
②可用于制备硅胶和木材防火剂的是___。
③可用于制计算机芯片的是___。
④可用于作净水剂的是___。
(2)8.4gNaHCO3正好与20mL盐酸完全反应。此盐酸的物质的量浓度是___,产生的CO2在标准状况下的体积是___L。
(3)高铁酸钠(Na2FeO4)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O
①请用“单线桥”标明该反应电子转移的方向与数目___。
②该反应中氧化剂是___;当有1molNa2FeO4生成,转移的电子有___mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】“烟气脱硫”是环境治理的重要工程,两种常见脱硫方法如下。回答相关问题:
方法I:用亚硫酸盐吸收烟气中的SO2。已知吸收过程中含硫组分物质的量分数与溶液pH的变化关系如图所示。
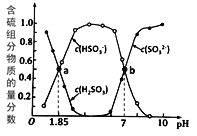
(1)若选用 (NH4)2SO3作为吸收液(已知NH3·H2O 的电离常数Kb=1.74×10-5):
①H2SO3的pKa1=________( pKa1 = -lgKa1);
②(NH4)2SO3溶液呈________(填“酸性”、“碱性”或“中性”),理由是________________;
③图中b点溶液中n(HSO3- ) : n(NH4+) =_________。
(2)若选用0.1mol/L 的Na2SO3作为吸收液,吸收过程中,下列有关粒子浓度关系一定正确的是(忽略溶液体积的变化)_________。
A.Na2SO3溶液中存在:c(Na+)>c(SO32-)>c(H2SO3)>c(HSO3-)
B.NaHSO3溶液中存在:c(Na+)>c(HSO3-)>c(SO32-)>c(H2SO3)
C.当吸收液呈中性时:2c(SO32-)+c(HSO3-)=0.2mol/L
D.当吸收液呈酸性时:c(Na+)=c(SO32-)+c(HSO3-)+c(H2SO3)
方法II:用含铬废水吸收烟气中的SO2。吸收原理如图所示:
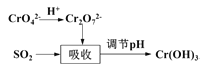
(3)“吸收”中反应的离子方程式为____________________
(4)欲使废水中的铬元素完全转化为Cr(OH)3沉淀,应调节pH的范围为____。(常温下Ksp[Cr(OH)3]=1.0×10-32)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com