
科目: 来源: 题型:
【题目】以钛白酸废液(主要含有TiO2+、Fe2+、Ca2+、SO![]() 等)为原料,获取磷酸钛(2TiO2·P2O5·H2O)和氧化铁黄(FeOOH)的部分流程如图:
等)为原料,获取磷酸钛(2TiO2·P2O5·H2O)和氧化铁黄(FeOOH)的部分流程如图:
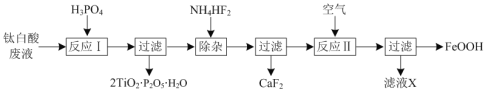
(1)反应Ⅰ中生成2TiO2·P2O5·H2O的离子方程式为___。
(2)反应Ⅱ时溶液的pH约为4,写出反应Ⅱ中Fe2+发生反应的离子方程式:___。
(3)碱性条件下,FeOOH可以被次氯酸钠氧化成Na2FeO4。该反应的离子方程式为___。
(4)TiO2是两性氧化物,TiO2与KHSO4熔融时反应生成TiOSO4的化学方程式为___。
查看答案和解析>>
科目: 来源: 题型:
【题目】按照要求回答下列有关烃类物质的问题现有A、B 两种烃,已知A的分子式为 C5Hm,而B的最简式为C5Hn(m、n 均为正整数).请回答下列问题:
(1)下列关于烃A和烃B的说法不正确的是_______(填序号).
a. 烃A和烃B可能互为同系物 b.烃A 和烃B可能互为同分异构体
c.当m=12时,烃A一定为烷烃 d.当n=11时,烃B可能的分子式有 2 种
(2)若烃A为链烃,且分子中所有碳原子一定共面,在一定条件下,1mol A 最多可与 1mol H2 加成,则A的名称是_____,该烃是否存在顺反异构_____(“是”或“否”)
(3)若烃B为苯的同系物,取一定量的烃B完全燃烧后,生成物先通过足量的浓硫酸,浓硫酸的质量增加 1.26g, 再通过足量的碱石灰,碱石灰的质量增加 4.4g,则烃B的分子式为_____;若其苯环上的一溴代物只有一种, 则符合此条件的烃B有_________种,其中核磁共振氢谱中有4组峰,且峰面积之比为6:3:3:2 的有机物的结构简式为______。
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期两种元素X、Y能形成XmYn型化合物.回答下列问题
(1)当n=2时,若同周期元素X、Y的最外层电子数之和为13.常温下,XY遇水易水解,并能产生能使品红溶液褪色的气体和淡黄色的单质X沉淀。则:
①元素X在周期表中的位置是________。②XmYn中含有的化学键的类型是________。
a 共价键 b 离子键 c 金属键 d 氢键
③写出XmYn与水反应的化学方程式________。
(2)若XmYn是烃类化合物.则
①当n=2时,XmYn的结构式为________。1mol XmYn能与2mol H2反应生成乙,乙能与氯气在光照下发生化学反应,最多可生成________种有机产物(不考虑立体异构).
②当n=6时,写出芳香烃XmYn与浓硝酸、浓硫酸在50℃-60℃时的化学方程式________。
③当n=8时,芳香烃XmYn的球棍模型可表示为 ,写出由XmYn聚合生成的高分子化合物的结构简式________。
,写出由XmYn聚合生成的高分子化合物的结构简式________。
查看答案和解析>>
科目: 来源: 题型:
【题目】请解答下列与蛋白质有关的题目:
(1)鸡蛋腐烂时,常闻到有臭鸡蛋气味的气体,该气体中主要含有___________________(填化学式),说明蛋白质中含有___________________(填元素名称)元素。
(2)误食重金属盐会中毒,这是因为___________________。
(3)浓硝酸溅在皮肤上,使皮肤呈现___________________色,这是由于浓硝酸和蛋白质发生了___________________反应。
查看答案和解析>>
科目: 来源: 题型:
【题目】端炔烃在催化剂存在下可发生偶联反应,成为 Glaser 反应。2R—C≡C—H![]() R—C≡C—C≡C—R+H2 该反应在研究新型发光材料、超分子化学等方面具有重要价值。下面是利用 Glaser 反应制备化合物 E 的一种合成路 线:
R—C≡C—C≡C—R+H2 该反应在研究新型发光材料、超分子化学等方面具有重要价值。下面是利用 Glaser 反应制备化合物 E 的一种合成路 线:
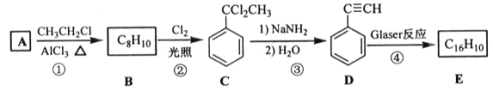
回答下列问题:
(1)B 的一氯取代物的种数为_______。
(2)①和③的反应类型分别为_______、_______。
(3)1 mol E 在催化剂的条件下与足量 H2 反应的化学方程式为_______。
(4)芳香化合物 F 是 C 的同分异构体,其分子中只有两种不同化学环境的氢,数目比为 3:1,写出其中 2 种的结构 简式_____。
(5)用课本所学知识写出用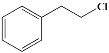 为原料(其他无机试剂任选)制备化合物 D 的合成路线_____。
为原料(其他无机试剂任选)制备化合物 D 的合成路线_____。
(合成路线常用的表示方式为:![]() )
)
查看答案和解析>>
科目: 来源: 题型:
【题目】由短周期元素组成的常见的纯净物,它们之间转化关系如图所示(可以在水溶液中反应)
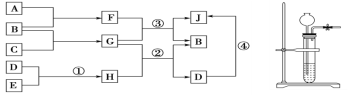
a.A、B、H在常温下均呈气态,F为液态,E为盐酸,D为溶于水的白色固体,A、B、C为单质,A在B中燃烧产生淡蓝色火焰。
b.实验室制取A、H的发生装置如图所示。
c.隔绝空气条件下,将G投入绿矾溶液中,有红褐色沉淀生成,还产生大量气泡。回答下列问题:
(1)化合物G中阳离子与阴离子个数之比为____________;J中所含化学键类型是____________________________________________。
(2)写出下列反应的化学方程式:
②_____________________________________________________;
③_____________________________________________________。
(3)反应①的离子方程式是____________________________________________
(4)化合物G有重要用途,用途为______________________________;
查看答案和解析>>
科目: 来源: 题型:
【题目】Al及其化合物在工业上有极其广泛的用途,
(1)焊接钢轨时用Al冶炼Fe的反应方程式为______;铝的化合物明矾可用于净水,其原理用离子方程式解释为___________。
(2)硅藻遗骸中主要成分是Al2O3、SiO2和Fe2O3。从中获取Al(OH)3的过程如下:
步骤I:取适量硅藻遗骸用70%H2SO4浸泡;
步骤II:向上述浸泡液中加入过量NaOH并过滤;
步骤III:向上述滤液中通入过量CO2过滤得到Al(OH)3。
①用70%H2SO4浸取硅藻遗骸的目的是________。
②步骤II中涉及铝元素的离子方程式为______;
③步骤III中能否用HCl代替CO2?_____(填“能”或“不能”);该步骤所得滤液中存在的电荷守恒式为_______;向该滤液中滴加少量NaOH溶液,则![]() ____填(“变大”、“变小”或“不变”)
____填(“变大”、“变小”或“不变”)
(3)Al(OH)3可用作阻热材料,试从Al(OH)3的化学性质角度分析其原因________。
查看答案和解析>>
科目: 来源: 题型:
【题目】外观与氯化钠相似的亚硝酸钠(Na2NO2)在生活中应用十分广泛,如可用作建筑钢材缓蚀剂、肉制品发色剂等。已知:2NO+Na2O2=2NaNO2 2NO2+Na2O2=2NaNO3
I.某学习小组设计如图装置制备亚硝酸钠(夹持装置已省略)
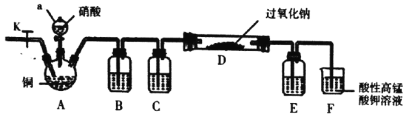
(1)仪器a的名称为________。
(2)装置B、C、E中的试制可选择___。
A 水、浓硫酸、浓硫酸
B 氢氧化钠溶液、浓硫酸、浓硫酸
C 酸性高锰酸钾溶液、浓硫酸、氢氧化钠溶液
D 水、浓硫酸、氢氧化钠溶液
(3)反应开始时先打开止水夹K,通入氮气至F中产生大量气泡,该操作的目的是________。
(4)装置D中的实验现象是________。
(5)装置F中发生反应的离子方程式为________。
Ⅱ.工业上可以用烧碱溶液吸收硝酸厂的尾气制得亚硝酸钠。某学习小组设计如下实验方案测定该产品中亚硝酸钠的质量分数。取1.500g产品配成250mL溶液,取25.00mL溶液于锥形瓶中加入过量的稀硫酸和碘化钾溶液充分反应后,加入适当的指示剂,用0.1000mol/L Na2S2O3标准溶液进行滴定,记录数据如下表。
实验序号 | 1 | 2 | 3 |
Na2S2O3标准溶液体积/mL | 20.02 | 19.98 | 20.00 |
已知: 2NaNO2+2KI+2H2SO4 =2NO↑+I2+2H2O+Na2SO4+K2SO4 2Na2S2O3+I2=Na2S4O6+2NaI
(6)合适的指示剂是________
(7)该产品的纯度为________。
(8)经过讨论,同学认为该产品中可能含有硝酸钠,它会使测定结果________(填“偏高”、“偏低”、“无影响”) 。
查看答案和解析>>
科目: 来源: 题型:
【题目】为了研究反应![]() 的能量变化情况,某同学设计了如图所示实验装置。当向盛有固体A(A不与水反应)的试管中滴加溶液B时,发现U形管中甲处液面下降,乙处液面上升。试回答下列问题。
的能量变化情况,某同学设计了如图所示实验装置。当向盛有固体A(A不与水反应)的试管中滴加溶液B时,发现U形管中甲处液面下降,乙处液面上升。试回答下列问题。

(1)所发生的反应________(填“放出”或“吸收”)热量。
(2)参加反应的A和B的总能量________(填“高于”或“低于”)生成的C和D的总能量。
(3)该反应中物质的化学能通过化学反应转化成________释放出来。
(4)该反应中,断裂反应物中化学键吸收的能量________(填“高于”或“低于”)形成生成物中化学键放出的能量。
(5)写出一个符合题中条件的化学方程式:____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】为消除目前燃料燃烧时产生的环境污染,同时缓解能源危机,有关专家提出了利用太阳能制取氢能的构想。下列说法正确的是
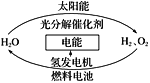
A. H2O的分解反应是放热反应
B. 光分解过程只涉及太阳能与电能的转化
C. 2H2O(l) = 2H2(g) + O2(g) △H > 0
D. 氢气不易贮存和运输,无开发利用价值
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com