
科目: 来源: 题型:
【题目】(1)在一定温度和压强下,1体积X2(g)和3体积Y2(g)化合生成2体积Z(g),则Z气体的化学式是___。
(2)A、B两种气体组成的混合气体8.6g,在标准状况下体积为8.96L。已知A与B的物质的量之比为3:1,相对分子质量之比为14:1,由此可推断A可能是__或__,B是__。
(3)在标准状况下,CO和CO2的混合气体质量为36g,体积为22.4L,则CO所占的体积是___L,质量是___g。
查看答案和解析>>
科目: 来源: 题型:
【题目】铁是人体内不可或缺的微量元素,其配合物的研究也是当今科研的重点之一。
![]() 基态Fe原子的价层电子轨道表达式为________________________________;同周期元素中,基态原子的未成对电子数比Fe多的元素为________
基态Fe原子的价层电子轨道表达式为________________________________;同周期元素中,基态原子的未成对电子数比Fe多的元素为________![]() 填元素符号
填元素符号![]() 。
。
![]() 常温下,五羰基铁
常温下,五羰基铁![]() 为黄色液体,其晶体类型为________________;CO与
为黄色液体,其晶体类型为________________;CO与![]() 互为等电子体,二者中沸点较高的是________,原因为________________________。
互为等电子体,二者中沸点较高的是________,原因为________________________。
![]() 普鲁士蓝的化学式为
普鲁士蓝的化学式为![]() ,碳原子与
,碳原子与![]() 形成配位键,其中提供孤电子对的是________
形成配位键,其中提供孤电子对的是________![]() 填元素符号
填元素符号![]() ,
,![]() 中碳原子的杂化方式为________,1mol普鲁士蓝中所含
中碳原子的杂化方式为________,1mol普鲁士蓝中所含![]() 键的数目为________________。
键的数目为________________。
![]() 邻羟基苯甲醛
邻羟基苯甲醛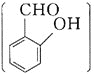 和对羟基苯甲醛
和对羟基苯甲醛 均能与
均能与![]() 溶液反应生成紫色配合物。对羟基苯甲醛在水中的溶解度略大于邻羟基苯甲醛在水中的溶解度,原因为________________________________________________________。
溶液反应生成紫色配合物。对羟基苯甲醛在水中的溶解度略大于邻羟基苯甲醛在水中的溶解度,原因为________________________________________________________。
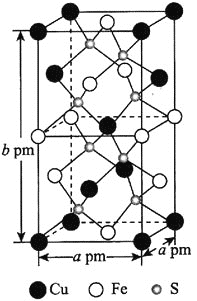
![]() 某含铁化合物的长方体晶胞结构如图所示,该化合物的化学式为________________,晶胞中距离Fe原子最近的S原子有________个,若阿伏加德罗常数的值为
某含铁化合物的长方体晶胞结构如图所示,该化合物的化学式为________________,晶胞中距离Fe原子最近的S原子有________个,若阿伏加德罗常数的值为![]() ,则该晶体的密度为________________________
,则该晶体的密度为________________________![]() 用含有
用含有![]() 、a、b的代数式表示
、a、b的代数式表示![]() 。
。
查看答案和解析>>
科目: 来源: 题型:
【题目】姜黄素是一种天然染料,工业上可用石油的裂解产物通过如图反应制得:
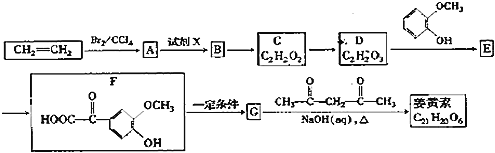
已知:![]()
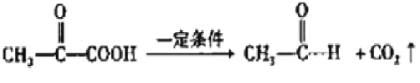
![]() CH3CHO+
CH3CHO+![]()
![]()
![]() +H2O
+H2O
请回答下列问题:
![]() 试剂X为 ______ ;
试剂X为 ______ ;
![]() 最多能消耗Na、NaOH、
最多能消耗Na、NaOH、![]() 的物质的量分别为3mo1、2mol、1mol,则E的结构简式为 ______ ;
的物质的量分别为3mo1、2mol、1mol,则E的结构简式为 ______ ;
![]() 姜黄素中的含氧官能团除甲氧基
姜黄素中的含氧官能团除甲氧基![]() 外还有 ______
外还有 ______ ![]() 写名称
写名称![]() ;
;
![]() 反应
反应![]() 的化学方程式为 ______ ,其反应类型是 ______ ;
的化学方程式为 ______ ,其反应类型是 ______ ;
![]() 符合下列条件G的同分异构体共有 ______ 种,其中核磁共振氢谱中有5组峰,且面积比为2:2:2:1:1的是 ______ ;
符合下列条件G的同分异构体共有 ______ 种,其中核磁共振氢谱中有5组峰,且面积比为2:2:2:1:1的是 ______ ;
①属于芳香酯类 ②苯环上有两个取代基 ③能与![]() 溶液发生显色反应
溶液发生显色反应
![]() 借鉴制取姜黄素的方法也能合成肉桂醛(
借鉴制取姜黄素的方法也能合成肉桂醛(![]() ),写出制备肉桂醛所需有机物的结构简式 ______ 。
),写出制备肉桂醛所需有机物的结构简式 ______ 。
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上以碳酸锰矿(主要成分为MnCO3,另含FeO、Fe2O3、CaO等杂质)为主要原料生产锰酸锂(LiMn2O4)的工艺流程如下:
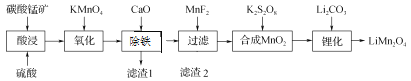
已知:部分离子沉淀的pH值。
离子 | 开始沉淀的pH值 | 沉淀完全时的pH值 |
Mn2+ | 8.8 | 10.8 |
Fe2+ | 7.5 | 9.5 |
Fe3+ | 2.2 | 3.5 |
(1) 为了提高碳酸锰矿浸岀的速率,在“酸浸”时可采取的措施有:①适当升高温度;②搅拌;③_____等。
(2) 氧化时发生的离子方程式:_________。
(3) 加入CaO“除铁”的原理是____________。
(4) 加入MnF2为了除去溶液中的Ca2+,若控制溶液中F-浓度为3×10-3 mol·L-1,则Ca2+的浓度为________mol·L-1[常温时,Ksp(CaF2)=2.7×10-11]。
(5) “锂化”是将MnO2和Li2CO3按4∶1的物质的量比配料,球磨3~5 h,然后升温至600~750 ℃,保温24 h,自然冷却至室温得产品。升温到515 ℃时,开始有CO2产生,比预计碳酸锂的分解温度(723 ℃)低得多。可能的原因是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】铁镁合金是目前已发现的储氢密度较高的储氢材料之一,其晶胞结构如图所示(黑球代表 Fe,白球代表 Mg)。则下列说法不正确的是
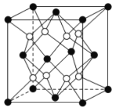
A.铁镁合金的化学式为 Mg2FeB.晶体中存在的化学键类型为金属键、离子键
C.晶胞中 Fe与 Mg的配位数均为4D.该晶胞的质量是![]() g
g
查看答案和解析>>
科目: 来源: 题型:
【题目】不同浓度的硫酸与锌反应时,硫酸可以被还原为SO2,也可被还原为氢气。为了验证这一事实,某同学拟用下图装置进行实验(实验时压强为10lkPa,温度为0℃)。
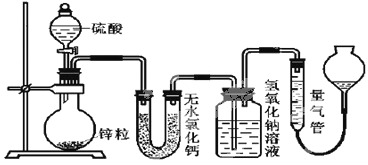
(1)若在烧瓶中放入1.30g锌粒,与cmol/LH2SO4反应,为保证实验结论的可靠,量气管的适宜规格是__。
A.200mL B.400mL C.500mL
(2)若1.30g锌粒完全溶解,氢氧化钠洗气瓶增重l.28g,则圆底烧瓶中发生反应的化学方程式为:__。
(3)若烧瓶中投入ag锌且完全反应,氢氧化钠洗气瓶增重bg。量气瓶中收集到VmL气体,则有:![]() ,依据的原理是___。
,依据的原理是___。
(4)若在烧瓶中投入dg锌,加入一定量的cmol/L浓硫酸VL,充分反应后锌有剩余,测得氢氧化钠洗气瓶增重mg,则整个实验过程产生的气体中,![]() =__(用含字母的代数式表示)。若撤走盛有无水氯化钙的U型管,
=__(用含字母的代数式表示)。若撤走盛有无水氯化钙的U型管,![]() 的数值将__(填偏大、偏小或无影响)。
的数值将__(填偏大、偏小或无影响)。
(5)反应结束后,为了准确地测量气体体积,除了待冷却至室温才开始读数外,量气管在读数时还应注意:①___;②___。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A的产量通常用来衡量一个国家的石油化工水平,现以A为主要原料合成一种具有果香味的物质E,其合成路线如下图所示。
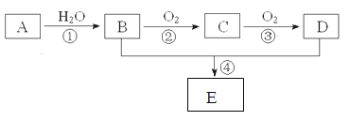
请回答下列问题:(电子式和化学方程式书写每空2分,其余每空1分)
(1)写出A的电子式 ,B、D分子中的官能团名称分别是 、 。
(2)写出下列反应的化学方程式,并注明反应类型:
① , ;
② , ;
④ , 。
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、 Z三种可溶性盐,其阳离子分别是Ba2+、Cu2+、Ag+中的某一种,阴离子分别是Cl-、SO42-、NO3-中的某一种。现做以下实验:
①将三种盐各取少量,分别溶于盛有5 mL蒸馏水的三支试管中,只有X盐溶液呈蓝色。
②分别向三支试管中加入2 mL稀盐酸,发现Y盐溶液中产生白色沉淀,Z盐溶液无明显现象。
(1)根据上述事实,推断这三种盐的化学式:X______,Y______,Z______。
(2)若上述三种阳离子Ba2+、Cu2+、Ag+对应的盐都为硝酸盐,将其混合配成溶液,选择合适试剂,将这三种离子逐一沉淀分离。其流程图如下:

部分物质溶解性表为
Ba2+ | Cu2+ | Ag+ | |
Cl- | 溶 | 溶 | 不 |
CO32- | 不 | 不 | 不 |
SO42- | 不 | 溶 | 微 |
S2- | 溶 | 不 | 不 |
①沉淀1的化学式为_________________。
②写出混合溶液与试剂A反应的离子方程式:______________。
③若C为Na2S,且它与B的阳离子相同,则试剂B的名称是____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A.氯气溶于水:Cl2+H2O=2H++Cl-+ClO-
B.Na2CO3溶液呈碱性的原因:CO![]() +H2O=HCO
+H2O=HCO![]() +OH-
+OH-
C.NaHCO3溶液中加足量Ba(OH)2溶液:HCO![]() +Ba2++OH-=BaCO3↓+H2O
+Ba2++OH-=BaCO3↓+H2O
D.酸性溶液中KIO3与KI反应生成I2:IO![]() +I-+6H+=I2+3H2O
+I-+6H+=I2+3H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,向容积为2 L的密闭容器中充入一定量的气体A和气体B,发生反应: 2A(g)+B(g) ![]() 2C(g),反应过程中测定部分数据见下表(表中t1<t2),下列说法正确的是
2C(g),反应过程中测定部分数据见下表(表中t1<t2),下列说法正确的是
反应时间/min | n(A)/mol | n(B)/mol |
0 | 0.10 | 0.060 |
t1 | 0.012 | |
t2 | 0.016 |
A.在0~t1 min内的平均反应速率为v(C)=![]() molL-1min-1
molL-1min-1
B.其他条件不变,起始时向容器中充入0.10 mol C和0.010 mol B,平衡时n(A)=0.012 mol
C.保持其他条件不变,升高温度,平衡时c(A)=0.0070 molL-1,则反应的ΔH<0
D.相同温度下,起始时向容器中充入0.15mol A和0.090mol B,平衡时A转化率小于88%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com