
科目: 来源: 题型:
【题目】发酵法制酒精的过程可粗略表示如下:
①(C6H10O5)n+nH2O![]() nC6H12O6 ②C6H12O6
nC6H12O6 ②C6H12O6![]() 2C2H5OH+2CO2↑
2C2H5OH+2CO2↑
(1)上述化学方程式中(C6H10O5)n可能表示_____ ____(填物质名称);
(2)C6H12O6名称是_________,常用_____ ____试剂来检验其存在;
(3)为检验苹果成熟过程中发生了反应①,可在青苹果汁中滴加碘酒,溶液呈_________色,向熟苹果汁中加入Cu(OH)2悬浊液,加热,反应生成____ ____(填实验现象);
(4)下列作用不属于水解反应的是_________
A.吃馒头时多咀嚼后有甜味
B.淀粉溶液和稀硫酸共热一段时间后,滴加碘水不显蓝色
C.不慎将浓硝酸沾到皮肤上会出现黄色斑痕
D.油脂与氢氧化钠溶液共煮后可以制得肥皂
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于苯的叙述正确的是( )
A.苯的分子式为C6H6,它不能使酸性KMnO4溶液褪色,属于饱和烃
B.从苯的凯库勒式(![]() )看,苯分子中含有碳碳双键,应属于烯烃
)看,苯分子中含有碳碳双键,应属于烯烃
C.在催化剂作用下,苯与液溴反应生成溴苯,发生了加成反应
D.苯分子为平面正六边形结构,6个碳原子之间的价键完全相同
查看答案和解析>>
科目: 来源: 题型:
【题目】某溶液中可能含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的质量随加入的NaOH的物质的量的变化如图所示:
等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的质量随加入的NaOH的物质的量的变化如图所示:

(1)由此可知,该溶液中肯定含有的离子是______________________________________,且各离子的物质的量之比为___________________________________________
(2)该溶液中肯定不含的阳离子是________________。
(3)写出NaOH的物质的量从8mol到9mol发生的离子反应方程式:____________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】向100 mLBaCl2、AlCl3、FeCl3的混合溶液A中,逐滴加入Na2SO4和NaOH的混合溶液B,产生的沉淀和加入混合溶液B的体积关系如下图所示:

(1)加入B溶液110 mL时,溶液中的沉淀是______,溶液中的溶质是__________。
(2)从90 mL至100mL之间加入10mL B溶液时发生的离子反应方程式是:Ba2++ SO42—=BaSO4↓,Al(OH)3+ OH— =AlO2— +2H2O,溶液B中Na2SO4与NaOH的物质的量浓度之比为____;
(3)计算A溶液中AlCl3的物质的量浓度,_______________写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
【题目】把由NaOH、![]() 、
、![]() 三种固体组成的混合物溶于足量的水中,有
三种固体组成的混合物溶于足量的水中,有![]() 白色沉淀析出,向所得的浑浊液中逐滴加入
白色沉淀析出,向所得的浑浊液中逐滴加入![]() 的盐酸,加入盐酸的体积和生成沉淀的质量如图所示。
的盐酸,加入盐酸的体积和生成沉淀的质量如图所示。
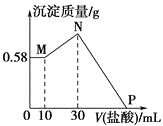
(1)混合物中NaOH的质量是________g,![]() 的质量是________g,
的质量是________g,![]() 的质量是________g。
的质量是________g。
(2)![]() 点加入盐酸的体积为________mL。
点加入盐酸的体积为________mL。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图表示从废旧普通锌锰电池内容物中回收制备KMnO4等物质的一种工艺(不考虑废旧电池中实际存在的少量其他金属)。
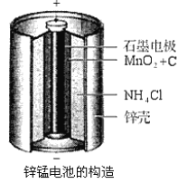
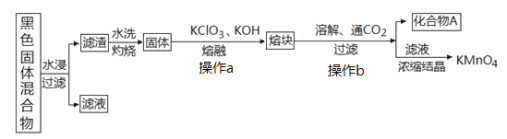
(1)KMnO4稀溶液是一种常用消毒剂,其消毒机理与下列物质相似的是______________(填序号)
A.双氧水B.75%酒精C.84消毒液(NaClO溶液)D.苯酚
(2)①黑色固体混合物水浸时为提高浸出速率,常采用的措施为_____________________(答出一条即可)。
②滤渣水洗灼烧后固体是一种黑色的化合物,操作a中得到熔块的主要成分是K2MnO4和KCl,该过程中发生反应的化学方程式为:_____________________________。
③图中产物A是一种难溶于水的黑色固体,常在有些反应中作催化剂,其化学式为:_________________。
(3)某实验小组用提纯后的KMnO4配置成0.1000mol/L溶液来测定某试样中过氧化氢的含量
①查阅资料后发现H2O2为二元弱酸,其酸性比碳酸弱。请写出H2O2在水溶液中的电离方程式:_____。
②配制250mL0.100mol/L标准KMnO4溶液,需要使用的玻璃仪器有烧杯、胶头滴管、量筒和、___________;
③滴定反应原理为2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑,该反应中H2O2体现___________(填“氧化性”、“还原性”、“酸性”);
④用0.100mol/L标准KMnO4溶液滴定含H2O2试样的溶液时,KMnO4溶液(酸化)放在_____滴定管中,并判断滴定至终点的现象是_____。
⑤用移液管吸取25.00mL试样置于锥形瓶中,重复滴定四次,每次消耗的高锰酸钾体积如表所示:
第一次 | 第二次 | 第三次 | 第四次 | |
体积(mL) | 17.10 | 18.10 | 17.00 | 16.90 |
则试样中过氧化氢的浓度为___________mol/L。
⑥下列操作会引起测定结果偏高的是___________。
A.滴定管在盛装高锰酸钾前未润洗
B.滴定过程中,锥形瓶震荡的太剧烈,以致部分液体溅出
C.滴定前读数正确,滴定终点时俯视读数
D.锥形瓶未用待测液润洗
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)已知:![]()
![]()
![]() +H2(g) ΔH=+124 kJ·mol-1,若反应体系达到平衡后,各物质的浓度在不同条件下(只改变一种条件)的变化状况如图所示(第10 min到14 min的
+H2(g) ΔH=+124 kJ·mol-1,若反应体系达到平衡后,各物质的浓度在不同条件下(只改变一种条件)的变化状况如图所示(第10 min到14 min的![]() 浓度变化曲线未表示出):
浓度变化曲线未表示出):
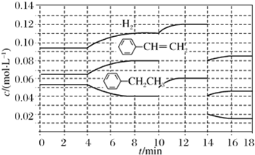
①第2 min反应温度T(2)与第8 min反应温度T(8)的高低:T(2)________(填“<”、“>”或“=”)T(8);第10 min时反应改变的条件是_______________________________。
②比较产物苯乙烯在2~3 min、5~6 min和12~13 min时平均反应速率[平均反应速率分别以v(2~3)、v(5~6)、v(12~13)表示]的大小___________。
(2)页岩气的主要成分为CH4,请回答下列问题:
①已知甲烷的燃烧热为890 kJ/mol;N2与O2反应生成NO的过程如下:
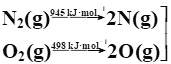
![]() 2NO(g)
2NO(g)
则CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(l) ΔH=______kJ/mol。
②页岩气可用于生产合成气(CO和H2)其反应的热化学方程式为CH4(g)+H2O(g)CO(g)+3H2(g) ΔH=206.2 kJ/mol。对于气相反应,用各组分的平衡压强(p)表示平衡常教(记作Kp),则生产合成气的Kp=_____(写出计算的表达式),你认为可同时提高化学反应速率和CH4转化率的措施是 ______(答出一条即可)。
③在某一给定进料比的情况下,温度、压强对平衡时H2物质的量分数的影响如图所示。
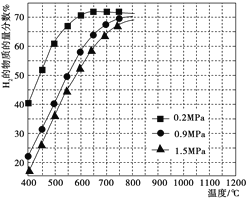
由图可知,在相同温度下,CH4的转化率随压强的增大而________(填“增大”“减小”或“不变”)。若要达到H2的物质的量分数>65%,以下条件中最合适的是_________(填序号)。
a.600℃,0.2 MPa b.600℃,0.9 MPa
c.700℃,0.9 MPa d.800℃,1.5 MPa
查看答案和解析>>
科目: 来源: 题型:
【题目】溶液中的化学反应大多数是离子反应,根据要求回答问题
(1)盐碱地(含较多NaCl、Na2CO3)不利于作物生长,通过施加适量石膏可以降低土壤的碱性.试用离子方程式表示:①盐碱地产生碱性的原因________、_________;
②Na2CO3溶液中离子浓度大小顺序为__________________________________________;
(2)常温下,等物质的量浓度的①氨水;②NH4HSO4;③NH4Cl;④(NH4)2CO3;⑤(NH4)2SO4溶液中,c(NH4+)由大到小的顺序为 > > > > (填序号).__________
(3)常温下,在pH=6的CH3COOH与CH3COONa的混合溶液中,水电离出来的c(OH-)=____________.
(4)常温下,将amol/L的醋酸与0.01mol/L的氢氧化钠溶液等体积混合,反应平衡时溶液中c(Na+)=c(CH3COO-),则溶液显 _________(填“酸”“碱”“中”)性,用含a的代数式表示CH3COOH的电离平衡常数Ka= ________________ 。
查看答案和解析>>
科目: 来源: 题型:
【题目】![]() 在铜版印刷中用作印刷电路铜板腐蚀剂,按要求回答下列问题:
在铜版印刷中用作印刷电路铜板腐蚀剂,按要求回答下列问题:
(1)氯化铁溶液腐蚀铜板的离子方程式: ______ .
(2)将5至6滴饱和氯化铁溶液滴入到25mL沸水中,继续加热,得红褐色液体.
写出反应的离子方程式: ______ .
(3)向100mL![]() 硫酸铝铵
硫酸铝铵![]() 溶液中逐滴滴入
溶液中逐滴滴入![]()
![]() 溶液.随着
溶液.随着![]() 溶液体积V的变化,沉淀物质的量n的变化如图所示:
溶液体积V的变化,沉淀物质的量n的变化如图所示:
①请认真思考,写出相应的离子方程式:
OA段: ______
OB段: ______
BC段: ______
CD段: ______

②当![]() 离子恰好全部沉淀时,生成
离子恰好全部沉淀时,生成![]() 物质的量为 ______ mol.
物质的量为 ______ mol.
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各表述与示意图一致的是
A. 如图表示向含
如图表示向含![]() 、
、![]() 、
、![]() 的盐溶液中滴加NaOH溶液时,沉淀的量与NaOH的体积关系图.则三种离子的物质的量之比为:
的盐溶液中滴加NaOH溶液时,沉淀的量与NaOH的体积关系图.则三种离子的物质的量之比为:![]() :
:![]() :
:![]()
![]() :1:2,其中使用的NaOH的浓度为2
:1:2,其中使用的NaOH的浓度为2![]()
B. 如图中曲线表示某反应过程的能量变化,当物质
如图中曲线表示某反应过程的能量变化,当物质![]() 与
与![]() 反应生成物质
反应生成物质![]() 是,
是,![]() ,若使用正催化剂,E值会减小
,若使用正催化剂,E值会减小
C.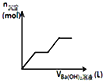 如图可用来表示向盐酸酸化的
如图可用来表示向盐酸酸化的![]() 溶液中加入
溶液中加入![]() 溶液时,产生沉淀的物质的量
溶液时,产生沉淀的物质的量![]() 与加入
与加入![]() 溶液体积
溶液体积![]() 之间的关系图
之间的关系图
D. 如图表示向一定质量的明矾溶液中滴加
如图表示向一定质量的明矾溶液中滴加![]() 溶液时,产生沉淀的质量
溶液时,产生沉淀的质量![]() 与加入
与加入![]() 溶液体积
溶液体积![]() 之间的关系图
之间的关系图
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com