
科目: 来源: 题型:
【题目】碳和硫是高中化学学习的两种重要非金属元素
(1)下列C原子的电子排布式表达的状态中能量最高的是_____。
A 1s22s22p2 B.1s22s22px12py1 C.1s22s22px12pz1 D.1s22s12px12py12pz1
(2)硫有一种结构为![]() 的分子(灰球代表硫原子)。其中硫原子杂化方式为_____。
的分子(灰球代表硫原子)。其中硫原子杂化方式为_____。
(3)Fe(CO)5可用作催化剂、汽油抗爆剂等,其分子中σ键和π键的数目之比为_____。
(4)已知CS2晶体结构类似于干冰。CS2晶体中与每个CS2分子距离最近且等距的CS2分予有_____个。推测CS2晶体密度与冰的晶体密度较大的为_____。可能的原因是_____。又知CS2晶体中晶胞参数是apm,NA表示阿佛加德罗常数的值,晶体密度为_____g/cm3(用含a、NA等符号的表达式表示)。
(5)Na2S是高子晶体,其晶格能可通过图的Born﹣Haber循环计算得到。
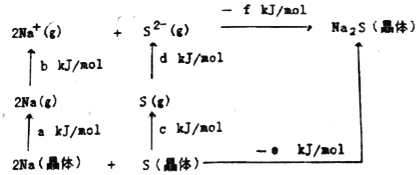
由此可知,Na原子的第一电离能为_____kJ/mol,Na2S的晶格能为_____kJ/mol。(用图中给出的符号作答)
查看答案和解析>>
科目: 来源: 题型:
【题目】【物质结构与性质,1 3分】
(1)与铜同周期、基态原子最外层电子数相同的过渡元素,其基态原子的电子排布式______________。
(2)下图曲线表示部分短周期元素的原子序数(按递增顺序排列)和其常见单质沸点的关系。其中A点表示的单质是________(填化学式)。

(3)三氟化硼分子的空间构型是__________;三溴化硼、三氯化硼分子结构与三氟化硼相似,如果把B—X键都当作单键考虑来计算键长,理论值与实测键长结果如下表。硼卤键长实测值比计算值要短得多,可能的原因是____________________________________________。

(4)CuCl的盐酸溶液能吸收CO生成复合物氯化羰基亚铜【Cu2C12(CO)2·2H20】,其结构如图。

①该复合物中Cl原子的杂化类型为_______________。
②该复合物中的配位体有________________种。
(5)已知HF与Fˉ通过氢键结合成![]() 。判断
。判断![]() 和
和![]() 微粒间能否形成氢键,并说明理由。____________________________________。
微粒间能否形成氢键,并说明理由。____________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上常釆用乙苯催化脱氢制苯乙烯,方程式为:![]() (g)
(g)![]()
![]() (g)+H2(g)
(g)+H2(g)
(1)已知:
化学键 | C﹣H | C﹣C | C=C | H﹣H |
键能/kJmol﹣1 | 412 | 348 | 612 | 436 |
计算上述反应的△H=_____kJmol﹣1。
(2)①利用计算结果与反应特点,选择理论上有利于提高苯乙烯平衡产率的条件_____。
A.低温 B.高温 C.高压 D.低压 E.合适的催化剂
②实际工业生产中常伴有乙苯裂解等副反应。而乙苯裂解反应无论在热力学还是在动力学上都比乙苯脱氢更有利,所以工业生产要使反应向脱氢方向进行需要采用_____条件来提高反应的选择性。
③工业生产中常采用恒压条件下向乙苯蒸汽中掺入水蒸气或CO2的办法来提高乙苯的平衡转化率,请从平衡移动的角度加以说明_____。
(3)利用膜反应新技术,可以实现边反应边分离出生成的氢气不同温度下,1.00mol乙苯在容积为1.00L的密闭容器中反应,氢气移出率α与乙苯平衡转化率关系如图所示:
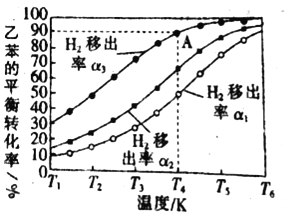
氢气移出率α![]()
①同温度时α1、α2、α3依次_____,(填“增大”“减小”)原因是_____。
②A点平衡常数为0.45mol/L,则α为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,将体积为V1的0.1000 molL﹣1 HCl溶液逐滴加入到体积为V2的0.1000 molL﹣1 Na2SO3溶液中,Na2SO3水溶液中H2SO3、HSO3﹣、SO32﹣在含硫微粒中的物质的量分数随pH的分布如图所示,下列说法正确的是( )
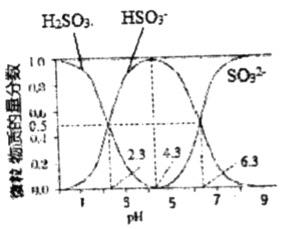
A.在pH=4.3时,溶液中:V1=2V2
B.在pH=2.3时,溶液中:0.1000mol/L>c(HSO3﹣)+c(SO32﹣)+c(H2SO3)
C.在pH=6.3时,溶液中,c(Na+)=c(Cl﹣)
D.在pH=7时,溶液中,c(Na+)=c(HSO3﹣)+2c(SO32﹣)
查看答案和解析>>
科目: 来源: 题型:
【题目】氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要应用.请回答下列问题。
(1)氮、磷、砷的电负性的大小关系是 ,砷原子M层电子排布式为 。
(2)K3[Fe(CN)6]晶体中Fe3+与CN-之间的键型为 ,该化学键能够形成的原因是 。
(3)已知:
CH4 | SiH4 | NH3 | PH3 | |
沸点(K) | 101.7 | 161.2 | 239.7 | 185.4 |
分解温度(K) | 873 | 773 | 1073 | 713.2 |
分析上表中四种物质的相关数据,请回答:
① CH4和SiH4比较,沸点高低的原因是 。
② NH3和PH3比较,分解温度高低的原因是 。
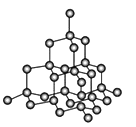
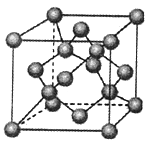
(4)金刚石是原子晶体,含有的最小环是六元环(如右边图),每个碳原子连接 个六元环,如左边图是金刚石的晶胞,若碳原子半径为r,金刚石晶胞的边长为a,根据硬球接触模型,碳原子在晶胞中的空间占有率 (不要求计算过程)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某原电池装置如图所示,电池总反应为2Ag+Cl2═2AgCl(忽略溶液体积变化)下列关于该电池装置工作时的说法正确的是( )
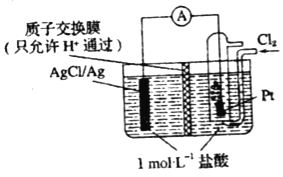
A.H+向左侧迁移
B.若有11.2L氯气(标准状况)参与反应,左侧电极质量增加71 g
C.左侧电极区反应为Ag﹣e﹣═Ag+
D.若把质子交换膜换成阴离子交换膜,一段时间右侧c(HCl)几乎不变
查看答案和解析>>
科目: 来源: 题型:
【题目】关于原电池装置Ⅰ若把盐桥(含氯化钾的琼胶)换成粗铜丝,左侧电解质溶液换成硫酸铜溶液,如图Ⅱ所示,两装置均工作一段时间(假设电极材料和电解质溶液均充足,且忽略能量损耗),关于以上两装置说法正确的是( )

A.两装置中锌(a)、锌 (c)两电极均发生氧化反应
B.当装置Ⅰ池铜(b)电极增重64g时,盐桥中转移2mol电子
C.取出Ⅱ装置中粗铜丝小心洗涤干燥称重比原铜丝质量轻
D.I池右侧硫酸铜溶液浓度几乎不变
查看答案和解析>>
科目: 来源: 题型:
【题目】K2Cr2O7溶液中存在平衡:Cr2O72﹣(橙色)+H2O2CrO42﹣(黄色)+2H+.已知Cr2O72﹣有强氧化性,而CrO42﹣则几乎没有氧化性,Cr3+呈绿色。向K2Cr2O7溶液中加入以下物质,关于溶液颜色变化的说法不正确的是( )
A.加70%的硫酸,溶液变橙色
B.加30%NaOH溶液,溶液变黄色
C.加70%的硫酸后再加C2H5OH,溶液可变成绿色
D.加30%NaOH溶液后,溶液变黄色,加C2H5OH无变化,再加过量硫酸,溶液仍无明显变化
查看答案和解析>>
科目: 来源: 题型:
【题目】根据元素周期表回答下列问题:
(1)写出元素Cu的基态原子的电子排布式:____________________。
(2)某元素A的核外价电子排布式为nsnnpn+1,该元素A原子核外最外层电子中成对电子共有________对。此元素A原子与O的第一电离能的相对大小为:A________ O(填“<”“>”或“=”)。
(3)元素C形成的最高价氧化物中含有________个π键。C和Cl形成化合物的电子式为_____________,此化合物中C的杂化方式为________。
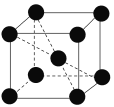
(4)已知元素钒形成单质的晶胞如下图所示,则其原子的配位数是________,假设晶胞的边长为d cm、密度为ρ g·cm-3,则元素钒的相对原子质量为_____________ (NA为阿伏加德罗常数)。
查看答案和解析>>
科目: 来源: 题型:
【题目】SO2溶于水生成亚硫酸,亚硫酸的酸性强于次氯酸。选择下面的装置和药品来探究亚硫酸与次氯酸的酸性强弱。仪器选择、连接顺序正确的是(SO2发生装置己略去,且通入的SO2纯净)( )
①NaHCO3溶液 ②品红溶液
②品红溶液 ③酸性KMnO4溶液
③酸性KMnO4溶液 ④漂白粉溶液
④漂白粉溶液
A.→②→④B.→①→③→②→④C.→②→①→④→③D.→①→④→②
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com