
科目: 来源: 题型:
【题目】25 ℃时,水的电离达到平衡:H2O![]() H++OH-;△H>0,下列叙述正确的是
H++OH-;△H>0,下列叙述正确的是
A.向水中加入少量固体NaHSO4,c(H+)增大,KW不变
B.向水中加入少量NaOH溶液,平衡逆向移动,c(OH-)降低
C.向水中加入少量CH3COONa固体,平衡逆向移动,c(H+)降低
D.将水加热,KW增大,pH不变
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,几种难溶金属氢氧化物分别在溶液中达到沉淀溶解平衡后,改变溶液的pH,金属阳离子浓度的变化如图所示。下列说法正确的是
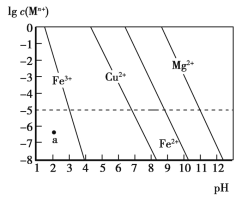
A.a点代表Fe(OH)3的饱和溶液
B.Ksp[Cu(OH)2]<Ksp[Fe(OH)2]
C.向0.1 mol·L-1Cu2+、Mg2+、Fe2+混合溶液中,逐滴滴加稀NaOH溶液,Mg2+最先沉淀
D.在pH=7的溶液中,Cu2+、Mg2+、Fe2+能大量共存
查看答案和解析>>
科目: 来源: 题型:
【题目】在生产生活和科学研究中,人们常常根据需要促进或抑制盐的水解。试回答下列问题:
(1)FeCl2溶液呈____(填“酸”、“中”、“碱”)性,原因是(用离子方程式表示):____;实验室在配制FeCl2溶液时,常将FeCl2固体先溶于较浓的盐酸中,以_____(填“促进”、“抑制”)其水解,然后再用蒸馏水稀释到所需的浓度。
(2)用离子方程式表示硫酸铝溶液和碳酸氢钠溶液混合时发生的主要反应____。
(3)为证明盐的水解是吸热的,四位同学分别设计了如下方案,其中正确的是____。
A.甲同学:在盐酸中加入氨水,混合液温度上升,说明盐类水解是吸热的。 |
B.乙同学:将硝酸铵晶体溶于水,水温降低,说明盐类水解是吸热的。 |
C.丙同学:在氨水加入氯化铵固体,溶液的pH变小,说明盐类水解是吸热的。 |
D.丁同学:在醋酸钠溶液中滴加2滴酚酞试剂,加热后红色加深,说明盐类水解是吸热的。 |
(4)把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是___。
查看答案和解析>>
科目: 来源: 题型:
【题目】按要求对图中两极进行必要的连接并填空:
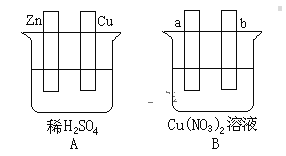
(1)在A图中,使铜片上冒H2气泡。请加以必要连接,则连接后的装置叫____。电极反应式:锌板:____;铜板:_____。
(2)在B图中,使a极析出铜,b极析出氧气。加以必要的连接后,该装置叫____。电极反应式,a极:____;b极:_____。经过一段时间后,停止反应,溶液的pH值____(升高、降低、不变),加入一定量的____后,溶液能恢复至与电解前完全一致。
查看答案和解析>>
科目: 来源: 题型:
【题目】恒容密闭容器中进行的可逆反应2NO2![]() 2NO +O2,可作为达到平衡状态的标志是( )
2NO +O2,可作为达到平衡状态的标志是( )
①单位时间内生成amo1O2的同时生成2amolNO2 ;
②单位时间内生成amolO2的同时生成2amolNO;
③混合气体的颜色不再改变;
④混合气体的密度不再改变的状态;
⑤混合气体的平均相对分子质量不再改变的状态;
⑥容器内的压强不再改变。
A.①②③④⑤B.②④⑤⑥C.①③④⑥D.①③⑤⑥
查看答案和解析>>
科目: 来源: 题型:
【题目】下列事实一定能说明HF是弱酸的是( )
①常温下NaF溶液的pH大于7; ②用HF溶液做导电性实验,灯泡很暗;
③HF与NaCl不能发生反应; ④常温下0.1mol/L的HF溶液的pH为2.3
⑤HF能与Na2CO3溶液反应,产生CO2气体 ⑥HF与水能以任意比混溶
⑦1mol/L的HF水溶液能使紫色石蕊试液变红
A. ①④ B. ②③⑤ C. ③④⑥ D. ①②⑦
查看答案和解析>>
科目: 来源: 题型:
【题目】为了配制NH4+浓度与Cl-的浓度比为1:1的溶液,可在NH4Cl溶液中加入:①适量HCl②适量NaCl③适量的氨水④适量的NaOH,正确的是
A. ①② B. ④ C. ③④ D. ③
查看答案和解析>>
科目: 来源: 题型:
【题目】下列方程式书写正确的是( )
A.HCO3-在水溶液中的电离方程式:HCO3-+H2O![]() H3O++CO32-
H3O++CO32-
B.H2SO3的电离方程式H2SO3![]() 2H++SO32-
2H++SO32-
C.CO32-的水解方程式:CO32-+2H2O![]() H2CO3+2OH-
H2CO3+2OH-
D.CaCO3的电离方程式:CaCO3Ca2++CO32-
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室用标准盐酸溶液测定某NaOH溶液的浓度,用甲基橙作指示剂,下列操作中可能使测定结果偏低的是( )
A.酸式滴定管在装酸液前未用标准盐酸溶液润洗2~3次
B.开始实验时酸式滴定管尖嘴部分有气泡,在滴定过程中气泡消失
C.锥形瓶内溶液颜色变化由黄色变橙色,立即记下滴定管液面所在刻度
D.盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗2~3次
查看答案和解析>>
科目: 来源: 题型:
【题目】甲醇是一种重要的化工原料,在化工领域有广泛应用。
(1)甲醇燃料电池由于结构简单、能量转化率高、对环境天污染,可作为常规能源的替代品而越来越受到关注。其工作原理如如图所示:
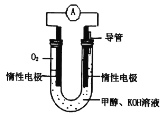
①该电池正极的电极反应为___,放电过程中负极区域溶液的pH值___(填“变大”或“变小”或“不变”)。
②该电池总反应的化学方程式为___。
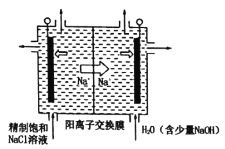
(2)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高校、光谱、安全的杀菌消毒剂。目前已开发出用电解法制取ClO2的新工艺。
①如图中用石墨作电极,在一定条件下电解饱和食盐水制取ClO2。则阳极产生ClO2的电极反应式为____。
②电解一段时间,当阴极产生的气体体积为112mL(标准状况)时,停止电解。通过阳离子交换膜的阳离子的物质的量为___mol。
(3)英国《自然》杂志近期报道了一种新型铝离子电池,以金属铝和石墨为电极,用A1Cl4-和有机阳离子构成电解质溶液,其放电工作原理如图所示。
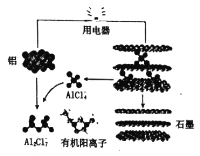
①电池放电时负极的电极反应式为___。
②充电时有机阳离子向___电极移动(填“铝”或“石墨”)。
③电池充电时,电路中每转移0.15mol电子,理论上生成___g铝。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com