
ĚâÄżÁбí(°üŔ¨´đ°¸şÍ˝âÎö)
10Ł®°ŃŇ»¶¨ÁżµÄNaHCO3şÍNa2O2µÄ»ěşĎÎď·ĹÔÚĂܱŐČÝĆ÷ÖĐĽÓČȡŁąŘÓÚ»ěşĎÎďĽÓČČÇ°şóĎűşÄŃÎËáµÄÎďÖʵÄÁżŁ¬ĎÂÁĐ˝áÂŰĹжĎŐýČ·µÄĘÇ
AŁ®ĽÓČČÇ°ĎűşÄµÄ¶ŕˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ
BŁ®ĽÓČČşóĎűşÄµÄ¶ŕ
CŁ®ĽÓČČÇ°ĽÓČČşóĎűşÄµÄŇ»Ńů¶ŕˇˇˇˇˇˇˇˇˇˇˇˇˇˇ
DŁ®˛»ÖŞNaHCO3şÍNa2O2ş¬ÁżÎŢ·¨Č·¶¨
9Ł®¶ÔÓÚżÉÄć·´Ó¦N2(g)+3H2(g)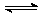 2NH3(g)Ł»ˇ÷HŁĽ0Ł¬ĎÂÁĐŃĐľżÄżµÄşÍĘľŇâÍĽĎŕ·űµÄĘÇ
2NH3(g)Ł»ˇ÷HŁĽ0Ł¬ĎÂÁĐŃĐľżÄżµÄşÍĘľŇâÍĽĎŕ·űµÄĘÇ
|
ˇˇ |
A |
B |
C |
D |
|
ŃĐľżÄżµÄ |
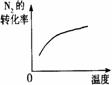
ѹǿ¶Ô·´Ó¦µÄÓ°Ďě(P2>P1) |
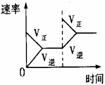
ζȶԷ´Ó¦µÄÓ°Ďě |
Ć˝şâĚĺϵÔöĽÓN2¶Ô·´Ó¦µÄÓ°Ďě |
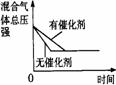
´ß»ŻĽÁ¶Ô·´Ó¦µÄÓ°Ďě |
|
ÍĽĘľ |
 |
 |
 |
 |
8Ł®ŇŃÖŞŁşH2O(g)=H2O(l)Ł» ˇ÷H1= -Q1kJˇ¤mol-1
ˇˇˇˇ CH3OH(g)=CH3OH(l)Ł» ˇ÷H2= -Q2kJˇ¤mol-1
2CH3OH(g)+3O2 = 2CO2(g)+4H2O(g)Ł» ˇ÷H3= -Q3kJˇ¤mol-1(Q1,Q2,Q3ľů´óÓÚ0)
ČôŇŞĘą32gҺ̬Ľ×´ĽÍęČ«ČĽÉŐŁ¬×îşó»Ö¸´µ˝ĘŇÎÂŁ¬·ĹłöµÄČČÁżÎŞ(µĄÎ»ŁşkJ)
ˇˇˇˇ AŁ®Q1+Q2+Q3
BŁ®0.5Q3-Q2+2Q1
ˇˇˇˇˇˇ CŁ®0.5Q3+Q2-2Q1
DŁ®0.5(Q1+Q2+Q3)
7Ł®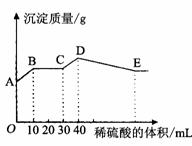 ˝«ÇâŃő»ŻÄơ˘ÂČ»Ż±µşÍÁňËáÂÁČýÖÖąĚĚĺ×éłÉµÄ»ěşĎÎďČÜÓÚ×ăÁżµÄË®ÖĐŁ¬łä·ÖČܽ⣬ÓĂ1molˇ¤L-1ϡÁňËáµÎ¶¨Ł¬ĽÓČëϡÁňËáµÄĚĺ»ýÓëÉúłÉłÁµíµÄÖĘÁżąŘϵČçÍĽËůĘľˇŁĎÂÁĐÓĐąŘĹжĎŐýČ·µÄĘÇ
˝«ÇâŃő»ŻÄơ˘ÂČ»Ż±µşÍÁňËáÂÁČýÖÖąĚĚĺ×éłÉµÄ»ěşĎÎďČÜÓÚ×ăÁżµÄË®ÖĐŁ¬łä·ÖČܽ⣬ÓĂ1molˇ¤L-1ϡÁňËáµÎ¶¨Ł¬ĽÓČëϡÁňËáµÄĚĺ»ýÓëÉúłÉłÁµíµÄÖĘÁżąŘϵČçÍĽËůĘľˇŁĎÂÁĐÓĐąŘĹжĎŐýČ·µÄĘÇ
AŁ®AµăËů±íĘľµÄłÁµíµÄ»ŻŃ§Ę˝ĘÇŁş Al(OH)3ˇ˘ BaSO4
BŁ®B~C¶ÎËů·˘Éú·´Ó¦µÄŔë×Ó·˝łĚĘ˝ĘÇŁşH+ˇˇ + OH-ˇˇ = H2O
CŁ®A~B¶ÎËů·˘Éú·´Ó¦µÄŔë×Ó·˝łĚĘ˝ĘÇŁşBa2+ + SO42- =BaSO4ˇý
DŁ®EµăËů±íĘľµÄČÜŇşÖĐŁşn (Na+) = n (Cl-)
6Ł®ÄłËáĘ˝ŃÎNaHYµÄË®ČÜŇşĎÔĽîĐÔŁ¬ĎÂÁĐĐđĘöŐýČ·µÄĘÇ
 ˇˇˇˇ AŁ®H2YµÄµçŔë·˝łĚĘ˝ŁşH2Yˇˇˇˇˇˇˇˇ 2H++Y2-
ˇˇˇˇ AŁ®H2YµÄµçŔë·˝łĚĘ˝ŁşH2Yˇˇˇˇˇˇˇˇ 2H++Y2-
ˇˇˇˇ BŁ®¸ĂËáĘ˝ŃÎČÜŇşÖĐŔë×ÓŨ¶ČąŘϵŁşc(H+)+c(Na+)=c(OH-)+c(Y2-)+c(HY-)
ˇˇˇˇ CŁ®¸ĂËáĘ˝ŃÎČÜŇşÖĐŔë×ÓŨ¶ČąŘϵŁşc(H+)+ c(H2Y) =c(OH-)+c(Y2-)
ˇˇˇˇ DŁ®¸ĂËáĘ˝ŃÎČÜŇşÖĐŔë×ÓŨ¶Č´óСąŘϵŁş c(Na+)> c(OH-)> c(H+)>c(HY-)
5Ł®ÔÚĽÓČëÂÁ·Ű˛úÉúÇâĆřµÄČÜŇşÖĐŁ¬ĎÂÁи÷×éŔë×ÓżÉÄÜ´óÁżą˛´ćµÄĘÇ
ˇˇˇˇ AŁ®NH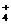 ˇ˘NO
ˇ˘NO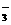 ˇ˘CO
ˇ˘CO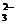 ˇ˘Na+ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ
ˇ˘Na+ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ
BŁ®Ba2+ˇ˘Mg2+ˇ˘HCO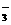 ˇ˘Na+
ˇ˘Na+
ˇˇˇˇ CŁ®H+ ˇ˘FŇ»ˇ˘K+ ˇ˘ClŁˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ
DŁ®K+ ˇ˘AlO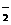 ˇ˘OHŇ»ˇ˘NO
ˇ˘OHŇ»ˇ˘NO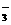
4Ł®ÓÉÁ˝ÖÖ¶ĚÖÜĆÚÔŞËŘAşÍMĐγɵÄŔë×Ó»ŻşĎÎďA2M3Ł¬A3+Ŕë×Ó±ČM2ŁŔë×ÓÉŮŇ»¸öµç
ˇˇˇˇ ×Ӳ㣬ÇŇA3+ľßÓĐÓëNeÔ×ÓĎŕͬµÄşËÍâµç×Ó˛ă˝áąąŁ¬ÔňĎÂÁĐ˵·¨ŐýČ·µÄĘÇ
ˇˇ AŁ®»ŻşĎÎďA2M3ĘÇČýŃő»Ż¶ţÂÁ
ˇˇ BŁ®A3+şÍM2Ł×îÍâµç×Ó˛ăÉϵĵç×ÓĘý¶ĽĘÇ8
ˇˇ CŁ®AµÄ×î¸ßĽŰŃő»ŻÎď¶ÔÓ¦µÄË®»ŻÎďĘÇÇżµç˝âÖĘ
ˇˇ DŁ®ÔŞËŘMĘǵÚ2ÖÜĆÚµÚVIA×ĺµÄÔŞËŘ
3Ł®ĎÂÁĐʵŃé˛Ů×÷şÍĘ¹ʴ¦ŔíÖĐŁ¬ŐýČ·µÄĘÇ
AŁ®Ňřľµ·´Ó¦ĘµŃéşó¸˝ÓĐŇřµÄĘԹܣ¬żÉÓĂϡÁňËáĎ´µÓ
BŁ®ÔÚÖĐѧˇ°ÁňËáÍľ§ĚĺÖнᾧˮş¬Áż˛â¶¨ˇ±µÄʵŃéÖĐłĆÁż˛Ů×÷ÖÂÉŮĐčŇŞËÄ´Î
CŁ®˛»É÷˝«Ĺ¨ÁňËáŐ´ÔÚƤ·ôÉĎŁ¬Á˘Ľ´ÓĂÇâŃő»ŻÄĆČÜŇşłĺĎ´
DŁ®ÔÚ250mLÉŐ±ÖĐŁ¬ĽÓČë216mLË®şÍ24gNaOHąĚĚ壬ĹäÖĆ10%NaOHČÜŇş
2Ł®ČôNA±íĘľ°˘·üĽÓµÂÂŢłŁĘýµÄÖµŁ¬ĎÂÁĐ˵·¨ŐýČ·µÄĘÇ
AŁ®2.3g NaÔÚ×ăÁżµÄO2ÖĐÍęČ«ČĽÉŐşÍÓëÔÚżŐĆřÖĐ»şÂý·´Ó¦ÍęČ«Ł¬×ŞŇƵĵç×ÓĘýľůÎŞ0.1NA
BŁ®11.2L Cl2Ëůş¬µÄÔ×ÓĘýÎŞNA
CŁ®»ŻŃ§É϶¨Ňĺ12g ĚĽÖеÄĚĽÔ×ÓĘýÎŞNAµÄĘýÖµ
ˇˇˇˇˇˇˇˇ ˇˇ¨E
DŁ®17g ˇˇŁ®O©UHÖĐËůş¬µç×ÓĘýÎŞ7NA
ˇˇˇˇˇˇˇˇ ˇˇ¨E
1Ł®ÓĂÓŇÍĽ±íĘľµÄһЩÎďÖĘ»ň¸ĹÄîÖ®ĽäµÄ´ÓĘô»ň°üş¬ąŘϵÖв»ŐýČ·µÄĘÇ
|
ˇˇ |
X |
Y |
|
||
|
Ŕý |
Ńő»ŻÎď |
»ŻşĎÎď |
´żľ»Îď |
||
|
A |
±˝ |
·ĽĎăĚţ |
ÓĐ»ú»ŻşĎÎď |
||
|
B |
ČÜŇş |
·Öɢϵ |
»ěşĎÎď |
||
|
C |
Çżµç˝âÖĘ |
µç˝âÖĘ |
»ŻşĎÎď |
||
|
D |
ÖĂ»»·´Ó¦ |
Ńő»Ż»ąÔ·´Ó¦ |
Ŕë×Ó·´Ó¦ |
ąúĽĘѧУÓĹѡ - Á·Ď°˛áÁбí - ĘÔĚâÁбí
şţ±±Ęˇ»ĄÁŞÍřÎĄ·¨şÍ˛»ÁĽĐĹϢľŮ±¨Ć˝Ě¨ | ÍřÉĎÓĐş¦ĐĹϢľŮ±¨×¨Çř | µçĐĹթƾٱ¨×¨Çř | ÉćŔúĘ·ĐéÎŢÖ÷ŇĺÓĐş¦ĐĹϢľŮ±¨×¨Çř | ÉćĆóÇÖȨľŮ±¨×¨Çř
ÎĄ·¨şÍ˛»ÁĽĐĹϢľŮ±¨µç»°Łş027-86699610 ľŮ±¨ÓĘĎ䣺58377363@163.com