
题目列表(包括答案和解析)
4.在200 mL 0.5 mol·L-1 NaOH溶液中,加入一定量SO3,在一定条件下蒸发所得溶液,析出的固体物质只有5.0 g,该固体物质的成分可能是(固体物质均不含结晶水)
A.Na2SO4 B.NaHSO4
C.NaOH和Na2SO4 D.Na2SO4和NaHSO4
3.向50 mL 18 mol/L硫酸中加入足量的铜片并加热,被还原的硫酸的物质的量(n)为
A.n=0.9 mol B.0.45 mol<n<0.9 mol
C.n=0.45 mol D.n<0.45 mol
2.已知98%的浓H2SO4的浓度为18.4 mol/L,则49%的硫酸溶液的浓度为
A.9.2 mol/L B.大于9.2 mol/L
C.小于9.2 mol/L D.不能确定
1.下列四种溶液中,一定存在SO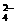 的是
的是
A.向甲溶液中加入BaCl2溶液,产生白色沉淀
B.向乙溶液中加入BaCl2溶液,有白色沉淀,再加入盐酸沉淀不溶解
C.向丙溶液中加入盐酸使之酸化,再加入BaCl2溶液,有白色沉淀产生
D.向丁溶液中加入硝酸酸化,再加入硝酸钡溶液,有白色沉淀产生
22.(8分)C和CaCO3的混合物在空气中加强热后,CaCO3完全分解,C被完全氧化,若生成物中CO2的质量与原混合物的质量相等,求原混合物中C的质量分数。
21.(7分)将CO2通入0.02 mol 氢氧化钠的溶液中,产物在低温低压下蒸干,得到固体物质1.37 g。由此计算通入的CO2在标准状况下的体积是多少L?
20.(12分)(2002年全国高考理综试题)在25℃,101 kPa条件下,将15 L O2通入10 L CO和H2的混合气体中,使其完全燃烧,干燥后,恢复至原来的温度和压强。
(1)若剩余气体的体积是15 L,则原CO和H2的混合气体中,V(CO)= L,V(H2)= L。
(2)若剩余气体的体积为a L,则原CO和H2的混合气体中,V(CO)∶V(H2)= 。
(3)若剩余气体的体积为a L,则a的取值范围是 。
19.(8分)水蒸气通过灼热的煤所产生的混合气,其主要成分是CO、H2,还含有CO2和水蒸气。请用下列装置设计一个实验,以确认上述混合气中含有CO和H2。
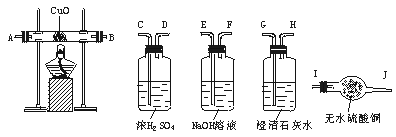
(1)上图所示装置的正确连接顺序是(填各接口的代码字母):
混合气→( )( )接( )( )接( )( )接( )( )接( )( )。
(2)确认混合气体中含有H2的实验现象是 。其理由是 。
18.(14分)将n mol木炭粉和1 mol FeO在反应器中混合,隔绝空气加强热。
(1)可能发生的化学反应有:
①FeO+C===Fe+CO↑
②2FeO+C===2Fe+CO2↑
③FeO+CO===Fe+CO2↑
④
(2)若n<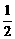 ,充分反应后,反应器中的固体物质是
,气体产物是
。
,充分反应后,反应器中的固体物质是
,气体产物是
。
(3)若n>1,充分反应后,反应器中的固体物质是 ,气体产物是 。
(4)若反应的气体产物是混合物,n的取值范围是 。
(5)若反应的气体产物是混合物,且混合物中CO和CO2的物质的量相等,则n的值为 。
17.某混合气体的质量百分组成为CO占22%、O2占48%、N2占20%、H2占10%,则此混合气体的平均式量为
A.27.32 B.12.5
C.20.17 D.17.95
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com