
题目列表(包括答案和解析)
5.(广东省肇庆一模)将某些化学知识用数轴表示直观形象、简明易记。下列用数轴表示正确的是
A.平衡常数与转化率关系:
B.分散系的分类: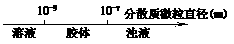

 C.AlCl3和NaOH反应后铝元素的存在形式:
C.AlCl3和NaOH反应后铝元素的存在形式: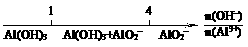
D.Na与O2反应的产物: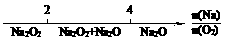
6.(广东省阳江市一模)下列事实不能用勒夏特列原理解释的是
A.打开冰镇啤酒瓶把啤酒倒入玻璃杯,杯中立即泛起大量泡沫
B.加热后的纯碱水洗油污比冷碱水效果好
C.FeCl3滴入沸水中,煮沸片刻得到红褐色胶体
D.镀层破损后,马口铁(镀锡的铁)比白铁(镀锌的铁)更易腐蚀
18.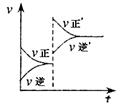 (江门调研)对于达到平衡的可逆反应:X+Y
(江门调研)对于达到平衡的可逆反应:X+Y  W+Z,增大压强,则正、逆反应速率(
W+Z,增大压强,则正、逆反应速率(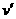 )变化的图象如右图所示,关于X、Y、Z、W物质的聚集状态的说法可能正确的是
)变化的图象如右图所示,关于X、Y、Z、W物质的聚集状态的说法可能正确的是
A.Z、W均匀为气体,X、Y有一种是气体
B.Z、W中有一种是气体,X、Y皆为非气体
C.X、Y、Z皆为气体,W为非气体
D.X、Y均为气体,W、Z中有一种是气体
5. (江门调研)2007
年诺贝尔化学奖德国科学家格哈德 · 埃特尔对有关一氧化碳在金属铂表面的氧化过程的研究,催生了汽车尾气净化装置。净化装置中的催化转化器,可将 CO、NO、NO2
和碳氢化合物等转化为无害的物质,有效降低尾气对环境的危害。下列有关说法不正确的是
(江门调研)2007
年诺贝尔化学奖德国科学家格哈德 · 埃特尔对有关一氧化碳在金属铂表面的氧化过程的研究,催生了汽车尾气净化装置。净化装置中的催化转化器,可将 CO、NO、NO2
和碳氢化合物等转化为无害的物质,有效降低尾气对环境的危害。下列有关说法不正确的是
A.催化转化器中的铂催化剂可加快 CO 氧化
B.铂表面做成蜂窝状更有利于提高催化效果。
C.在铂催化下,NO、NO2 可被 CO 还原成 N2
D.碳氢化合物在铂催化下,被 CO 直接氧化成 CO2和 H2O
4.(江门调研)化学工业在经济发展中的作用举足轻重,下列有关工业生产的叙述中,正确的是
A.硫酸生产中常采用高压条件提高SO2的转化率
B.合成氨中采用及时分离氨气提高反应速率
C.电解精炼铜时,会有金属银比铜先在阴极上析出
D.铝热反应常用于冶炼某些熔点较高的金属
19.(惠州三模)某温度下,将2mo1A和3mo1B充入一密闭容器中,发生反应:aA(g)+B(g) C(g)+D(g),5min 后达到平衡。已知该温度下其平衡常数K=1 ,若温度不变时将容器的体积扩大为原来的10倍,A的转化率不发生变化, 则
C(g)+D(g),5min 后达到平衡。已知该温度下其平衡常数K=1 ,若温度不变时将容器的体积扩大为原来的10倍,A的转化率不发生变化, 则
A.a=1 B.a =2
C.B的转化率为40 % D.B的转化率为60 %
1.(惠州三模)2007 年诺贝尔化学奖得主--德国科学家格哈德·埃特尔对一氧化碳在铂表面氧化过程的研究,催生了汽车尾气净化装置。净化装置中催化转化器可将CO、NO、NO2等转化为无害物质。下列有关说法不正确的是
A.催化转化器中的铂催化剂可加快CO的氧化
B.铂表面做成蜂窝状更有利于提高催化效果
C.在铂催化下,NO、NO2可被CO还原成N2
D.使用铂催化剂,可以提高CO、NO、NO2的转化率
17.(惠州二模)将1mol
H2(g) 和2mol I2(g) 置于某2L密闭容器中,在一定温度下发生反应:H2(g)+
I2(g) 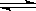 2HI(g)
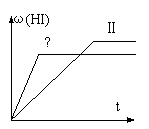
;△H<0,并达到平衡,HI的体积分数ω(HI)随时间变化如图(II)所示。若改变反应条件,ω(HI)的变化曲线如图(Ⅰ)所示,则改变的条件可能是
2HI(g)
;△H<0,并达到平衡,HI的体积分数ω(HI)随时间变化如图(II)所示。若改变反应条件,ω(HI)的变化曲线如图(Ⅰ)所示,则改变的条件可能是
A.恒温恒容条件下,加入适当催化剂 B.恒温条件下,缩小反应容器体积
C.恒容条件下升高温度 D.恒温条件下,扩大反应容器体积
15. (广州市调研)一定条件下,对于可逆反应X(g)+3Y(g)
(广州市调研)一定条件下,对于可逆反应X(g)+3Y(g) 2Z(g),若X、Y、Z的起始浓度分别为c
2Z(g),若X、Y、Z的起始浓度分别为c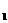 、c
、c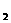 、c
、c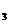 (均不为零),到达平衡时,X、Y、Z的浓度分别为0.1 mol/L、0.3 mol/L、0.08 mol/L,则下列判断正确的是
(均不为零),到达平衡时,X、Y、Z的浓度分别为0.1 mol/L、0.3 mol/L、0.08 mol/L,则下列判断正确的是
A.c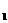 :c
:c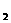 =1:3
=1:3
B.平衡时,Y和Z的生成速率之比为2:3
C.X、Y的转化率相等
D.c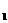 的取值范围为0.04<c
的取值范围为0.04<c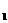 <0.14 mol/L
<0.14 mol/L
16.(广东省韶关市一模)对于平衡体系:aA(g)+bB(g) cC(g)+dD(g);正反应放热,有下列判断,其中正确的是
cC(g)+dD(g);正反应放热,有下列判断,其中正确的是
A.若温度不变,容器体积扩大一倍,此时A的浓度是原来的0.48倍,则a+b大于c+d
B.若从正反应开始,平衡时,A、B的转化率相等,则起始时A、B的物质的量之比为a:b
C.若平衡体系中共有气体m mol,再向其中充入n molB,达到平衡时气体总物质的量为(m+n)mol,则a+b=c+d
D.若a+b=c+d ,则对于体积不变的容器,升高温度,平衡向左移动,容器中气体的压强不变
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com