
题目列表(包括答案和解析)
6.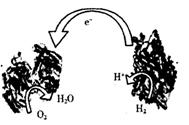 2006年,科学家发明了一种能够给电子设备提供动力的生物燃料电池。该电池的两个涂覆着催化剂酶的电极处于充满空气和少量氢气的玻璃槽中,总反应为:2H2
+O2=2H2O ,由于气体可以混合从而省去了昂贵的燃料隔离膜,其工作原理如图。下列说法不正确的是
2006年,科学家发明了一种能够给电子设备提供动力的生物燃料电池。该电池的两个涂覆着催化剂酶的电极处于充满空气和少量氢气的玻璃槽中,总反应为:2H2
+O2=2H2O ,由于气体可以混合从而省去了昂贵的燃料隔离膜,其工作原理如图。下列说法不正确的是
A. 右边电极为该电池的负极
B. 该电池可以在高温环境下使用
C. 该装置为化学能转变为电能的装置
D. 该电池正极发生的是还原反应
2、(揭阳一模)下列变化中,属于化学变化的是
①橡胶的老化 ②油脂的硬化 ③石油的裂化 ④蛋白质的盐析
A. ①②③④
B. 只有②③
C. 只有①③
D. 只有①②③
18.(汕头二模)用电解质溶液为氢氧化钾水溶液的氢氧燃料电池电解饱和硫酸钠溶液一段时间,假设电解时温度不变且用惰性电极,下列说法不正确的是
A.当电池负极消耗m g气体时,电解池阴极有m g气体生成
B.电解池的阳极反应式为:4OH--4e-=2H2O+O2↑
C.反应后,电池中c(KOH)不变;电解池中溶液pH变大
D.电解后,c(Na2SO4)不变,且溶液中有晶体析出
13.(汕头二模)根据热化学方程式S(s)+O2(g)=SO2(g);△H=-297.23kJ·mol-1,分析下列说法中正确的是
A.S(g)+O2(g)=SO2(g);|△H|>297.23 kJ·mol-1
B.S(g)+O2(g)=SO2(g);|△H|<297.23 kJ·mol-1
C.1molSO2(g)所具有的能量大于1molS(s)与1molO2(g)所具有的能量之和
D.1molSO2(g)所具有的能量小于1molS(s)与1molO2(g)所具有的能量之和
9.(汕头二模)已知同温度下的溶解度:Zn(OH)2>ZnS,MgCO3>Mg(OH)2;就溶解或电离出S2-的能力而言,FeS>H2S>CuS,则下列离子方程式错误的是
A.Mg2+ + 2HCO3- + 2Ca2+ + 4OH- = Mg(OH)2↓+ 2CaCO3↓+ 2H2O
B.Cu2+ + H2S = CuS↓+ 2H+
C.FeS + 2H+ = Fe2+ + H2S↑
D.Zn2+ + S2- + 2H2O = Zn(OH)2↓+ H2S↑
8.(汕头二模)著名丹麦物理学家尼·玻尔(N·Bohr)将他钟爱的金制诺贝尔奖章用王水溶解成“金溶液”:Au + HNO3
+3HCl → AuCl3 +NO +2H2O,AuCl3 +HCl →
HAuCl4 (四氯合金酸)纳粹分子对这种溶液“愚笨得”视而不见、毫无所知。战争结束后,物理学家又根据以下反应,炼出黄金并铸出更加灿烂夺目得奖章:2HAuCl4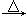 2HCl↑+Cl2↑+Au,表现出伟大科学家对祖国的无比热爱和非凡智慧。尼·玻尔的以上操作中应用的化学原理正确的是
2HCl↑+Cl2↑+Au,表现出伟大科学家对祖国的无比热爱和非凡智慧。尼·玻尔的以上操作中应用的化学原理正确的是
A.王水有很强的氧化性
B.金离子(在配离子[AuCl4]-中)有很强的还原性
C.盐酸有很强的还原性
D.氯气是上述反应中的氧化剂
5.(汕头二模)用惰性电极电解1 L足量KCl的溶液,若通过n mol电子的电量,则溶液的pH与n的关系是(设电解前后溶液的体积不变)
A.pH= lg n B.pH=-lg n C.pH=14+lgn D.pH=lgn-14
4.(汕头二模)下列反应的离子方程式正确的是
①硝酸银与盐酸混合:Ag++HCl=AgCl↓+H+
②碘化亚铁溶液中通入少量Cl2:Cl2+2I-=2Cl-+I2
③石灰石溶于醋酸:CaCO3+2CH3COOH=2CH3COO-+ Ca2++CO2↑+H2O
④铁粉和稀盐酸反应:2Fe+6H+==2Fe3++3H2↑
⑤小苏打溶液中加入少量的石灰水:Ca2+ +2OH-+2HCO3-=CaCO3↓+CO32- +2H2O
⑥次氯酸钙溶液中通入过量二氧化碳:Ca2++2ClO- + CO2 + H2O =CaCO3↓+ 2HClO
⑦过量的石灰水与磷酸二氢钾溶液反应:3Ca2++6OH-+3H2PO4-=Ca3(PO4)2↓+PO43-+6H2O
⑧氯气与水反应Cl2 + H2O = 2H+ + Cl - + ClO-
⑨纯碱溶液中滴加少量盐酸CO32- + H+ = HCO3-
A.①②⑤⑨ B.②③⑤⑨ C.④⑤⑥⑦ D.②③⑧⑨
14.(广州二模)铅蓄电池用途极广,电解液为30% H2SO4溶液,电池的总反应式可表示为:
Pb(s)+PbO2(s)+2H2SO4(aq)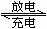 2PbSO4(s)+2H2O(l)
2PbSO4(s)+2H2O(l)
下列有关叙述正确的是
A.放电时电解液的密度不断增大
B.放电时电子从Pb通过导线转移到PbO2
C.充电时Pb极与外电源的负极相连
D.充电时PbO2电极发生还原反应,Pb电极上发生氧化反应
11.(广州二模)下列反应的离子方程式书写正确的是
A.碳酸氢钙溶液与稀硝酸反应:HCO3-+H+=CO2↑+H2O
B.水玻璃中通入过量二氧化碳气体:SiO32-+CO2+H2O=H2SiO3+CO32-
C.浓烧碱溶液中加入铝片:Al+OH-+H2O=AlO2-+H2↑
D.硫酸氢钠溶液与足量氢氧化钡溶液混合:2H++SO42-+Ba2++OH-=BaSO4↓+2H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com