
题目列表(包括答案和解析)
8.下列叙述正确的是 ( )
A.沸点:CH4<SiH4<GeH4<SnH4
B.离子半径:K+>Na+>S2->F-
C.非金属性:F>O>P>S
D.酸性:H2CO3<HBr<CH3COOH<HClO
|
2X(g)+Y(g) Z(g)+W(g);△H<0
Z(g)+W(g);△H<0
若改变某一条件,下列说法正确的是 ( )
A.使用催化剂或缩小容器容积,平衡均不发生移动
B.升温既可以提高反应速率又可以提高X的转化率
C.向容器中加入少量Z,平衡后混合气体中Z的体积分数变小
D.向容器中加入一定量的Y,上述反应的△H不变
7.下列溶液中能大量共存的离子组是 ( )
A.pH=1的溶液:Fe2+、NO3-、S2-、K+
B.含有大量NH4+的溶液:H+、Cu2+、Cl-、NO3-
C.含有大量AlO2-的溶液:Al3+、SO42-、ClO-、Na+
D.含有大量OH-的溶液:HCO3-、MnO4-、Ba2+、CH3COO-
6.下列事实可证明NH3·H2O是弱碱的是 ( )
A.铵盐受热易分解
B.氨水可以使酚酞试液变红
C.0.1mol/L氯化铵溶液的pH约为5
D.氨水能与氯化亚铁溶液反应生成氢氧化亚铁
20、(12分)某研究性学习小组对氨气制法和性质进行如下设计:
⑴下面是该小组同学提出实验室制备氨气的几种方案
A、硝酸铵固体和氢氧化钙固体混合加热
B、加热氯化铵固体
C、氯化铵固体和氢氧化钙固体混合加热
D、将浓硫酸滴入浓氨水中
你认为可行的是 (填字母),
该反应的化学方程式
 ⑵该小组同学把1 mol O2和NH3的混合气体导入密闭容器中,在催化剂的作用下加热,使之充分反应,恢复到常温常压下。若整个容器中的反应随着氧气的量的增加而发生如下两个反应:
⑵该小组同学把1 mol O2和NH3的混合气体导入密闭容器中,在催化剂的作用下加热,使之充分反应,恢复到常温常压下。若整个容器中的反应随着氧气的量的增加而发生如下两个反应:
4NH3 + 5O2 4NO + 6H20;4NO + 3O2 + 2H2O = 4HNO3 设原混合气体中有x mol O2,最后容器中生成y mol HNO3,再向容器中注入100 mL H2O,得到溶液。
①向溶液中滴入酚酞,溶液呈红色,x的取值范围 ,
y = (用x的代数式表示,下同)
②容器中有不溶气体,此气体在空气中变为红棕色,x的取值范围
y =
19.(11分)某研究性学习小组将一定浓度Na2CO3溶液滴入CuSO4溶液中得到蓝色沉淀。
甲同学认为两者反应生成只有CuCO3一种沉淀;
乙同学认为这两者相互促进水解反应,生成Cu(OH)2一种沉淀;
丙同学认为生成CuCO3和Cu(OH)2两种沉淀。(查阅资料知:CuCO3和Cu(OH)2均不带结晶水)
Ⅰ.按照乙同学得理解Na2CO3溶液和CuSO4溶液反应的化学反应方程式为
;
在探究沉淀物成分前,须将沉淀从溶液中分离并净化。具体操作为①过滤②洗涤③干燥。
Ⅱ.请用下图所示装置,选择必要的试剂,定性探究生成物的成分。
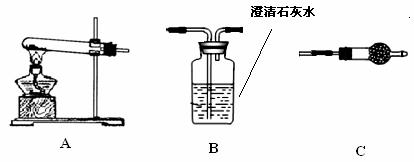


 (1)各装置连接顺序为
。
(1)各装置连接顺序为
。
(2)装置C中装有试剂的名称是
。
(3)能证明生成物中有CuCO3的实验现象是
。
Ⅲ.若CuCO3和Cu(OH)2两者都有,可通过下列所示装置进行定量分析来测定其组成。
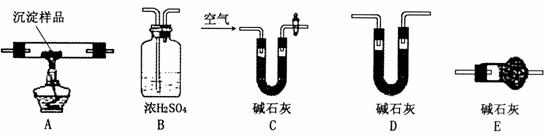

(1)装置C中碱石灰的作用是
,实验开始时和实验结束时都要通人过量的空气其作用分别是
。
(2)若沉淀样品的质量为m克,装置B质量增加了n克,则沉淀中CuCO3的质量分数为
。
18.(12分)聚丙烯酰胺主要用于水的净化处理、纸浆的
加工等。丙烯酰胺是一种不饱和酰胺,是生产聚丙烯酰胺的原料。其结构简式为:
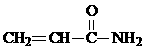
丙烯酰胺可由化合物A(分子式C3H6)经几步反应制得,反应过程如下:
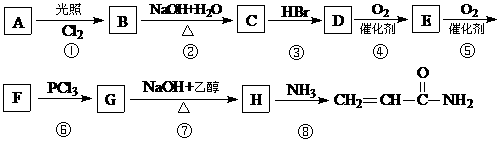
已知:(1)3RCOOH+PCl3 3RCOCl+H3PO3
3RCOCl+H3PO3
(2)RCOCl+NH3 RCONH2+HCl
RCONH2+HCl
试回答下列问题:
(1)关于丙烯酰胺的下列叙述中正确的是:
A.能使酸性KMnO4溶液褪色;
B.能发生加聚反应生成高分子化合物;
C.与α-氨基乙酸互为同系物;
D.能与H2发生加成反应
(2)写出D E的反应方程式:
E的反应方程式:
(3)C D的目的是
;上述反应过程中属于取代反应的是:
。
D的目的是
;上述反应过程中属于取代反应的是:
。
(4)丙烯酰胺有多种同分异构体,同时符合下列要求的同分异构体有多种,试写出2种:
①链状,无碳碳叁键;
②同一个碳原子上不能同时连有-NH2和-OH或双键和-NH2(-OH);
③同一个碳原子上不能连有2个双键。
17. (10分)已知C为淡黄色固体,B、D、E、F标况下均为气体,且水溶液均呈酸性,其中F为单质,G为常见金属,G在CO2中燃烧生成白色和黑色两种固体,K是正盐,A的分子结构和H2O2相似,且均满足8电子结构,以上物质均由短周期元素组成。请完成以下各问题:
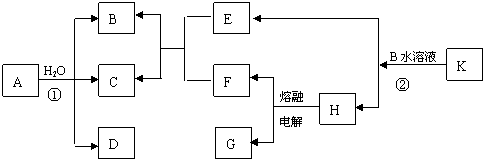
(1)B、D、E、F气体的水溶液中具有漂白能力的是 、 (写化学式)。
(2)用电子式表示E分子的形成过程 。
(3)实验室从H结晶水合物再进一步得到H的无水物应 (填写操作过程)。
(4)写出反应①的化学方程式 ;
D和F反应离子方程式 。
16.(10分)
(1)部分短周期元素的原子半径及常见化合价如下表:
|
元素代号 |
M |
Q |
R |
T |
X |
|
原子半径/nm |
0.160 |
0.143 |
0.099 |
0.074 |
0.102 |
|
常见化合价 |
+2 |
+3 |
-1 |
-2 |
+6,-2 |
① R元素的阴离子结构示意图为________________。
② 探究M和Q两种元素金属性强弱的实验方法是
________________________________
__________________________________________________________________。
③ 工业生产中排放的SO2用饱和Na2XO3溶液吸收可化害为利生产化工原料,该反应的化学方程式为____________________________________________________。若将金属Q的硫酸盐溶液滴加到饱和Na2XO3溶液中,观察到的现象有_________________________________
____________________________________。
(2)几种常见弱酸的电离平衡常数(25℃)如下表。
|
酸 |
电离方程式 |
电离平衡常数K |
|
CH3COOH |
CH3COOH CH3COO-+H+ CH3COO-+H+ |
1.76×10-5 |
|
H2CO3 |
H2CO3 H++HCO3- H++HCO3-HCO3-  H++CO32- H++CO32- |
K1=4.31×10-7 K2=5.61×10-11 |
|
H3PO4 |
H3PO4 H++H2PO4― - H++H2PO4― -H2PO4―  H++HPO42― H++HPO42― HPO42―  H++PO43- H++PO43- |
K1=7.1×10-3 K2=6.3×10-8 K3=4.2×10-13 |
① 若把HCO3-、H2PO4-、HPO42-都看作是酸,则它们的酸性由强到弱的顺序是____________________________________________________。
② 物质的量浓度相同时,Na3PO4溶液的碱性比Na2CO3溶液_______(强 / 弱)。
15.用硫酸铁电化浸出黄铜矿精矿工艺中,精矿在阳极浸出的反应比较复杂,其中有一主要反应:CuFeS2+4Fe3+=Cu2++5Fe2++2S。下列说法正确的是
A.反应中硫元素被氧化,所有铁元素均被还原
B.还原剂是S2-和Cu+,氧化剂是Fe3+
C.氧化产物是S,还原产物是Cu2+和Fe2+
D.当转移1mol电子时,46 g CuFeS2参加反应
第II卷(非选择题,共55分)
14.液态锂离子电池是Li+嵌入化合物的二次电池。正极采用锂化合物LiCoO2,负极采用碳电极,充电后成为锂-碳层间化合物LixC6(0<x≤1),电解质为溶解有锂盐LiPF6、LiAsF6等的有机溶液。下列有关说法错误的是
A.LiCoO2改写为氧化物的形式为:Li2O·Co2O3
B.该电池的电解液使用有机溶剂主要是由于有机溶剂与锂盐有很好的互溶性
C.该电池充电时阴极的反应为:Li++6C+xe-=LixC6+(1-x)Li+
D.放电时电解质中PF6-和AsF6-等离子向负极移动
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com