
题目列表(包括答案和解析)
9.丁烷(化学式C4H10)燃烧时,火苗高且亮,在白天二百米以外也能清晰可见,下列关
于丁烷叙述正确的是( )
①丁烷是由碳、氢两种元素组成的 ②丁烷是由丁烷分子构成的
③丁烷常温下为气态 ④丁烷有2种同分异构体 ⑤丁烷分子只由共价键组成
A.①②③④⑤ B.①②⑤ C.②③④⑤ D.①②④⑤
解析:丁烷是由丁烷分子组成的常温下呈气态的烃。分子中只含有共价键,有正丁
烷和异丁烷两种同分异构体。所以题中说法都正确。
答案:A
8.鉴别甲烷、一氧化碳和氢气三种无色气体的方法,是将它们分别( )
A.先后通入溴水和澄清石灰水
B.点燃后罩上涂有澄清石灰水的烧杯
C.点燃,先后罩上干燥的冷烧杯和涂有澄清石灰水的烧杯
D.点燃后将燃烧产物通入澄清石灰水
解析:三种气体燃烧分别生成CO2和H2O、CO2、H2O,根据三种产物的性质可选
择。A项三者均不反应,不能区别;B项不能区别CH4和CO;D项不能
区别CH4和CO,且燃烧后气体不易收集。
答案:C
7.(2008·潍坊模拟)下列有机物命名正确的是( )
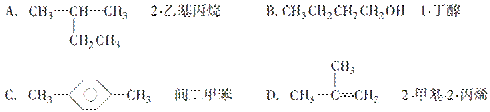
解析:A项物质(烃)的正确命名应为2?甲基丁烷;C项应为对二甲苯;D.项应为2?
甲基丙稀。
答案:B
6.化学家们合成了如图所示的一系列的星烷,如三星烷、四星烷、五星烷等。下列说
法不正确的是( )

A.它们之间互为同系物 B.三星烷的化学式为C9H12
C.三星烷与丙苯互为同分异构体 D.它们的一氯代物均只有两种
解析:三星烷、四星烷、五星烷等所含碳环大小不同,它们不互为同系物,A项说法
不正确;B、C、D三项说法均正确。
答案:A
5. 如图所示:一端封闭的U型管,封闭着的一端有一段CH4和Cl2的混合
如图所示:一端封闭的U型管,封闭着的一端有一段CH4和Cl2的混合
气体,在水平部分有一段气柱,其他两段为液柱,已知液体与气体不
反应,使CH4和Cl2在稍暗的光线下缓慢反应,则中间气柱的长度如何
变化(假设中间气柱未移出U型管的水平部分) ( )
A.变大 B.变小 C.不变 D.难以确定
解析:在U型管封闭的一端,CH4和Cl2的混合气体会发生反应,生成的二氯甲烷、
三氯甲烷、四氯甲烷在常温下都是液体,所以反应后气体的物质的量减少,体积减
小,压强减小,U形管左侧液面就要上升,U型管底部水平气柱的长度增大。
答案:A
4.(江西定南月考)下列化学式及结构式中,从成键情况看不合理的是( )
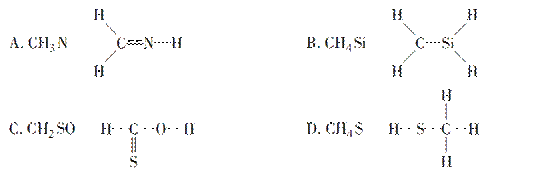
解析:根据元素原子的成键特点,C、H、O、N、S、Si形成共价键的数目分别
为4、1、2、3、2、4,B中C和Si原子均只形成三个共价键,不合理。
答案:B
3.下列说法正确的是( )
A.凡是分子组成相差一个或几个CH2原子团的物质,彼此一定是同系物
B.两种化合物组成元素相同,各元素质量分数也相同,则二者一定是同分异构体
C.相对分子质量相同的几种化合物,互称为同分异构体
D.组成元素的质量分数相同,且相对分子质量也相同的不同化合物,互为同分异
构体
解析:(1)分子组成相差一个或若干个CH2原子团的物质,其分子结构不一定相似,
如CH3-CH=CH2与 ,A说法错误。
,A说法错误。
(2)若两种化合物组成元素相同,各元素的质量分数也相同,则它们的最简式必定
相同。最简式相同的化合物可能是同分异构体,也可能不是同分异构体,如
CH3(CH2)2CH3和CH3CH(CH3)2,CH2=CH2和CH2=CH=CH3;B说法错误。
(3)相对分子质量相同的物质是很多的,如C2H6O(乙醇)与CH2O2(甲酸)具有相同的
相对分子质量,但由于它们的分子组成不同,所以它们不是同分异构体;
C说法错误。
(4)当不同化合物组成元素的质量分数相同,相对分子质量也相同时,其分子式一
定相同,因此这样的不同化合物互为同分异构体。D正确。
答案:D
2.某实验小组对甲、乙、丙、丁四种固体样品的性质进行测试,结果如下表:
|
物质 性质 |
甲 |
乙 |
丙 |
丁 |
|
熔点 |
高 |
低 |
高 |
低 |
|
水溶性 |
溶 |
不溶 |
不溶 |
溶 |
|
高温 |
稳定 |
分解 |
稳定 |
稳定 |
|
导电性 |
导电 |
不导电 |
不导电 |
导电 |
则这四种固体物质中最可能是有机物的是( )
A.甲 B.乙 C.丙 D.丁
解析:据有机物一般不易溶于水、不导电、熔点较低的特点判断乙物质可能
是有机物。
答案:B
1.下列说法中正确的是 ( )
A.有机物都是从有机体分离出来的物质
B.有机物都是共价化合物
C.有机物不一定都不溶于水
D.有机物不具备无机物的性质
解析:有机物不一定要从有机体中分离出来,
如用无机物可制取有机物:CO+2H2催化剂加热、加压CH3OH(甲醇);
有些有机盐 如CH3COONa、CH3COONH4等属于离子化合物;
乙醇,乙酸等有机物能溶于水;无机物与有机物没有绝对界限,
必然有些共同特点与性质。
答案:C
5.(2010·盐城中学期中考题)X、Y、Z、W和N均是由短周期元素组成的五种化合物。已知五种化合物的焰色反应均呈黄色,Y、Z和N均由三种元素组成。请根据题目要求回答下列问题。
(1)固体化合物X为浅黄色粉末,该化合物中含有的化学键有( )
A.离子键 B.极性共价键
C.非极性共价键 D.氢键
(2)写出X与二氧化碳反应的化学方程式_________________________________。
(3)下表为Y与Z实验的部分内容:
|
序号 |
主要实验步骤及实验现象 |
|
① |
在含Y的溶液中,加入稀硫酸溶液,产生浅黄色沉淀和无色有刺激性气味的气体,该气体可使品红溶液褪色。 |
|
② |
在含Z的溶液中,滴加盐酸,开始有白色沉淀,继续滴加盐酸,白色沉淀先增加后消失,然后加入过量的氨水又出现白色沉淀。 |
|
③ |
将实验②最终得到的混合物加热蒸发、灼烧,最终得到白色固体。 |
写出Y与稀硫酸反应的离子方程式______________________________________。
(4)写出含0.1 mol Z的溶液与20 mL 5 mol/L的盐酸反应的离子方程式______。
实验③加热蒸发、灼烧得到的最终产物主要是__________________________。
(5)化合物W和N可以相互转化:W△CO2+H2ON。若有W和N·xH2O的混合物6.52 g,加热到完全反应后,气体产物通过浓H2SO4时浓H2SO4增重1.71 g,剩余气体通过碱石灰时碱石灰增重1.10 g,则混合物中W的质量为________,N·xH2O的化学式为____________。
解析:(1)依据焰色反应现象知,五种化合物都含有钠元素,根据X的颜色知,它是过氧化钠,Na+与O22-之间存在离子键,O22-中氧与氧之间存在非极性共价键。(3)据实验现象:Y+H2SO4―→S↓+SO2↑等,联想高二化学学生实验二“化学反应速率和化学平衡”中化学反应原理:Na2S2O3+H2SO4===Na2SO4+S↓+SO2↑+H2O,可知Y为硫代硫酸钠。又根据“Z+盐酸―→白色沉淀,白色沉淀+盐酸―→溶液,溶液+氨水―→白色沉淀”,由短周期元素组成的物质中只有偏铝酸钠符合题意,Z为偏铝酸钠。灼烧氢氧化铝:2Al(OH)3Al2O3+3H2O。(4)n(HCl)=20×10-3L×5 mol/L=0.1 mol,n(HCl)=n(NaAlO2),NaAlO2+HCl+H2O===Al(OH)3↓+NaCl。(5)根据W、N转化关系,“CO2+H2O”暗示:W为碳酸氢钠,N为碳酸钠。设W、N·xH2O的物质的量分别为a,b。根据混合物质量得:
84 g·mol-1×a+(106+18x)g·mol-1×b=6.52 g①
2NaHCO3Na2CO3+CO2↑+H2O
a a/2 a/2
Na2CO3·xH2ONa2CO3+xH2O
b bx
根据浓硫酸净增质量得:
(a/2+bx)×18 g·mol-1=1.71 g②
根据碱石灰净增质量得:a/2×44 g·mol-1=1.10 g③
联立①②③方程解得:a=0.05 mol,b=0.01 mol,x=7。
m(NaHCO3)=0.05 mol×84 g·mol-1=4.2 g。
答案:(1)AC
(2)2CO2+2Na2O2===2Na2CO3+O2
(3)S2O32-+2H+===S↓+SO2↑+H2O
(4)AlO2-+H++H2O===Al(OH)3↓ Al2O3
(5)4.2 g Na2CO3·7H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com