
3. 情感态度与价值观目标
通过对作为计算机、光通信等高科技关键材料的硅、二氧化硅等无机非金属材料的学习,利用学生对高科技的浓烈兴趣,激发学生对化学的兴趣,通过对我国从古到今,从烧制陶瓷到现代科技成就的介绍,培养学生的民族自豪感。
2. 方法与过程目标
学习从不同的角度出发对常见材料进行分类的方法,能根据同一类别不同物质的性质归纳出该类物质的通性,并能运用通性简单预测其他物质的性质。
1. 知识技能目标
掌握硅、二氧化硅的物理化学性质,粗硅的制法。认识硅、二氧化硅作为无机非金属材料的特性及其用途,了解硅酸盐等无机非金属材料的基本组成、性能、用途。
(二)知识框架
1.半导体材料与单质硅
①单质硅的物理性质:
②硅的化学性质:常温下不活泼,除氟气、氢氟酸和强碱外,一般不与其他物质反应。加热条件下,可与氧气反应。
Si + O2 加热===== SiO2 Si + 2F2 === SiF4 Si + 4HF === SiF4 ↑+ 2H2↑
③硅的工业制法:
工业上,用焦炭在电炉中还原SiO2得到含有少量杂质的粗硅后再提纯。
SiO2 + 2C 高温===== Si + 2CO↑
④硅的主要用途:作半导体材料;制造太阳能电池;制造硅合金等。
2.二氧化硅与光导纤维
①物理性质
②化学性质
SiO2 + 2NaOH == Na2SiO3 + H2O SiO2 + CaO 高温===== CaSiO3
SiO2 + 4HF == SiF4↑ + 2H2O
③二氧化硅的用途:制造电子元器件、光学仪器、精密仪器轴承、光导纤维、石英钟、工艺品、玻璃等。
3.硅酸盐与无机非金属材料
①玻璃、水泥
|
|
玻 璃 |
水 泥 |
|
原 料 |
纯碱(Na2CO3)石灰石(CaCO3)石英(SiO2) |
主要原料 石灰石 粘土 辅助原料 适量的石膏等 |
|
原 理 |
高温下复杂物理化学变化 |
高温下复杂物理化学变化 |
|
化学方程式 |
Na2CO3+SiO2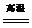 Na2SiO3+CO2 Na2SiO3+CO2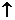 CaCO3+SiO2 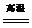 CaSiO3+CO2 CaSiO3+CO2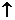 |
|
|
主要成分及特性 |
普通玻璃
钠玻璃(Na2O·CaO·6SiO2)玻璃是非晶体,称为玻璃态物质无固定熔点,在某一温度范围内软化可加工成制品 |
3CaO·SiO2硅酸三钙、2CaO·SiO2硅酸二钙、3CaO·Al2O3铝酸三钙 |
②无机非金属材料:
高温结构陶瓷、生物陶瓷、压电陶瓷等
(一)知识脉络
本节教材以无机非金属材料和硅单质及其化合物的性质两条线索相互交叉而展开,介绍了硅、二氧化硅的性质,硅单质的制法,硅、二氧化硅在计算机及通信等高技术领域的应用,常见的硅酸盐材料玻璃、水泥、陶瓷和新型无机硅酸盐材料的主要成分和用途。与旧教材相比,本教材加大了各种材料在社会日常生活中应用介绍的力度。
3、为了降低开发成本,海水化学资源的利用将走什么道路?我国科学家在此领域取得了哪些成就?
[概括整合] 根据P99的提示,概括整合本节内容。
[作业] P100-101 3、4
[研究性学习课题] P101 5、6
(深圳市深圳中学 罗吉祥 编写)
第四章 元素与材料世界
第一节 硅 无机非金属材料(2课时)
2、溴及其化合物在工业、农业、医药等方面有哪些用途?
1、海水提溴的化学反应原理是什么?工业流程所经历的主要步骤有哪些?
2、碘容易升华的性质有什么重要用途?
[过渡] 氯、溴和碘的单质除了具有以上物理性质之外,在化学性质方面有哪些相同和不同呢?
[活动探究] 我们已经认识了氯气的强氧化性,请用氯水、溴水、碘水、氯化钠溶液、溴化钠溶液、碘化钾溶液,设计实验探究氯、溴、碘三种单质的氧化性强弱。记录实验现象、实验结论或化学方程式。
你的实验方案与实验记录
|
实验内容 |
实验现象 |
实验结论或化学方程式 |
|
|
|
|
<思考>:1、通过实验探究,你认为氯、溴、碘单质的化学性质有什么共同特点?它们的氧化性强弱如何?写出发生反应的离子反应方程式。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com