
科目: 来源: 题型:
【题目】锶元素的原子结构示意图和在元素周期表中显示的信息如图所示:
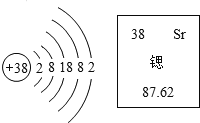
(1)锶属于______元素(填“金属”或“非金属”)。
(2)锶元素的原子序数为___________________。
(3)氧化锶的化学式是_____________,氧化锶与水能发生化合反应生成氢氧化锶并放出大量热,请你写出反应的化学方程式_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在宏观和微观之间建立联系是化学学科特有的思维方式。某反应的微观示意图如下,下列说法正确的是
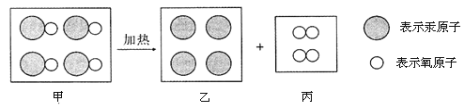
A. 甲、乙、丙三种物质都是由分子构成的
B. 化学反应前后所有元素的化合价都没有发生变化
C. 在化学反应前后,原子的种类和数目都没有发生改变
D. 该反应的化学方程式为:2HgO=2Hg+ 2O2↑
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组通过探究活动学习和理解化学知识.请你一起研究学习,并回答有关问题.
研究主题:水溶液中复分解反应的实质
相关信息:一定体积的溶液中,离子的数目越多,其离子的浓度越大.电导率传感器用于测量溶液的导电性强弱,能反映离子浓度大小.相同温度下同种溶液电导率越大,离子浓度越大.
(1)实验一:恒温条件下,向100mL一定浓度的稀Ba(OH)2溶液中滴加2﹣3滴无色酚酞试液,插入电导率传感器,然后滴加稀硫酸,测得溶液的电导率变化如图中甲曲线所示.
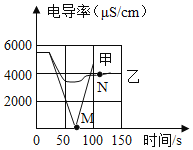
①甲曲线M点时混合液体呈_____色;
②通过对甲曲线的分析,下列说法错误的是_____(填序号).
a.M点前曲线下滑的过程中,H+和OH﹣结合成H2O,Ba2+和SO42﹣结合成BaSO4
b.M点时离子浓度几乎为零
c.M点后溶液电导率逐渐增大,仅由于溶液中H+在逐渐增大
③经测定,M点时消耗稀H2SO4溶液50mL,且过滤后滤液质量为147. 67g。请计算原Ba(OH)2溶液的溶质质量分数_____ (写出计算过程,各种稀溶液的密度都可看成1g·mL-1)。
(2)实验二:恒温条件下,向100mL同浓度的稀Ba(OH)2溶液中滴加2﹣3滴无色酚酞试液,插入电导率传感器,然后滴加稀Na2SO4溶液,测得溶液的电导率变化如上图乙曲线所示.
①通过对乙曲线的分析,下列说法错误的是_____(填序号).
a.开始至完全反应过程中,电导率减小,溶液由红色逐渐变为无色
b.电导率下降到最低点时仍然较大,表明溶液中还存在较多离子
c.整个实验过程中,溶液中Na+数目一直增大
②N点时,溶液中含有的离子是______________(填离子符号).
③通过比较分析,结合已学知识可知,溶液中复分解反应的实质是参与反应的离子,结合生成了沉淀、气体或水,导致其浓度_____(填“增大”或“减小”).
查看答案和解析>>
科目: 来源: 题型:
【题目】某化工厂用废硫酸制备硫酸钾的流程如下,请回答下列问题:
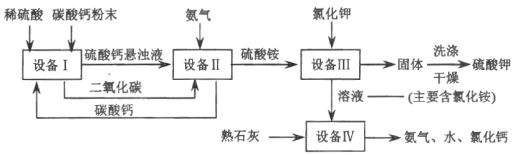
资料:已知20℃时硫酸铵、硫酸钾溶解度如下表:
物质 | 硫酸钾 | 氯化钾 | 氯化铵 | 硫酸铵 |
溶解度/g(20℃) | 11.1 | 34.2 | 37.2 | 75.4 |
(1)“设备I”中将碳酸钙研成粉末的目的是___________。
(2)“设备II”中发生的化学反应方程式是____________,并且______(填“先通氨气”或“先通二氧化碳”)
(3)“设备III”中发生的化学反应方程式是___________。
洗涤从“设备III”中得到的固体时,不用水而是用饱和硫酸钾溶液,其目的是________。
(4)上述流程中可循环使用的物质除水外,还有___________(填写化学式).
查看答案和解析>>
科目: 来源: 题型:
【题目】化学是以实验为基础的科学,实验是科学探究的重要手段。
(1)请结合下列实验装置图回答有关问题。
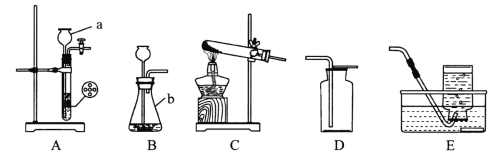
①仪器a的用途是_________,b的名称是_________。
②用高锰酸钾固体制取氧气用于铁丝燃烧实验,最佳装置组合:____________(填字母),写出高锰酸钾反应的化学方程式_______________________。
③实验室制取二氧化碳气体,装置A、B都可用作发生装置,反应的化学方程式是____________,可以通过________操作使装置A中反应很快停止。
(2)实验室将制取纯净、干燥的CO,然后用CO还原Fe2O3并检验气体产物。已知CO发生装置中的反应为:H2C2O4 H2O+CO2↑+CO↑
H2O+CO2↑+CO↑
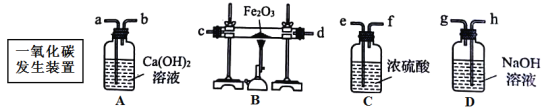
①①A装置中能观察到什么现象___________________
②写出B装置中反应的化学方程式__________________
③要达到实验目的,装置中导管接口从左到右的连接顺序为:一氧化碳发生装置接_____________(填写ABCD装置字母)。
④从环保角度考虑,还需对以上装置进行改进,措施具体为____________
查看答案和解析>>
科目: 来源: 题型:
【题目】下表提供了硝酸钾固体在不同温度时的溶解度。
温度/℃ | 0 | 20 | 40 | 60 | 80 |
溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 |
(1)20℃时,向50 g水中加入20 g硝酸钾,充分溶解后得到__________(选填:饱和或不饱和)溶液,溶液的溶质质量分数为_________(保留一位小数)。
(2)现有60℃时的硝酸钾饱和溶液210 g,若降温至20℃,析出硝酸钾晶体的质量是____,通过________操作可将析出的硝酸钾晶体和溶液分离。
(3)现有80℃时溶质质量分数为30%的硝酸钾溶液,则降温到________(填字母)能得到硝酸钾针状晶体。
a. 0℃-20℃ b. 20℃-40℃ c. 40℃-60℃ d. 60℃-80℃
(4)用100g10%的硝酸钾溶液配制5%的硝酸钾溶液。需要加水_______亳升(水的密度为1.0g·mL-1)
查看答案和解析>>
科目: 来源: 题型:
【题目】写出下列反应的化学方程式,并按要求填空。
(1)将锌粒投入少量硫酸铜溶液中充分反应_________,溶液质量________ (填"变大"、"变小"或"不变")
(2)服用碳酸氢钠以治疗胃酸过多症________, 基本反应类型是________
(3)用稀盐酸除铁锈________
(4)亚硫酸发生氧化反应形成硫酸________,在反应过程中溶液的酸性_______ (填“增强”、 “减弱”或“不变”)
(5)工业上用氨气和二氧化碳在高温高压条件下合成尿素[化学式:CO(NH2)2]__________,尿素属于______氮肥
查看答案和解析>>
科目: 来源: 题型:
【题目】用化学知识可以解释许多生活生产中的问题和现象。
(1)“腌笃鲜”是苏州的一道时令美食。下列制作“腌笃鲜”的食材中,能提供蛋白质的是_________(填字母序号).
a.春笋 b.咸肉
b.咸肉 c.百叶
c.百叶 d.排骨
d.排骨
(2)很多便利店售自热小火锅,其发热的原理是利用了生石灰与水反应放热,写出发生反应的化学方程式______________,反应结束后得到的是_________液。
(3)铝制门窗比较耐腐蚀,主要原因是_______(用文字叙述)。小红还发现新买的家具带有异味,于是在室内放了几个活性炭包以达到除去异味的目的,这是利用了活性炭的______性。
查看答案和解析>>
科目: 来源: 题型:
【题目】用化学符号填空:
(1)地壳中含量最多的金属元素和非金属元素组成的化合物________;
(2)2个氢分子 ________; (3)海水中含量最多的阳离子________;
(4)相对分子质量最小的氧化物_________;
(5)写出硝酸亚铁并标氮元素的化合价________;
查看答案和解析>>
科目: 来源: 题型:
【题目】NSR技术通过BaO和Ba(NO3)2的相互转化实现NOx(氮氧化物)的储存和还原,能有效降低柴油发动机在空气过量条件下的NOx排放。其工作原理如下图所示。下列说法不正确的是
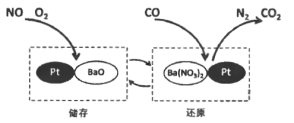
A. 降低NOx排放可以减少空气中酸雨的形成
B. 储存时,吸收NOx (如NO, NO2)的物质是BaO
C. 还原时,发生的反应是: ![]()
D. 若有28 g CO参与反应,则生成CO2的质量为22g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com