
【题目】香豆素类化合物具有芳香气味,是生药中的一类重要的活性成分,主要分布在伞形科、豆科、菊科、芸香科、茄科、瑞香科、兰科等植物中。化合物X是一种香豆素衍生物,可以用作香料,其合成路线如下:
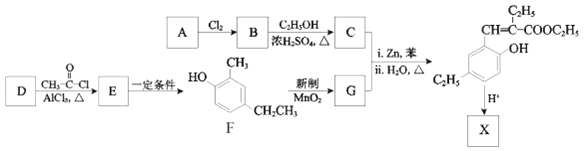
已知:
①RCHO+R’CH2Cl![]() RCH=CHR’
RCH=CHR’
②![]()
![]()
![]()
![]()
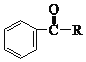
![]()
③![]()
(1)已知A的分子式为C4H8O2,A所含官能团的名称是______。
(2)B生成C反应的化学方程式是______。
(3)G的结构简式是______。
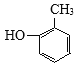
(4)D的分子式是C7H8O,与F互为同系物。则D的结构简式是______。
(5)E可以经多步反应合成F,请写出一条可能的合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件) ______。
(6)X的分子式是C13H14O2,X与足量NaOH溶液共热的化学方程式是______。
【答案】羧基 CH3CH2CHClCOOH+CH3CH2OH![]() CH3CH2CHClCOOCH2CH3+H2O
CH3CH2CHClCOOCH2CH3+H2O 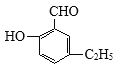
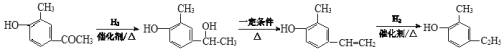
![]() +2NaOH
+2NaOH![]()
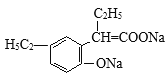 +H2O
+H2O
【解析】
A与Cl2发生取代反应产生B,B发生酯化反应生成C,则C中含有酯基和氯原子,C与G发生信息①的反应,则C为CH3CH2CHClCOOCH2CH3,G为 ,B为CH3CH2CHClCOOH,A为CH3CH2CH2COOH;
,B为CH3CH2CHClCOOH,A为CH3CH2CH2COOH;
F的结构简式是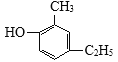 ,D的分子式是C7H8O,与F互为同系物,则D为
,D的分子式是C7H8O,与F互为同系物,则D为 ,根据信息②知,E为
,根据信息②知,E为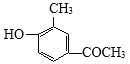 ,F发生氧化反应生成G,
,F发生氧化反应生成G, 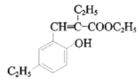 发生水解反应产物再发生酯化反应生成X,X的分子式是C13H14O2,X为
发生水解反应产物再发生酯化反应生成X,X的分子式是C13H14O2,X为![]() 。
。
(5)E为 ,F为
,F为 ,E和H2发生加成反应生成
,E和H2发生加成反应生成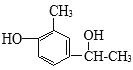 ,
, 发生消去反应生成
发生消去反应生成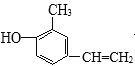 ,
, 与H2发生加成反应生成F,结合题目分析解答。
与H2发生加成反应生成F,结合题目分析解答。
(1)A为CH3CH2CH2COOH,A中官能团名称是羧基;
(2) B为CH3CH2CHClCOOH,C为CH3CH2CHClCOOCH2CH3,B与CH3![]() CH3CH2CHClCOOCH2CH3+H2O;
CH3CH2CHClCOOCH2CH3+H2O;
(3)根据上述分析可知G结构简式为 ;
;
(4)D的分子式是C7H8O,与F互为同系物,F为 ,则D的结构简式是
,则D的结构简式是 ;
;
(5) E为 ,E和H2发生加成反应生成
,E和H2发生加成反应生成 ,
, 发生消去反应生成
发生消去反应生成 ,
, 与H2发生加成反应生成F:
与H2发生加成反应生成F: ,则E生成F的合成路线为:
,则E生成F的合成路线为: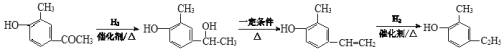 ;
;
(6)X为![]() ,X和NaOH溶液发生水解反应,反应方程式为:
,X和NaOH溶液发生水解反应,反应方程式为:![]() +2NaOH
+2NaOH![]()
 +H2O。
+H2O。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列装置或操作能达到目的的是
A. 装置用于测定生成氢气的速率
装置用于测定生成氢气的速率
B. 装置依据单位时间内颜色变化来比较浓度对反应速率的影响
装置依据单位时间内颜色变化来比较浓度对反应速率的影响
C. 装置依据 U 型管两边液面的高低判断钠和水反应的热效应
装置依据 U 型管两边液面的高低判断钠和水反应的热效应
D. 装置依据出现浑浊的快慢比较温度对反应速率的影响
装置依据出现浑浊的快慢比较温度对反应速率的影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物G的合成路线如下:
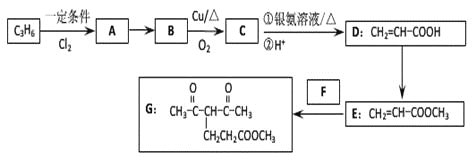
(1)D中含氧官能团的名称为_________,1 molG发生加成反应最多消耗_______mol H2 。
(2)去掉E中含有少量D的试剂和操作是________________________________________;下列有关E的说法正确的是_____________(填字母序号)。
A.可发生氧化反应 | B.催化条件下可发生缩聚反应 |
C.可发生取代反应 | D.是CH2=CHCOOCH2CH3的同系物 |
E.易溶于水
(3)写出A→B的化学反应方程式:________________________________________
(4)反应E + F→G属于下列麦克尔加成反应类型,则F的结构简式为______________________。
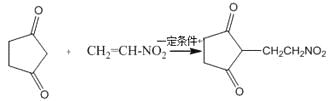
(5)比G少2个氢原子的物质具有下列性质:任写一种该物质的结构简式_________________。
①遇FeCl3溶液显紫色; ②苯环上的一氯取代物只有一种;
③1mol物质最多可消耗2mol Na和1mol NaOH。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:
①H2(g)+![]() O2(g)=H2O(l) ΔH=-285.8 kJ/mol
O2(g)=H2O(l) ΔH=-285.8 kJ/mol
②H2(g)+![]() O2(g)=H2O(g) ΔH=-241.8 kJ/mol
O2(g)=H2O(g) ΔH=-241.8 kJ/mol
③C(s)+![]() O2(g)=CO(g) ΔH=-110.5 kJ/mol
O2(g)=CO(g) ΔH=-110.5 kJ/mol
④C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ/mol
回答下列问题:
(1)上述反应中属于放热反应的是_______。
(2)H2的燃烧热为_______,C的燃烧热为_______。
(3)燃烧10 g H2生成液态水,放出的热量为_______。
(4)CO的燃烧热为_____________,其热化学方程式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2L容器中X、Y、Z三种物质的量随时间的变化曲线如图所示。由图中数据分析,

(1)达到平衡时,Y的浓度为_________________
(2)反应开始至2min,Z的平均反应速率为_____________
(3)该反应的化学方程式为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.过氧化钠的电子式是 Na+[:O:O:]2-Na+
B.原子最外层电子排布式为4s1和5s1 是同一主族元素
C.电负性差值大于 1.7 的化合物一定是离子化合物
D.配合物[Cu(H2O)4]SO4中,中心离子是Cu2+,配位体是H2O,配位数是 4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应mA(g)+nB(g) ![]() pC(g)的速率和平衡的影响图像如下,下列判断正确的是
pC(g)的速率和平衡的影响图像如下,下列判断正确的是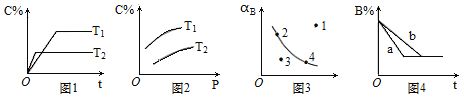
A.由图1可知,T1<T2,该反应正反应为吸热反应
B.由图2可知,该反应m+n﹤p
C.图3中,表示反应速率υ正<υ逆的是点1
D.图4中,若m+n=p,则a曲线一定使用了催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】影响化学反应速率的因素很多,某化学小组用实验的方法进行探究。
Ⅰ.探究一:备选药品:镁片、铝片、0.500 mol·L-1H2SO4、18.4 mol·L-1H2SO4。
甲同学研究的实验报告:
实验步骤 | 现象 | 结论 |
①用砂纸打磨镁片和铝片; ②分别取等体积等浓度的硫酸于两支试管中; ③将镁片和铝片同时投入到试管中。 | 金属的性质越活泼, 反应速率越快 |
(1)甲同学用砂纸打磨镁片和铝片的原因是______________________________;选择H2SO4浓度为________________。
(2) 实验报告中现象为_______________________________________________。
Ⅱ.探究二:实验室经常用Na2S2O3与H2SO4的反应探究化学反应速率的影响因素,利用图1所示装置(夹持装置略去)进行实验,观察到锥形瓶底部有淡黄色浑浊。
(3)请用化学方程式表示出实验原理_________________________________,乙同学在实验过程中对产生的气体进行收集,并在2min内6个时间点对注射器内气体进行读数,记录数据并绘制出图像(如图2)。
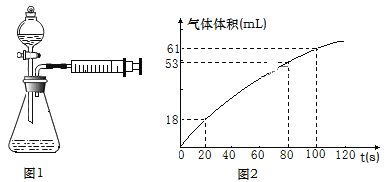
0~20s内反应速率υ1=__________mL·s-1,80~100s内反应速率υ2=__________mL·s-1。不考虑实验测量误差,分析速率差异的主要原因是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,等质量的CO气体和CO2气体相比较,下列叙述中正确的是
A.物质的量之比为7:11B.原子数之比为22:21
C.体积之比为1:1D.密度之比为11:7
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com