
【题目】用0.1000mol/L NaOH溶液滴定分别滴定0.1000mol/L的盐酸和醋酸溶液各25.00 mL。滴定过程中溶液pH随滴入的NaOH溶液体积变化的两条滴定曲线如图所示:
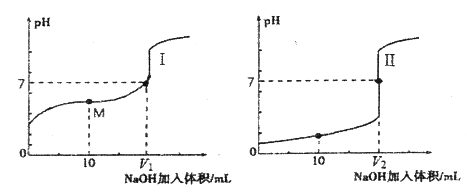
(1)滴定醋酸的曲线是_____________(填“Ⅰ”或“Ⅱ”)。
(2)下列方法中可使溶液中醋酸的电离程度减小的是_____________(填字母序号)。
A. 微热溶液 B. 加少量冰醋酸
C. 加少量醋酸钠固体 D. 加少量碳酸钠固体
(3)V1和V2的关系:V1________V2(填“>”、“=”或“<”)。
(4)M点对应的溶液中,各离子的物质的量浓度由大到小的顺序是_____________。
【答案】I BC < c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
【解析】
(1)醋酸为弱酸,则0.1000mol/L的醋酸溶液pH应大于1,所以滴定醋酸的曲线是I;
(2)A. 电离吸热,微热溶液会促进醋酸的电离,故A错误;
B. 加少量的冰醋酸,醋酸的浓度增大,浓度越大电离程度越小,故B正确;
C. 醋酸钠固体可以电离出醋酸根离子,抑制醋酸的电离,故C正确;
D. 加入碳酸钠固体,碳酸根消耗氢离子,使醋酸的电离平衡右移,促进醋酸的电离,故D错误;
综上所述选BC;
(3)CH3COONa是强碱弱酸盐其水溶液呈碱性,要使混合溶液呈中性,则CH3COOH应该稍微过量,NaCl是强酸强碱盐,其水溶液呈中性,酸碱的物质的量相等,所以V1<V2;
(4)M点混合溶液中溶质为等物质的量浓度的CH3COONa、CH3COOH,pH小于7,溶液呈酸性,则c(H+)>c(OH-),CH3COOH电离程度大于CH3COONa水解程度,结合电荷守恒得c(CH3COO-)>c(Na+),溶液中离子浓度大小顺序是c(CH3COO-)>c(Na+)>c(H+)>c(OH-)。


 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案科目:高中化学 来源: 题型:
【题目】按下列要求作答。
(1)第二周期中,第一电离能介于B和N之间的元素共有_________种。
(2)第四周期中,原子核外电子排布有两个未成对电子的元素有_________种。
(3)硅烷(Si,H2H2n+2)的沸点与其相对分子质量的变化关系如图所示,呈现这种变化关系的原因是___________________________。
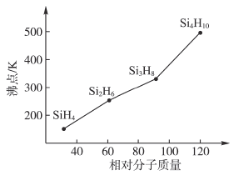
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知标准状况下CH4的体积为4.48L,该气体的物质的量为___________,分子数为___________, 原子数约为___________,质子数为___________,电子数为___________,摩尔质量为___________,质量为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.H2(g)+I2(g)![]() 2HI(g),其他条件不变,缩小反应容器体积,正逆反应速率不变
2HI(g),其他条件不变,缩小反应容器体积,正逆反应速率不变
B.C(s)+H2O(g)![]() H2(g)+CO(g),碳的质量不再改变说明反应已达平衡
H2(g)+CO(g),碳的质量不再改变说明反应已达平衡
C.若压强不再随时间变化能说明反应2A(?)+B(g)![]() 2C(?)已达平衡,则A、C不能同时是气体
2C(?)已达平衡,则A、C不能同时是气体
D.恒压条件下发生反应N2(g)+3H2(g)![]() 2NH3(g),当气体压强不再改变时,反应达到平衡状态
2NH3(g),当气体压强不再改变时,反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂(Li)-空气电池的工作原理如图所示。下列说法不正确的是( )
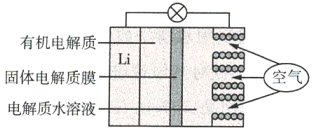
A.金属锂作负极,发生氧化反应
B.Li+通过有机电解质向水溶液处移动
C.正极的电极反应:O2+4e-=2O2-
D.电池总反应:4Li+O2+2H2O=4LiOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A.溴化亚铁溶液中通少量的氯气:2Br-+ Cl2=== 2Cl-+ Br2
B.氢氧化铁悬浊液溶于氢碘酸溶液中:2Fe(OH)3+6H++2I- = 2Fe2++I2+6H2O
C.碳酸氢钙与少量的NaOH溶液反应:Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32-
D.稀硝酸与过量的铁屑反应:3Fe+8H++2NO3-=3Fe3++2NO↑+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一恒容容器中进行如下反应 A(g)+3B(g) ![]() 2C(g),下列情况一定能说明反应已达到平衡的是
2C(g),下列情况一定能说明反应已达到平衡的是
①单位时间内,有1molB反应,同时有2molC生成
②容器内压强不随时间而变化
③单位时间内,有2molC生成,同时有1molA生成
④用 A、B、C表示的该反应的化学反应速率之比为 1∶3∶2
⑤气体的平均摩尔质量不随时间而变化⑥气体的密度不随时间而变化
A.①④⑥B.①②③C.①②⑥D.②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯乙酮常温下为无色晶体或浅黄色油状液体,是山楂、含羞草、紫丁香等香精的调合原料,并广泛用于皂用香精和烟草香精中,可由苯经下述反应制备:
![]() +(CH3CO)2O
+(CH3CO)2O![]()
![]() +CH3COOH
+CH3COOH
NA代表阿伏加德罗常数的值。下列有关说法正确的是
A.气态苯乙酮的密度是气态乙酸密度的2倍
B.1mol苯所含的化学单键数目为12 NA
C.0.5mol乙酸酐中含有的电子数目为27 NA
D.1L2mol/LCH3COOH溶液与足量钠反应生成的气体分子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁在自然界分布广泛,在工业、农业和国防科技中有重要应用。

回答下列问题:
(1)用铁矿石(赤铁矿)冶炼生铁的高炉如图(a)所示。原料中除铁矿石和焦炭外还有________。除去铁矿石中脉石(主要成分为![]() )的化学反应方程式为___________________、_____________________________;高炉排出气体的主要成分有
)的化学反应方程式为___________________、_____________________________;高炉排出气体的主要成分有![]() 、
、![]() 和_________(填化学式)。
和_________(填化学式)。
(2)有人设计出“二步熔融还原法”炼铁工艺,其流程如图(b)所示,其中,还原竖炉相当于高炉的______部分,主要反应的化学方程式为__________________;熔融造气炉相当于高炉的部分。
(3)铁矿石中常含有硫,使高炉气中混有![]() 污染空气,脱
污染空气,脱![]() 的方法是________________________________________________________________。
的方法是________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com