
科目: 来源: 题型:
【题目】如图为某“导电分子线”的结构,下列对该有机分子的说法,正确的是( )
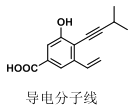
A.最多有 7 个原子共线
B.最多有 13 个碳原子共面
C.可发生加成、酯化、消去反应
D.不考虑立体异构,该分子中共有 7 种化学环境不同的氢
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中能大量共存的是
A. ![]() =1×10-12的溶液:Na+、K+、ClO-、CO32-
=1×10-12的溶液:Na+、K+、ClO-、CO32-
B. 滴入酚酞变红色的溶液:K+、Ca2+、HCO3-、CO32-
C. 能溶解Al(OH)3的溶液:K+、NH4+、NO3—、CH3COO—
D. 0.1mol/LFe(NO3)2溶液:H+、Cu2+、SO42—、Cl—
查看答案和解析>>
科目: 来源: 题型:
【题目】以电石渣[主要成分Ca(0H)2,含Fe203、MgO和Si02等杂质]为原料制备纳米碳酸钙的—种工艺流程如下:
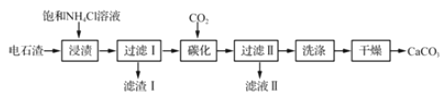
(1)电石渣溶于水形成电石渣浆时会发生反应,生成的物质中除水外还有______。
(2)“浸渍”时,NH4Cl和Ca(0H)2反应的化学方程式为______。
(3)“浸渍”时,一定时间内Ca2+浸取率随温度变化如图所示。Ca2+浸取率随温度升高而上升的原因可能是______。
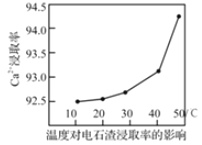
A.温度升高,增大浸取反应速率,从而提高Ca2+浸取率
B.温度升高,溶液黏稠度减小,从而提高Ca2+浸取率
C.温度升高,NH4Cl溶液水解程度减小,从而提高Ca2+浸取率
(4)“碳化”时,-般采用低温工艺,对应的离子方程式为___。
(5)滤液Ⅱ中,可循环利用的溶质的化学式为___。
(6)“洗涤”时,检验是否洗净的方法是:__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】W、M、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数依次增大。W的一种核素在考古时常用来鉴定一些文物的年代;M的氧化物是导致酸雨的主要物质之一。X的某一种单质是大气污染物监测物之一;Y的基态原子核外有6个原子轨道处于半充满状态;Z能形成红色的Z2O和黑色的ZO两种氧化物。
(1)Y3+基态的电子排布式可表示为 。
(2)MX3-的空间构型 (用文字描述)。
(3)M可形成多种氢化物,其中MH3的碱性强于M2H4的原因是 。
(4)根据等电子原理,WX分子的结构式为 。
(5)1 mol WX2中含有的σ键数目为 。
(6)H2X分子中X原子轨道的杂化类型为 。
(7)向Z2+的溶液中加入过量NaOH溶液,可生成Z的配位数为4的配位离子,写出该配位离子的结构式 。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1) 一种铜金合金晶体具有面心立方最密堆积的结构。在晶胞中,Au原子位于顶点,Cu原子位于面心,则该合金中Au原子与Cu原子个数之比为__________,该晶体中原子之间的作用力是_____________。
(2)上述晶体具有储氢功能,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中.若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与CaF2(如图)的结构相似,该晶体储氢后的化学式应为______.

(3)立方BP(磷化硼)的晶胞结构如图所示,晶胞中含B原子数目为_____________ 。
(4)科学家把C60和K掺杂在一起制造出的化合物具有超导性能,其晶胞如图所示。该化合物中的K原子和C60分子的个数比为_____________________ 。


(5)铁有γ、δ、α三种同素异形体,γ晶体晶胞中所含有的铁原子数为________,δ、α两种晶胞中铁原子的配位数之比为__________。

查看答案和解析>>
科目: 来源: 题型:
【题目】Ti、Fe、Cu、Ni为过渡金属元素,在工业生产中有重要的应用.
(1)①常温下Fe(CO)5呈液态,熔点为-20.5℃,沸点为103℃.据此可以判断其晶体为_________晶体,Fe(CO)5中铁的化合价为0,则该物质中含有的化学键类型有______(填字母).
A 离子键 B 极性共价键 C 非极性共价键 D 配位键
②NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4,该配合物中心离子的配位数为________,配体H2O中O原子的杂化方式为________.
③NiO、FeO的晶体结构类型均与氧化钠的相同,Ni2+和Fe2+的离子半径分别为69pm和78pm,则熔点NiO_______FeO(填“<”或“>”).
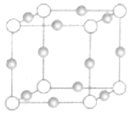
(2)Cu、N两元素形成某种化合物的晶胞结构如图(灰色球表示Cu原子),已知紧邻的白球与灰球之间的距离为acm,该晶胞的密度为________gcm-3.
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃时,浓度均为0.1 mol/L的溶液,其pH如下表所示。有关说法正确的是
序号 | ① | ② | ③ | ④ |
溶液 | NaCl | CH3COONH4 | NaF | NaHCO3 |
pH | 7.0 | 7.0 | 8.1 | 8.4 |
A.酸性强弱:H2CO3>HF
B.①和②中溶质均未水解
C.离子的总浓度:①>③
D.④中:c(HCO3-) + 2c(CO32-) + c(H2CO3)![]() 0.1 mol/L
0.1 mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】正硼酸(H3BO3)是一种片层状结构白色晶体,层内的H3BO3分子通过氢键相连(如下图)。下列有关说法正确的是( )
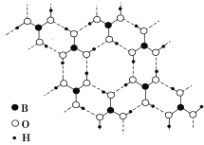
A. 正硼酸晶体属于原子晶体
B. H3BO3分子的稳定性与氢键有关
C. 分子中硼原子最外层为8电子稳定结构
D. 含1 mol H3BO3的晶体中有3 mol氢键
查看答案和解析>>
科目: 来源: 题型:
【题目】已知某可逆反应mA(g)+nB(g)pC(g)在密闭容器中进行,如图表示反应时间 t时、温度 T 和压强P 与反应混合气体中 C 的体积分数(C%)的关系曲线,由曲线分析,下列判断正确的是
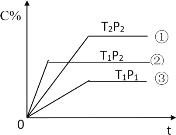
A.T1<T2 P1>P2 m+n<p ΔH>0
B.T1>T2 P1<P2 m+n>p ΔH<0
C.T1<T2 P1>P2 m+n<p ΔH<0
D.T1>T2 P1<P2 m+n>p ΔH>0
查看答案和解析>>
科目: 来源: 题型:
【题目】如图展示了实验室制取少量乙酸乙酯的实验装置。下列关于该反应实验操作及现象的叙述,不正确的是( )
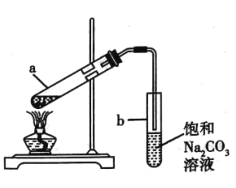
A.向a 试管中先加入乙醇,然后缓缓加入浓硫酸,边加边振荡试管,最后加入乙酸。
B.试管a 中通常加入过量的乙酸,目的在于提高乙醇的转化率
C.试管b 中导气管下端管口不能浸入液面以下,目的在于防止倒吸
D.反应结束后,若观察到试管b 中有少量白色固体析出,该固体可能为NaHCO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com