
科目: 来源: 题型:
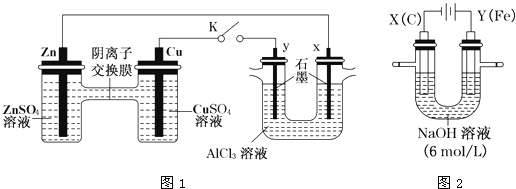
【题目】某课外小组分别用下图所示装置对原电池和电解原理进行实验探究。
请回答:
Ⅰ.用图1所示装置进行第一组实验(K闭合)。
(1)Zn极为________极;实验过程中,SO42-____________(填“从左向右”、“从右向左”或“不”)移动。
(2)反应初期,y极的电极反应现象为________________;检验y极反应产物的方法是________________。
(3)Cu极的电极反应式为____________。
(4)Ⅱ.用图2所示装置进行第二组实验。实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色。电解过程中,X极的电极反应式为__________。
(5)电解过程中,Y极发生的电极反应为Fe-6e-+8OH-=FeO42-+4H2O和4OH--4e-=2H2O+O2↑,若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少________g。
(6)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为:2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2该电池正极发生反应的电极反应式为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】白磷(P4)是一种常见的晶体,可用于制备较纯的磷酸。
(1)白磷是________(填原子或分子)晶体,31 g白磷与足量的氧气完全燃烧释放出745.5 kJ的热量,请写出白磷燃烧的热化学反应方程式:______________________________________。
(2)已知白磷和氯酸溶液可发生如下反应:________P4+___HClO3+___ ______→____HCl+____H3PO4,配平并完成上述反应方程式______________,该反应的氧化剂是___________。
(3)白磷有毒,实验室可采用CuSO4溶液进行处理,其反应为:11P4+60CuSO4+96H2O==20Cu3P+24H3PO4+60H2SO4,该反应的氧化产物是________,若有11 mol P4反应,则有________ mol电子转移。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一压强始终与外界大气压相同的密闭容器中,将适量硫粉和碳粉的混合物与一定量的O2完全反应,恢复到常温,放出504.875kJ的热量,反应后O2有剩余。在标准状况下测得反应后混合气体的体积为44.8L,已知反应后的混合气体中某种气体(A)的质量与物质的量均为另两种气体之和,且C(s)+O2(g) = CO2(g) ΔH=-393.5kJ/mol-1。
(1)投入O2的总体积在标准状况下的体积为____________L。
(2)A为_________。
A.SO2 B.CO2 C.O2 D.无法确定
(3)反应后混合气体的平均摩尔质量为__________________。
(4)混合气体中![]() =_____________。
=_____________。
(5)表示硫燃烧热的热化学方程式为_____________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在压强为0.1MPa条件下,容积为V L的密闭容器中a mol CO与2a mol H2在催化剂作用下反应生成甲醇:CO(g)+2H2(g)![]() CH3OH(g),CO的平衡转化率与温度、压强的关系如下图所示,则:
CH3OH(g),CO的平衡转化率与温度、压强的关系如下图所示,则:
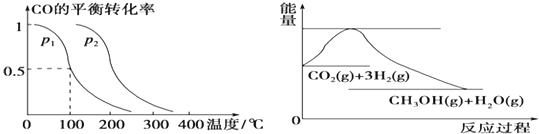
(1)①p1________p2(填“>”、“<”或“=”)。
②在其他条件不变的情况下,向容器中再增加a mol CO与2a mol H2,达到新平衡时,CO的平衡转化率________(填“增大”、“减小”或“不变”)。
③在p1下,100℃时,CO(g)+2H2(g)![]() CH3OH(g)反应的平衡常数为______(用含a、V的代数式表示)。
CH3OH(g)反应的平衡常数为______(用含a、V的代数式表示)。
(2)上图表示CO2与H2反应生成CH3OH和H2O的过程中能量(单位为kJmol﹣1)的变化,该反应的△H_________0,△S_______0。
(3)为探究反应原理,现进行如下实验,在体积为1L的密闭容器中,充入1mol CO2和3mol H2, 一定条件下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),测得CO2(g)和CH3OH(g)的浓度随时间变化的曲线如图所示:
CH3OH(g)+H2O(g),测得CO2(g)和CH3OH(g)的浓度随时间变化的曲线如图所示:
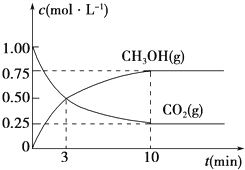
①从反应开始到平衡,CO2的平均反应速率v(CO2)=_________________________。
②下列措施中能使化学平衡向正反应方向移动的是________(填编号)。
A.升高温度
B.将CH3OH(g)及时液化移出
C.选择高效催化剂
D.再充入1mol CH3OH(g)和1mol H2O(g)
查看答案和解析>>
科目: 来源: 题型:
【题目】根据要求回答问题:
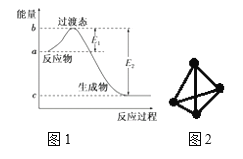
(1)图1是1 mol NO2(g)和1 mol CO(g)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是________(填“增大”、“减小”或“不变”,下同),ΔH的变化是________。
(2)已知CH3OH(l)的燃烧热为726.5kJ·mol-1,CH3OH(l)+ 1/2O2(g)═CO2(g)+2H2(g)△H= -a kJ·mol-1 ,则a________726.5(填“>”、“<”或“=”)。
(3)科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图2所示),与白磷分子相似。已知断裂1mol N-N键吸收193 kJ热量,断裂1 mol N≡N键吸收941 kJ热量,则1 mol N4气体转化为2 mol N2时的△H= ________。
(4)在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-。这两步的能量变化如图:
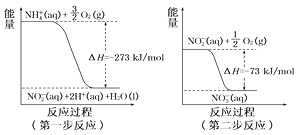
第二步反应是________反应(填“放热”或“吸热”)。1 mol NH4+(aq)全部氧化成NO3-(aq)的热化学方程式是_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】将一定质量的铜与100 mL一定物质的量浓度的硝酸反应,铜完全溶解时产生的NO和NO2混合气体在标准状况下的体积为11.2 L。待产生的气体全部释放后,向溶液中加入100mL 6 mol·L-1的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的物质的量浓度是( )
A.6mol/LB.10mol/LC.11mol/LD.12 mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】Mg-VOCl2电池是一种基于阴离子传导的新型二次电池,其简化装置示意图如下。总反应为Mg+2VOCl2![]() MgCl2+2VOCl,下列说法错误的是
MgCl2+2VOCl,下列说法错误的是

A.采用Mg作电极材料比Li的安全性更高
B.为该电池充电时Mg电极应与电源的正极相连
C.放电时正极反应为VOCl2+e-= VOCl+Cl-
D.放电过程中Cl-穿过复合离子液体向Mg移动
查看答案和解析>>
科目: 来源: 题型:
【题目】W、X、Y和Z为原子序数依次增大的四种短周期元素。X是短周期原子半径最大的元素,Y的最高化合价与最低价相加为0,Z是同周期非金属性最强的元素,W、X、Y三种元素形成的一种化合物结构如图所示。下列叙述正确的是
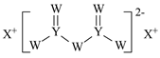
A.X单质的熔点高于Y单质
B.气态氢化物稳定性:Y<Z
C.Z的氧化物对应的水化物为强酸
D.X分别与W、Z形成的二元化合物溶于水显碱性
查看答案和解析>>
科目: 来源: 题型:
【题目】碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活中的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如下:
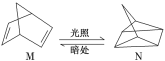
ΔH=+88.6 kJ/mol则M、N相比,较稳定的是_____________。
(2)已知CH3OH(l)的燃烧热ΔH=-238.6 kJ/mol,CH3OH(l)+12O2(g)=CO2(g)+2H2(g) ΔH=-a kJ/mol,则a________238.6(填“>”“<”或“=”)。
(3)将Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:__________________________________。
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s) ΔH=-1 176 kJ/mol,则反应过程中,每转移1 mol电子放出的热量为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】氯酸钾和亚硫酸氢钾溶液能发生氧化还原反应:ClO3-+3HSO3-=3SO42-+Cl-+3H+
已知该反应的速率随c(H+)的增大而加快。下列为用ClO3-在单位时间内物质的量浓度变化表示的该反应v-t图。下列说法中不正确的是
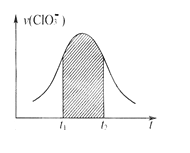
A. 反应开始时速率增大可能是c(H+)所致
B. 纵坐标为v(Cl-)的v-t曲线与图中曲线完全重合
C. 纵坐标为v(H+)的v-t曲线与图中曲线完全重合
D. 后期反应速率下降的主要原因是反应物浓度减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com