
科目: 来源: 题型:
【题目】CH3COOH是常见的弱酸,现有常温下0.1molL-1的CH3COOH溶液。
(1)若温度不变,加水稀释过程中,下列表达式的数据一定变小的是________(填字母序号,下同);若该溶液升高温度,下列表达式的数据增大的是________。
A c(H+)
B c(H+)c(OH-)
C 
D 
(2)某化学兴趣小组装好了如图所示的实验装置,一支胶头滴管盛有盐酸,另一支胶头滴管盛有同体积、同浓度的醋酸。实验时同时完全捏扁a、b胶头滴管的胶头,观察实验现象

①装置A、B中用红墨水而不用水的目的是________________。
②实验刚开始时,发现装置A中的长导管液面上升得比装置B中的要快。则胶头滴管a中盛的是__________。 两装置反应结束时(无固体剩余)。静置后两装置中的长导管或面均有所下降,最终液面高度__________(填“相等”。“A中的高”或“B中的高”).
(3)实验表明,液态时纯硫酸的电离能力强于纯硝酸,纯硫酸的导电性也是显著强于纯水。又知液态纯酸都能像水那样进行自身电离而建立平衡。且在一定温度下都有各自的离子积常数。据此回答:
①5°C时,液态纯硫酸的离子积常数K(H2SO4)_____1×10-14(填“>”“<”或“=”).
②在纯硫酸与纯硝酸的液态混合酸中,存在的阴离子主要是__________。
(4)在某温度下的水溶液中,c(H+)=10xmolL-1,c(OH-)=10ymolL-1,x与y的关系如图所示:

①该温度下,水的离子积为____________。
②该温度下,0.01 molL-1 NaOH溶液中水电离出c(OH-)为____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】将一根较纯铁棒垂直没入水中,由于深水处溶氧量较少,一段时间后发现AB段产生较多铁锈,BC段腐蚀严重,下列关于此现象的说法错误的是
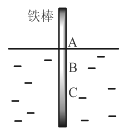
A.铁棒AB段发生反应为O2+ 4e-+ 2H2O = 4OH-
B.腐蚀过程中在铁棒上会产生微电流,且方向是AB段到BC段
C.向水中加入一定量硫酸钾固体后,对铁棒的生锈速率几乎无影响
D.产生这种现象的本质原因是铁棒所处的化学环境不同
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA表示阿伏加德罗常数,下列叙述中正确的是( )
A.常温常压下,11.2L二氧化碳含有的原子数等于1.5NA
B.标准状况下,22.4LCCl4中所含分子数为NA
C.标准状况下,18g水所含原子数为NA
D.常温常压下,48gO2与O3混合物含有的氧原子数为3NA
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期元素A,B,C,D的原子序数依次递增,它们的核电荷数之和32,原子最外层电子数之和为10,A与C同主族,B与D同主族,A,C原子最外层电子数之和等于B原子的次外层电子数。则下列叙述中正确的是
A.D元素处于元素周期表中第3周期第Ⅳ族
B.四种元素的原子半径:![]()
C.B,D的最高价氧化物中,B、D与氧原子均为双键
D.一定条件下,B单质能置换出D单质,C单质能置换出A单质
查看答案和解析>>
科目: 来源: 题型:
【题目】欲除去下列物质中的杂质(括号内为杂质)所用试剂和操作方法都正确的( )
①Cl2(HCl):饱和食盐水、过滤
②CO2(SO2):饱和Na2CO3溶液、洗气
③铁粉(铝粉):NaOH溶液、过滤
④MnO2(KCl):水、溶解后过滤
⑤碳粉(碘单质):CCl4、分液
⑥C2H5OH(H2O):加新制CaO后蒸馏
A.①②③B.③④⑥C.②④⑤D.①④⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】二氧化碳是用途非常广泛的化工基础原料,回答下列问题:
(1)工业上可以用CO2来生产燃料甲醇。
已知:CO2(g) +3H2(g) CH3OH(l) +H2O(l) H= -130kJmol-1
2H2(g)+O2(g)=2H2O(l) H=-572kJmol-1
CH3OH(1)的燃烧热H=________kJmol-1。
(2)在催化剂作用下,CO2和CH4可直接转化为乙酸:CO2(g)+CH4(g)=CH3COOH(g) H>0,在不同温度下乙酸的生成速率变化如图所示。
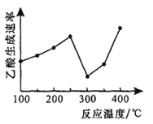
①当温度在250°C-300°C范围时,乙酸的生成速率减慢的主要原因是___________。
②欲使乙酸的平衡产率提高,应采取的措施是__________(任写一条措施即可)。
(3)一定条件下,在密闭容器中发生反应,2CO(g) C(s)+CO2(g).
①下列能说明该反应达到平衡的是______________。
A 容器内混合物的质量不变
B CO和CO2的物质的量之比不再变化
C 混合气体的平均摩尔质量不再变化
D 生成amo1CO2的同时消耗2amol.CO
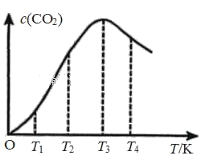
②向某恒容容器中通入一定量的CO发生上述反应,在不同温度下CO2的物质的量浓度c (CO2)随温度的变化如上图所示,则该反应为________(填“放热”或“吸热”)反应。
③向容积可变的某恒压容器中通入amolCO,T°C时反应经过10min达平衡,CO的体积分数为75%。CO的平衡转化率为________。在容积改变的条件下,反应速率可用单位时间内反应物成生成物的物质的量变化来表示,则0-10min内平均反应速率v(CO2)=________。
查看答案和解析>>
科目: 来源: 题型:
【题目】双氧水(H2O2)和水都是极弱电解质,但H2O2溶液显酸性
(1)若把H2O2看成二元弱酸。请写出其在水中的电离方程式:_________。
(2)二氧化锰是实验室制取氧气的催化剂。下列是某同学设计实验探究双氧水分解实验方案:
实验 | 20.0mL双氧水溶液浓度 | 粉状MnO2 | 温度 | 待测数据 |
Ⅰ | 5% | 0.2g | 20°C | |
Ⅱ | 5% | 0.5g | 20°C | |
Ⅲ | 10% | 0.2g | 20°C |

①利用实验Ⅰ和Ⅲ,探究________对化学反应速率的影响,实验待测数据是_________:若在本组实验中现象不明显,可采取的措施是_________________。
(3)加0.1 mol MnO2,粉末于50mL过氧化氢溶液(H2O2,ρ=1.1 gmL-1)中,在标准状况下放出气体的体积和时间的关系如图所示。

①前4min内氧气的产生速率为________mLmin-1
②A、B、C、D各点反应速率由快到慢的顺序为_____________。
③解释反应速率变化的原因_________________。
④计算H2O2初始状态的浓度______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】[化学——选修3:物质结构与性质]
砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。回答下列问题:
(1)写出基态As原子的核外电子排布式________________________。
(2)根据元素周期律,原子半径Ga_____________As,第一电离能Ga____________As。(填“大于”或“小于”)
(3)AsCl3分子的立体构型为____________________,其中As的杂化轨道类型为_________。
(4)GaF3的熔点高于1000℃,GaCl3的熔点为77.9℃,其原因是_____________________。
(5)GaAs的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如图所示。该晶体的类型为________________,Ga与As以________键键合。Ga和As的摩尔质量分别为MGag·mol-1和MAs g·mol-1,原子半径分别为rGapm和rAspm,阿伏伽德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为____________________。

查看答案和解析>>
科目: 来源: 题型:
【题目】能源是人类赖以生存和发展的重要物质基础,常规能源的合理利用和新能源的合理开发是当今社会面临的严峻课题,回答下列问题:
(1)乙醇(C2H5OH)是未来内燃机的首选环保型液体燃料。1 g乙醇完全燃烧生成液态水放出a kJ的热量,则乙醇燃烧的热化学方程式为__________。
(2)由于C3H8(g)= C3H6(g)+H2(g) H=+bkJmol(b>0)的反应中,反应物具有的总能量________(填“大于”“等于”或“小于”)生成物具有的总能量,那么在化学反应时,反应物就需要________(填“放出”或“吸收”)能量才能转化为生成物。
(3)关于用水制取二次能源氢气,以下研究方向不正确的是________。
A 组成水的氢和氧都是可以燃烧的物质,因此可研究在水不分解的情况下,使氢成为二次能源
B 设法将太阳光聚焦,产生高温,使水分解产生氢气
C 寻找高效催化剂,使水分解产生氢气,同时释放能量
D 寻找特殊催化剂,用于开发廉价能源,以分解水制取氢气
(4)已知下列两个热化学方程式,
A 2H2(g)+O2(g)=2H2O(l) H = -571.6kJmol-1
B C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) H= -2220kJmol-1
能表示燃烧热的热化学方程式为________(填A或B)。将标况下22.4L的C3H8和H2混合气体(其中H2的体积分数为1/2),在上述条件下完全燃烧,则放出的热量为________kJ。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com