
题目列表(包括答案和解析)
5.下列物质和苯甲醇互为同系物的是( )
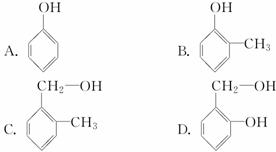
解析:A、B、D均属于酚类,所以不可能和苯甲醇互为同系物。
答案:C
4.(2009·三亚月考)请根据官能团的不同对下列有机物进行分类。

①CH3CH2OH ② ③CH3CH2Br
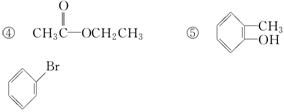
⑥
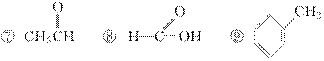
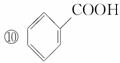
(1)芳香烃:____________;(2)卤代烃:____________;
(3)醇:____________;(4)酚:____________;
(5)醛:____________;(6)酮:____________;
(7)羧酸:____________;(8)酯:____________。
解析:(1)从结构分析,芳香烃必须含有苯环;从元素组成看,芳香烃只含有碳、氢两种元素。符合这两个条件的上述有机化合物只有⑨。
(2)从元素组成来看,卤代烃含有碳、氢、卤素(F、Cl、Br、I)等元素,但不含其他元素。符合该条件的上述有机化合物有③⑥。
(3)(4)中醇、酚都含有羟基,而且元素组成为碳、氢、氧。醇中羟基连接在非苯环碳原子上,如上述有机化合物①;而酚中羟基是直接连接在苯环碳原子上,如上述有机化合物⑤。
(5)(6)中醛、酮都含有羰基,但醛中的羰基(也叫醛基)碳原子上连有氢原子,而酮中羰基(也叫酮基)碳原子上连接的是两个碳原子。因此上述有机化合物⑦为醛,②为酮。
(7)羧酸含有羧基,元素组成只有碳、氢、氧,⑧⑩就是羧酸。
(8)酯含有酯基,元素组成只有碳、氢、氧,上述有机化合物④就是一种酯。
答案:(1)⑨ (2)③⑥ (3)① (4)⑤ (5)⑦ (6)② (7)⑧⑩ (8)④
考点2 烃的衍生物的结构及应用
3.(2008·广东卷改编)从有机化合物的分类来看,下列反应中的X属于( )
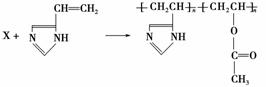
A.醇 B.烷烃 C.烯烃 D.酯
解析:该反应为两种单体的加聚反应,由生成物的结构简式可推知反应物X的结构简式为
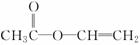
,所以X属于酯类化合物。
答案:D
2.(2009·衡阳八中月考)下列关于羟基和氢氧根的说法中,不正确的是( )
A.羟基比氢氧根少一个电子
B.两者的组成元素相同
C.羟基不带电,氢氧根带一个单位负电荷
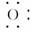
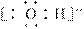 D.羟基比氢氧根稳定
D.羟基比氢氧根稳定
解析:OH-的电子式为 ,-OH的电子式为· ·H,故A、B、C均正确;
由于-OH中的氧原子不是8电子稳定结构,而OH-中的氧原子是8电子稳定结构,故
羟基不如氢氧根稳定,D不正确。
答案:D
1.一些治感冒的药物含有PPA成分,PPA对感冒有比较好的对症疗效,但也有较大的副作用,我国早已禁止使用含有PPA成分的感冒药。PPA是盐酸苯丙醇胺(pheng propanlamine的缩写),从其名称看,其有机成分的分子结构中肯定不含下列中的( )
A.-OH B.-COOH C.-C6H5E D.-NH2
解析:由名称可知不可能含有-COOH。
答案:B
13.茶是我国人民喜爱的饮品。某校化学兴趣小组的同学设计以下实验来定性检验茶叶中含有Ca、Al、Fe三种元素。
查阅部分资料:草酸铵[(NH4)2C2O4]属于弱电解质。草酸钙(CaC2O4)难溶于水。Ca2+、Al3+、Fe3+完全沉淀的pH为Ca(OH)2;pH≥13;Al(OH)3:pH≥5.5;Fe(OH)3:pH≥4.1。
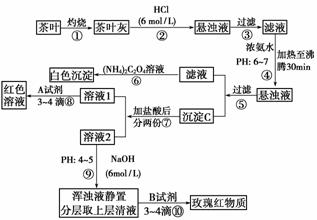
试根据上述过程及信息填空:
(1)步骤②加盐酸的作用是_________________________________________________。
(2)写出检验Ca2+的离子方程式______________________________________________。
(3)写出沉淀C所含主要物质的化学式__________________________________。
(4)写出步骤⑧用A试剂生成红色溶液的离子方程式____________________________。
(5)步骤⑨的作用是_______________________________________________,
猜测步骤⑩的目的是_________________________________________________。
解析:根据实验流程知第②步用盐酸把Fe3+、Al3+、Ca2+从固体物质中浸出。第③步得到含有Ca2+、Al3+、Fe3+的溶液。
第④步控制pH为6-7时,Fe(OH)3、Al(OH)3完全沉淀。第⑥步生成CaC2O4沉淀。第⑧步是利用SCN-检验Fe3+的存在。溶液2控制pH为4-5时,Fe(OH)3完全沉淀,铝元素以Al3+形式存在。
答案:(1)使Ca2+、Al3+、Fe3+溶解在盐酸中
(2)Ca2++(NH4)2C2O4===CaC2O4↓+2NH4+
(3)Fe(OH)3、Al(OH)3
(4)Fe3++3SCN-===Fe(SCN)3
(5)使Fe3+转化为Fe(OH)3沉淀 检验Al3+的存在
12.有A、B、C、D四种强电解质,它们在水中电离时可产生下列离子(每种物质只含一种阴离子且互不重复)
|
阳离子 |
Na+、Ba2+、NH4+ |
|
阴离子 |
CH3COO-、Cl-、OH-、SO42- |
已知:①A、C溶液的pH均大于7,A、B两溶液中水的电离程度相同;
②C溶液和D溶液相遇时只生成白色沉淀,B溶液和C溶液相遇时只生成刺激性气味的气体,A溶液和D溶液混合时无明显现象。
(1)A是__________,B是__________,C是________,D是________;
(2)将等体积、等物质的量浓度的B溶液和C溶液混合,反应后溶液中各种离子浓度由大到小的顺序为:______________。
解析:由A、C两溶液的pH>7,结合离子共存可推知,A、C为Ba(OH)2、CH3COONa中的一种,又由A、B溶液中水的电离程度相同,知A、B水解程度相近,即水解形成的弱酸或弱碱的电离程度相近,进而推知A、B为CH3COONa、NH4Cl中的一种,再结合C溶液和D溶液相遇时只产生白色沉淀、B溶液和C溶液相遇时只产生刺激性气味的气体、A溶液和D溶液混合时无明显现象,推出A为CH3COONa,B为NH4Cl,C为Ba(OH)2,D为Na2SO4。当B、C混合时,发生反应NH4++OH-===NH3↑+H2O,故等体积等物质的量浓度的NH4Cl与Ba(OH)2混合时,各离子浓度由大到小的顺序为:c(OH-)>c(Ba2+)=c(Cl-)>c(NH4+)>c(H+)。
答案:(1)CH3COONa NH4Cl Ba(OH)2 Na2SO4
(2)c(OH-)>c(Ba2+)=c(Cl-)>c(NH4+)>c(H+)
11.有一无色气体(可能由O2、N2、CO2、HCl、NH3、H2、NO、NO2中的一种或几种组成)如图所示,通过洗气瓶,发现气体减少一部分体积,通过干燥管后气体呈红棕色,再将该气体适量地通入盛满水倒立于水槽的试管内,发现倒立试管里水位下降后又缓慢上升,最后试管内仍为一满试管液体。由此判断:

(1)干燥管内固体是________(化学式)。
(2)原气体中一定有________。
(3)原气体中一定没有________。
(4)从浓硫酸洗气瓶出来的气体为________,其体积比为________。
解析:因为该气体无色,故原气体中一定没有NO2,通过浓硫酸洗气瓶,发现气体减少一部分体积,说明有能溶于硫酸的气体即NH3,则原气体中一定没有HCl;通过干燥管后气体呈红棕色,说明原气体中有NO,则原气体中一定没有O2,而通过干燥管时又有O2生成把NO氧化为NO2,故干燥管内固体应是Na2O2,则原气体中还一定有CO2。再将该气体适量地通入盛满水倒立于水槽的试管内,发现倒立试管里水位下降后又缓慢上升,最后试管内仍为一满试管液体。说明气体都全部溶于水了,则原气体中一定也没有H2和N2。由2Na2O2+2CO2===2Na2CO3+O2及4NO+3O2+2H2O===4HNO3,可知6CO2-3O2-4NO,故CO2与NO体积比为3∶2。
答案:(1)Na2O2 (2)NH3、CO2、NO (3)O2、HCl、NO2、H2、N2 (4)CO2与NO 体积比为3∶2
10. (2008·宿迁调研)某研究性学习小组在整理实验室化学试剂时,发现一盛有无色溶液的试剂瓶,标签破损,如图。某同学根据中学化学知识,对该试剂可能是什么物质的溶液进行了如下猜想和验证,选择你认为错误(包括猜想物质的化学式、检验需要的试剂、操作、现象及结论)的选项( )
(2008·宿迁调研)某研究性学习小组在整理实验室化学试剂时,发现一盛有无色溶液的试剂瓶,标签破损,如图。某同学根据中学化学知识,对该试剂可能是什么物质的溶液进行了如下猜想和验证,选择你认为错误(包括猜想物质的化学式、检验需要的试剂、操作、现象及结论)的选项( )
|
选项 |
猜想物质 的化学式 |
检验需要 的试剂 |
操作、现象及结论 |
|
A |
Na2SO4 |
稀盐酸、氯化钡溶液 |
取少量该溶液于试管中,滴入稀盐酸,若无明显现象,再滴入氯化钡溶液,如果产生白色沉淀,则原溶液是Na2SO4溶液 |
|
B |
Na2CO3 |
稀盐酸、澄清的石灰水 |
取少量该溶液于试管中,滴入稀盐酸,如果产生的无色气体能使澄清的石灰水变浑浊,则原溶液一定是Na2CO3溶液 |
|
C |
Na2SO3 |
稀盐酸、澄清的石灰水、品红溶液 |
取少量该溶液于试管中,滴入稀盐酸,如果产生的无色气体既能使澄清的石灰水变浑浊,还能使品红溶液褪色,则原溶液是Na2SO3溶液 |
|
D |
Na2SiO3 |
过量稀盐酸 |
取少量该溶液于试管中,滴入稀盐酸,产生白色胶状沉淀,盐酸过量时沉淀不溶解,则原溶液是Na2SiO3溶液 |
解析:B项的猜想和结论不相符,SO2也可使澄清的石灰水变浑浊。
答案:B
9.(2010·咸阳模拟)提纯含有少量硝酸钡杂质的硝酸钾溶液,可以使用的方法为( )
A.加入过量碳酸钠溶液,过滤,除去沉淀,溶液中补加适量硝酸
B.加入过量硫酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸
C.加入过量硫酸钠溶液,过滤,除去沉淀,溶液中补加适量硝酸
D.加入过量碳酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸
 解析:此题的主要目的是:既除去原混合溶液中的Ba2+,但又不能引入新的杂质(如Na+或SO42-)。解题思路如下:
解析:此题的主要目的是:既除去原混合溶液中的Ba2+,但又不能引入新的杂质(如Na+或SO42-)。解题思路如下:
答案:D
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com