
ĢāÄæĮŠ±ķ(°üĄØ“š°øŗĶ½āĪö)
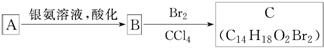
15£®(2010”¤ĮijĒ)ÓŠ»śĪļAĪŖÜŌĄņĻćŠĶĻćĮĻ”£
 ””
””
(1)A·Ö×ÓÖŠŗ¬Ńõ¹ŁÄÜĶŵÄĆū³ĘŹĒ________________________________________________________________________”£
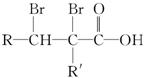
(2)CµÄ·Ö×Ó½į¹¹æɱķŹ¾ĪŖ(ĘäÖŠRŗĶR”ä“ś±ķ²»Ķ¬µÄĢž»ł)£ŗ
 ””
””
AµÄ»ÆѧŹ½ŹĒ________£¬AæÉŅŌ·¢ÉśµÄ·“Ó¦ŹĒ________(ĢīŠ“ŠņŗÅ×ÖÄø)”£
a£®»¹Ō·“Ó¦”””””” b.ĻūČ„·“Ó¦”””””””” c.õ„»Æ·“Ó¦”””””””” d.Ė®½ā·“Ó¦
(3)ŅŃÖŖŗ¬ÓŠĢž»łRµÄÓŠ»śĪļR-OHÓėÅØäåĖ®·“Ó¦²śÉś°×É«³Įµķ£¬Ōņŗ¬ÓŠĢž»łR”äµÄÓŠ»śĪļR”ä-OHµÄĄą±šŹōÓŚ______________”£
(4)A·Ö×Ó½į¹¹ÖŠÖ»ÓŠŅ»øö¼×»ł£¬AµÄ½į¹¹¼ņŹ½ŹĒ________________”£
(5)ŌŚÅØĮņĖį“ęŌŚĻĀ£¬BÓėŅŅ“¼¹²ČČÉś³É»ÆŗĻĪļC16H22O2µÄ»Æѧ·½³ĢŹ½ŹĒ________________________________________________________________________”£
(6)ŌŚAµÄ¶ąÖÖĶ¬·ÖŅģ¹¹ĢåÖŠ£¬·Ö×Ó½į¹¹ÖŠ³żĢž»łR”äŗ¬ÓŠČżøö¼×»łĶā£¬ĘäÓą²æ·Ö¾łÓėAĻąĶ¬µÄÓŠ________ÖÖ”£
½āĪö£ŗ±¾Ģā×ŪŗĻ漲铼”¢Č©”¢ōČĖį¼°õ„Ö®¼äµÄ×Ŗ»Æ¹ŲĻµ”£ÓÉ×Ŗ»Æ¹ŲĻµæÉŅŌ擳öAÄÜ·¢ÉśŅų¾µ·“Ó¦£¬ĖµĆ÷ŗ¬ÓŠČ©»ł£¬ŌŁøł¾ŻŌ×ÓŹŲŗć£¬ÓÉCµÄ·Ö×ÓŹ½ŗĶ½į¹¹Ź½æÉŅŌĶĘ³öAµÄ»ÆѧŹ½ĪŖC14H18O£¬ŅņĘäŗ¬Č©»ł£¬ĒŅÉś³ÉµÄBÄÜÓėBr2·¢Éś¼Ó³É·“Ó¦£¬ĖµĆ÷»¹ŗ¬ÓŠĢ¼Ģ¼Ė«¼ü£¬Ņņ“ĖæÉŅŌ·¢Éś»¹Ō·“Ó¦”£ĮŖĻė±½·ÓÄÜÓėÅØäåĖ®·“Ó¦²śÉś°×É«³Įµķ£¬ČēR”ä-OHÓ¦ĪŖ“¼Ąą(ŅņRŗĶR”äĪŖ²»Ķ¬µÄĢž»ł)”£ČōA·Ö×ÓÖ»ŗ¬ÓŠŅ»øö¼×»ł£¬ŌņAµÄ½į¹¹¼ņŹ½ĪŖ
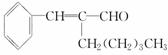 ””
””
£»”” £»Ėį»ÆŗóµÄBĪŖ
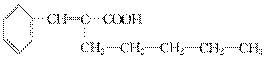 ””
””
£¬ĖüÓėŅŅ“¼¹²ČČÓ¦øĆ·¢Éśõ„»Æ·“Ó¦£¬·½³Ģ
 ””
””
Ź½¼ū“š°ø”£
ŌŁøł¾ŻĢāÉčŅŖĒó£¬æÉŠ“³öAµÄĶ¬·ÖŅģ¹¹Ģå£ŗ
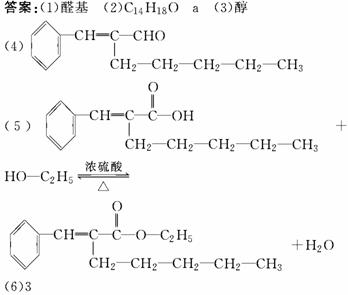 ””
””
14£®±½¼×Č©ŌŚŅ½Ņ©”¢Č¾ĮĻ”¢ĻćĮĻµČŠŠŅµÓŠ×Źć·ŗµÄÓ¦ÓĆ”£ŹµŃéŹŅĶعżČēĻĀĶ¼ĖłŹ¾µÄĮ÷³ĢÓɼױ½Ńõ»ÆÖʱø±½¼×Č©”£
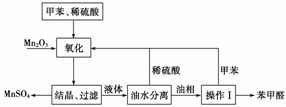
ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)Mn2O3Ńõ»Æ¼×±½µÄ·“Ó¦ŠčŅŖ²»¶Ļ½Į°č£¬½Į°čµÄ×÷ÓĆŹĒ________________________________________________________________________”£
(2)¼×±½¾Ńõ»ÆŗóµĆµ½µÄ»ģŗĻĪļĶعż½į¾§”¢¹żĀĖ½ųŠŠ·ÖĄė”£øĆ¹ż³ĢÖŠŠč½«»ģŗĻĪļĄäČ“£¬ĘäÄæµÄŹĒ
________________________________________________________________________ӣ
(3)ŹµŃé¹ż³ĢÖŠ£¬æÉŃ»·Ź¹ÓƵÄĪļÖŹ·Ö±šĪŖ__________”¢______________”£
(4)ŹµŃéÖŠ·ÖĄė¼×±½ŗĶ±½¼×Č©²ÉÓĆµÄ²Ł×÷¢ńŹĒ________£¬
ĘäŌĄķŹĒ____________________________________________________________________”£
(5)ŹµŃéÖŠ·¢ĻÖ£¬·“Ó¦Ź±¼ä²»Ķ¬±½¼×Č©µÄ²śĀŹŅ²²»Ķ¬(Źż¾Ż¼ūĻĀ±ķ)”£
|
·“Ó¦Ź±¼ä/h |
1 |
2 |
3 |
4 |
5 |
|
±½¼×Č©²śĀŹ/% |
76.0 |
87.5 |
83.6 |
72.5 |
64.8 |
Ēė½įŗĻ±½¼×Č©µÄ½į¹¹£¬·ÖĪöµ±·“Ó¦Ź±¼ä¹ż³¤Ź±£¬±½¼×Č©²śĀŹĻĀ½µµÄŌŅņ________________________________________________________________________”£
½āĪö£ŗ±¾ĢāŅŌŅ½Ņ©”¢Č¾ĮĻ”¢ĻćĮĻµČŠŠŅµ¹ć·ŗÓ¦ÓƵı½¼×Č©µÄÖʱøĪŖ±³¾°æ¼²éĮĖ½į¾§ŗĶÕōĮóĮ½ÖÖĪļÖŹ·ÖĄėµÄ»ł±¾·½·Ø£¬¼Čæ¼²éĮĖŹµŃéÄÜĮ¦ŗĶ·ÖĪöĘĄ¼ŪÄÜĮ¦£¬ÓÖæ¼²éĢž¼°ĢžµÄŃÜÉśĪļµÄĻą»„×Ŗ»Æ¼°Č©»ł¹ŁÄÜĶŵĊŌÖŹ”£
(1)½Į°čæÉŅŌŹ¹Mn2O3Óė¼×±½³ä·Ö½Ó“„£¬¼Óæģ·“Ó¦ĖŁĀŹ£»
(2)“ÓĮ÷³ĢĶ¼æÉŅŌ擳ö”°½į¾§¹żĀĖ”±æÉµĆ¾§ĢåMnSO4£¬Ņņ“Ė£¬½«»ģŗĻĪļĄäČ“µÄÄæµÄŅ»¶ØŹĒ½µµĶMnSO4µÄČܽā¶ČÓŠĄūÓŚMnSO4µÄĪö³ö”£
(3)“ÓĮ÷³ĢĶ¼æÉÖ±½Ó擳ö¼×±½æÉŃ»·Ź¹ÓĆ£¬¶ųĻ”H2SO4ŌŚ¼×±½µÄŃõ»Æ¹ż³ĢÖŠ½öĘš½éÖŹ×÷ÓĆ£¬ÓĶĖ®·ÖĄėŗóŅ²æÉŃ»·Ź¹ÓĆ”£
(4)øł¾ŻÖʱøŌĄķ£¬ÓĶ²ćŗ¬ÓŠµÄĪļÖŹĪŖ±½¼×Č©ŗĶĪ“±»Ńõ»ÆµÄ¼×±½£¬¶ųÕāĮ½ÕߏĒ»„ČÜĪļ£¬Ö»ÄÜĄūÓĆĖüĆĒµÄ·Šµć²»Ķ¬£¬ĄūÓĆÕōĮó(»ņ·ÖĮó)µÄ·½·Ø·ÖĄė”£
(5)“ÓĖłøųŹż¾Żæ“£¬Ėꏱ¼äµÄŃÓ³¤£¬±½¼×Č©µÄ²śĀŹ½µµĶ£¬øł¾Ż±½¼×Č©ÖŠĖłŗ¬Č©»łŅ×±»Ńõ»Æ£¬æÉ·ÖĪöĘäŌŅņæĻ¶ØŹĒ±½¼×Č©±»Ńõ»Æµ¼ÖĀ”£
“š°ø£ŗ(1)Ź¹·“Ó¦Īļ³ä·Ö½Ó“„£¬Ōö“ó·“Ó¦ĖŁĀŹ
(2)½µµĶMnSO4µÄČܽā¶Č””(3)Ļ”ĮņĖį””¼×±½
(4)ÕōĮ󔔥ūÓĆ¼×±½ŗĶ±½¼×Č©µÄ·Šµć²īŅģŹ¹¶žÕß·ÖĄė
(5)²æ·Ö±½¼×Č©±»Ńõ»Æ³É±½¼×Ėį
13£®(2009”¤°²ĒģŅ»ÖŠŌĀæ¼)ÓŠ»śĪļA”¢B”¢C¶¼ŹĒÖŲŅŖµÄ»Æ¹¤ŌĮĻ£¬A-DÖ®¼äÓŠČēĶ¼ĖłŹ¾µÄ×Ŗ»Æ¹ŲĻµ”£
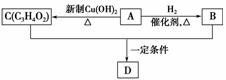
(1)AÖŠ¹ŁÄÜĶŵÄĆū³ĘĪŖ________________________________________________________________________”£
(2)A”śCµÄŹµŃéĻÖĻóĪŖ__________________________£¬
·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ________________________________________________________________________”£
(3)l molAgnÓė2 mol H2£¬¼Ó³ÉµĆ²śĪļB”£Ķź³ÉB+C”śDµÄ»Æѧ·½³ĢŹ½£ŗ__________________________________£¬
·“Ó¦ĄąŠĶĪŖ______________________”£
½āĪö£ŗA“ß»ÆŃõ»ÆŗóµĆC(C3H4O2)£¬æÉÖŖC·Ö×ÓÖŠŗ¬-COOH£¬²Š»łĪŖ”°C2H3”±£¬¹¹³ÉCHCH2£¬¹ŹCĪŖCH2CHCOOH£¬ÓÉ“ĖĶĘÖŖAĪŖCH2CHCHO£¬BĪŖCH3CH2CH2OH£¬ĪŖCH2CHCOOCH2CH2CH3”£
“š°ø£ŗ(1)Č©»ł”¢Ģ¼Ģ¼Ė«¼ü
(2)²śÉś×©ŗģÉ«³Įµķ””CH2CHCHO+2Cu(OH)2CH2CHCOOH+Cu2O”ż+2H2O
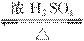 ””
””
(3)CH2=CHCOOH+CH3CH2CH2OH”””””””””””””” CH2CHCOOCH2CH2CH3+H2O””Č”
“ś·“Ó¦(õ„»Æ·“Ó¦)
12£®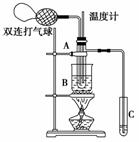 (2009”¤Õż¶Ø֊ѧŌĀæ¼)ŅŅČ©ŌŚ“߻ƼĮ“ęŌŚµÄĢõ¼žĻĀ£¬æÉŅŌ±»æÕĘųŃõ
(2009”¤Õż¶Ø֊ѧŌĀæ¼)ŅŅČ©ŌŚ“߻ƼĮ“ęŌŚµÄĢõ¼žĻĀ£¬æÉŅŌ±»æÕĘųŃõ
»Æ³ÉŅŅĖį”£ŅĄ¾Ż“ĖŌĄķÉč¼ĘŹµŃéÖĘµĆ²¢ŌŚŹŌ¹ÜCÖŠŹÕ¼Æµ½ÉŁĮæŅŅ
ĖįČÜŅŗ(ČēĶ¼ĖłŹ¾£¬ŹŌ¹ÜA֊װӊ40%µÄŅŅČ©Ė®ČÜŅŗ”¢Ķ·Ū£¬ŹŌ¹Ü
C֊װӊŹŹĮæÕōĮóĖ®£»ÉÕ±B֊װӊijŅŗĢå)”£ŅŃÖŖŌŚ60”ę-80”ę
Ź±£¬ÓĆĖ«Į¬“ņĘųĒņ¹ÄČėæÕĘų¼“æÉ·¢ÉśŅŅČ©µÄŃõ»Æ·“Ó¦£¬Į¬Šų¹ÄČėŹ®
¼ø“Ī£¬·“Ó¦»ł±¾ĶźČ«”£ÓŠ¹ŲĪļÖŹµÄ·ŠµćČēĻĀ£ŗ
|
ĪļÖŹ |
ŅŅČ© |
ŅŅĖį |
øŹÓĶ |
Ė® |
|
·Šµć/”ę |
20.8 |
117.9 |
290 |
100 |
ĒėĶź³ÉĻĀĮŠĪŹĢā£ŗ
(1)ŹŌ¹ÜAÄŚŌŚ60”ę-80”ꏱ·¢ÉśµÄÖ÷ŅŖ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ(×¢Ć÷·“Ó¦Ģõ¼ž)________”£
(2)ČēĶ¼ĖłŹ¾£¬ŌŚŹµŃéµÄ²»Ķ¬½×¶Ī£¬ŠčŅŖµ÷ÕūĪĀ¶Č¼ĘŌŚŹŌ¹ÜAÄŚµÄĪ»ÖĆ£¬ŌŚŹµŃéæŖŹ¼Ź±ĪĀ¶Č¼ĘĖ®ŅųĒņµÄĪ»ÖĆÓ¦ŌŚ________£»µ±ŹŌ¹ÜAÄŚÖ÷ŅŖ·“Ó¦Ķź³Éŗó£¬ĪĀ¶Č¼ĘĖ®ŅųĒņµÄĪ»ÖĆÓ¦ŌŚ________£¬ÄæµÄŹĒ________________________”£
(3)ÉÕ±BµÄ×÷ÓĆŹĒ________________________________________________________________________£»
ÉÕ±BÄŚŹ¢×°µÄŅŗĢåæÉŅŌŹĒ________(Ń”Ģī”°øŹÓĶ”±»ņ”°Ė®”±)”£
(4)ČōĻė¼ģŃéŹŌ¹ÜCÖŠŹĒ·ńŗ¬ÓŠ²śĪļŅŅĖį£¬ĒėÄćŌŚĖłĢį¹©µÄŅ©Ę·ÖŠ½ųŠŠŃ”Ōń£¬Éč¼ĘŅ»øö¼ņ±ćµÄŹµŃé·½°ø”£
ĖłĢį¹©µÄŅ©Ę·ÓŠ£ŗpHŹŌÖ½£¬ŗģÉ«µÄŹÆČļŹŌÖ½£¬°×É«µÄ“×ĖįĒ¦ŹŌÖ½£¬Ģ¼ĖįĒāÄĘ·ŪÄ©”£ŹµŃéŅĒĘ÷ČĪŃ””£
øĆ·½°øĪŖ(¼ņŹö²Ł×÷¹ż³Ģ)£ŗ________________________________________________________________________”£
½āĪö£ŗ×Ū¹ŪČ«Ģā£¬æÉÖŖ±¾ŹµŃéµÄŌĄķŹĒ£ŗÓĆĖ«Į¬“ņĘųĒņ¹ÄČėæÕĘų£¬Ź¹æÕĘųÖŠµÄŃõĘųÓėAÖŠµÄŅŅČ©ŌŚĪĀ¶ČĪŖ60”ę-80”ꏱ·“Ӧɜ³ÉŅŅĖį£¬ŅņŅŅĖįŹĒŅŗĢ壬ŅŖŌŚCÖŠŹÕ¼Æµ½ŅŅĖį£¬ŠėŹ¹AÖŠ»ģŗĻŅŗµÄ·ŠµćŌŚ117.9”ęŅŌÉĻ(ÓÉĢāÖŠŠÅĻ¢µĆ³ö)£¬“ÓĶ¼Ź¾×°ÖĆæÉŅŌ擳ö£¬øĆ·“Ó¦²ÉČ”ĮĖĖ®Ō”¼ÓČȵķ½Ź½£¬ČōŅŖŹ¹·“Ó¦Õż³£½ųŠŠ£¬²¢Ź¹ŅŅĖįĖ³ĄūÕō³ö£¬ĖłŃ”ČÜŅŗµÄ·Šµć±ŲŠė±Č117.9”ęøߣ¬øł¾ŻĢāÖŠŠÅĻ¢£¬Ö»ÄÜŃ”ŌńøŹÓĶ”£ŅŅĖį×īµäŠĶµÄŠŌÖŹ¾ĶŹĒĖüµÄĖįŠŌ£¬¹ŹŅŖ¼ģŃéCÖŠŹĒ·ńŗ¬ÓŠŅŅĖįµÄÉč¼Ę·½°øÓ¦ŅŌ“ĖĪŖĒŠČėµć”£·ÖĪöĢāÖŠĢį¹©µÄĖÄÖÖŹŌ¼Į£¬ŗģÉ«ŹÆČļŹŌÖ½”¢°×É«µÄ“×ĖįĒ¦ŹŌÖ½²»ÄÜŃ”ÓĆ(ŅņŹÆČļŹŌŅŗÓöĖį±äŗģÉ«£»“×ĖįĒ¦ÓėŅŅĖį²»·“Ó¦)£¬Ōņ·½°øÉč¼ĘŹ±±ćæÉ“ÓpHŹŌÖ½ŗĶNaHCO3·ŪÄ©×ÅŹÖ”£
“š°ø£ŗ(1)2CH3CHO+O2Cu”÷2CH3COOH
(2)ŹŌ¹ÜAµÄ·“Ó¦ŅŗÖŠ””ĀŌµĶÓŚŹŌ¹ÜAµÄÖ§¹ÜæŚ“¦””ŹÕ¼Æŗ¬ŅŅĖįµÄĮó·Ö
(3)Ź¹ŹŌ¹ÜAÄŚµÄ·“Ó¦Ņŗ¾łŌČŹÜČČ·¢Éś·“Ó¦£¬Ź¹Éś³ÉµÄŅŅĖį±ä³ÉÕōĘų½ųČėŹŌ¹ÜC””øŹÓĶ
(4)·½°øŅ»£ŗ½«ÉŁĮæNaHCO3·ŪÄ©·ÅČėŅ»Ö§½ą¾»µÄŹŌ¹ÜÖŠ£¬¼ÓČėÉŁĮæŹŌ¹ÜCÖŠµÄŅŗĢ壬ČōÓŠĘųĢå²śÉś£¬ŌņĖµĆ÷ŹŌ¹ÜCÖŠŗ¬ÓŠ²śĪļŅŅĖį£»·½°ø¶ž£ŗ°ŃŅ»æépHŹŌÖ½·ÅŌŚ±ķĆęĆó(»ņ²£Į§Ę¬)ÉĻ£¬ÓĆ½ą¾»”¢øÉŌļµÄ²£Į§°ōÕŗČ”ŹŌ¹ÜCÄŚµÄŅŗĢ壬µćŌŚpHŹŌÖ½ÖŠ²æ£¬ŹŌÖ½±äÉ«ŗó£¬ÓƱź×¼±ČÉ«æØ±Č½ĻĄ“Č·¶ØČÜŅŗµÄpH£¬½ų¶ųĖµĆ÷ŹĒ·ńÓŠŅŅĖįÉś³É
11£®Čō±„ŗĶŅ»ŌŖČ©CnH2nO»¹Ō²śĪļƻӊĶ¬·ÖŅģ¹¹Ģ壬nÖµĪŖ________”£±„ŗĶŅ»ŌŖ“¼CnH2n+2OÓŠĶ¬Ąą»ÆŗĻĪļĶ¬·ÖŅģ¹¹ĢåŹ±£¬nÖµ×īŠ”ĪŖ________£»ČōÄÜ·¢ÉśĻūČ„·“Ó¦Ź±£¬nÖµ×īŠ”ĪŖ________£»Čō²»ÄÜ·¢ÉśĻūČ„·“Ó¦Ź±£¬nÖµ(n£½1³żĶā)×īŠ”ĪŖ________”£ÄÜ·¢Éś¼Ó³É·“Ó¦µÄÓŠ»śĪļ·Ö×ÓÖŠĢ¼Ō×ÓŹż×īŠ”ĪŖ________”£
 ½āĪö£ŗ¼×Č©”¢ŅŅČ©”¢±ūČ©»¹Ō²śĪļƻӊĶ¬·ÖŅģ¹¹Ģ唣
½āĪö£ŗ¼×Č©”¢ŅŅČ©”¢±ūČ©»¹Ō²śĪļƻӊĶ¬·ÖŅģ¹¹Ģ唣
ӣ
“š°ø£ŗ1”¢2”¢3””3””2””5””1
10£®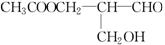 ĆĄ¹śæĘѧ¼ŅĶžĮ®”¤Åµ¶ūĖ¹”¢°ŲĮÖ”¤É³ĘÕĄūĖ¹ŗĶČÕ±¾»Æѧ¼ŅŅ°ŅĄĮ¼ÖĪŅņĶعżŹ¹ÓĆæģĖŁŗĶæÉæŲµÄÖŲŅŖ»Æѧ·“Ó¦Ą“ŗĻ³ÉijŠ©ŹÖŠŌ·Ö×ӵķ½·Ø¶ų»ńµĆ2001ÄźµÄŵ±“¶ū»Æѧ½±”£ĖłĪ½ŹÖŠŌ·Ö×ÓŹĒÖøŌŚ·Ö×ÓÖŠ£¬µ±Ņ»øöĢ¼Ō×ÓÉĻĮ¬ÓŠ±Ė“Ė»„²»ĻąĶ¬µÄĖÄøöŌ×Ó»ņŌ×ÓĶÅŹ±£¬³Ę“Ė·Ö×ÓĪŖŹÖ ŠŌ·Ö×Ó£¬ÖŠŠÄĢ¼Ō×ÓĪŖŹÖŠŌĢ¼Ō×Ó”£·²ŹĒÓŠŅ»øöŹÖŠŌĢ¼Ō×ÓµÄĪļÖŹŅ»¶Ø¾ßÓŠ¹āѧ»īŠŌ”£ĄżČē£¬ÓŠ»ś»ÆŗĻĪļ””””””””””””””””””””””
””ÓŠ¹āѧ»īŠŌ”£ŌņøĆÓŠ»ś»ÆŗĻĪļ·Ö±š·¢ÉśČēĻĀ
ĆĄ¹śæĘѧ¼ŅĶžĮ®”¤Åµ¶ūĖ¹”¢°ŲĮÖ”¤É³ĘÕĄūĖ¹ŗĶČÕ±¾»Æѧ¼ŅŅ°ŅĄĮ¼ÖĪŅņĶعżŹ¹ÓĆæģĖŁŗĶæÉæŲµÄÖŲŅŖ»Æѧ·“Ó¦Ą“ŗĻ³ÉijŠ©ŹÖŠŌ·Ö×ӵķ½·Ø¶ų»ńµĆ2001ÄźµÄŵ±“¶ū»Æѧ½±”£ĖłĪ½ŹÖŠŌ·Ö×ÓŹĒÖøŌŚ·Ö×ÓÖŠ£¬µ±Ņ»øöĢ¼Ō×ÓÉĻĮ¬ÓŠ±Ė“Ė»„²»ĻąĶ¬µÄĖÄøöŌ×Ó»ņŌ×ÓĶÅŹ±£¬³Ę“Ė·Ö×ÓĪŖŹÖ ŠŌ·Ö×Ó£¬ÖŠŠÄĢ¼Ō×ÓĪŖŹÖŠŌĢ¼Ō×Ó”£·²ŹĒÓŠŅ»øöŹÖŠŌĢ¼Ō×ÓµÄĪļÖŹŅ»¶Ø¾ßÓŠ¹āѧ»īŠŌ”£ĄżČē£¬ÓŠ»ś»ÆŗĻĪļ””””””””””””””””””””””
””ÓŠ¹āѧ»īŠŌ”£ŌņøĆÓŠ»ś»ÆŗĻĪļ·Ö±š·¢ÉśČēĻĀ
·“Ó¦ŗó£¬Éś³ÉµÄÓŠ»śĪļČŌÓŠ¹āѧ»īŠŌµÄŹĒ(””)
A£®ÓėŅŅĖį·¢Éśõ„»Æ·“Ó¦”””””””” B.ÓėNaOHĖ®ČÜŅŗ¹²ČČ
C£®ÓėŅų°±ČÜŅŗ×÷ÓĆ”””””””””””” D.ŌŚ“߻ƼĮ“ęŌŚĻĀÓėĒāĘų×÷ÓĆ
½āĪö£ŗ±¾Ģāæ¼²éµÄŹĒ¶ŌÓŠ»śĢāŅāµÄĄķ½ā”£Ņ»°ćÄѶȔ£“ÓĢāŅā·ÖĪöæÉÖŖ£¬ĖłĪ½ŹÖŠŌ£¬¼“Ķ¬Ņ»øöĢ¼Ō×ÓÉĻĮ¬ÓŠĖÄøö²»Ķ¬µÄŌ×Ó»ņŌ×ÓĶÅ£¬ÓÉÓŚÓėŅŅĖį·“Ӧɜ³ÉĮĖõ„µÄ½į¹¹£¬ÓėŌĄ“µÄõ„½į¹¹ŹĒŅ»ŃłµÄ£¬ĖłŅŌ¹āѧ»īŠŌĻūŹ§£¬A²»Ń”£»BÖŠÓÉÓŚĖ®½āÉś³ÉµÄ“¼½į¹¹ÓėŌĄ““¼µÄ½į¹¹Ņ»Ńł£¬ĖłŅŌ¹āѧ»īŠŌĻūŹ§£¬B²»Ń”£»DÖŠ·¢Éś¼ÓĒā»¹Ō£¬Éś³ÉµÄ“¼½į¹¹ÓėŌĄ““¼µÄ½į¹¹Ņ»Ńł£¬ĖłŅŌ¹āѧ»īŠŌĻūŹ§£¬D²»Ń””£
“š°ø£ŗC
9£®¾ß±ØµĄ£¬¼×ŠĶH1N1Į÷øŠŹĒæÉ·Ą”¢æÉæŲ”¢æÉÖĪµÄ£¬1,5?Īģ¶žČ©(¼ņ³ĘGA)ŹĒŅ»ÖÖÖŲŅŖµÄ±„ŗĶÖ±Į“¶žŌŖČ©”£2%µÄGAČÜŅŗ¾ßÓŠ¹ćĘ×”¢øߊ§”¢ĪŽ“Ģ¼¤”¢ĪŽøÆŹ“µČĢŲµć£¬¶Ō¼×ŠĶH1N1Į÷øŠµČ¼²²”ÓŠĮ¼ŗƵķĄÖĪ×÷ÓĆ”£øł¾ŻÉĻŹöŠÅĻ¢£¬ÅŠ¶ĻĻĀĮŠĖµ·ØÕżČ·µÄŹĒ(””)
A£®Īģ¶žČ©µÄ·Ö×ÓŹ½ĪŖC5H8O2·ūŗĻ“Ė·Ö×ÓŹ½µÄ¶žŌŖČ©ÓŠ5ÖÖ
B£®1 molĪģ¶žČ©Óė×ćĮæµÄŅų°±ČÜŅŗ·“Ó¦£¬×ī¶ąæɵĆ2 molµ„ÖŹŅų
C£®Īģ¶žČ©²»ÄÜŹ¹ĖįŠŌøßĆĢĖį¼ŲČÜŅŗĶŹÉ«
D.Īģ¶žČ©¾“ß»ÆŃõ»ÆæÉŅŌµĆµ½µÄĪģ¶žĖįÓŠ4ÖÖĶ¬·ÖŅģ¹¹Ģå
½āĪö£ŗ1,5?Īģ¶žČ©µÄ·Ö×ÓŹ½ĪŖC5H8O2£¬·ūŗĻ“Ė·Ö×ÓŹ½µÄ¶žŌŖČ©ÓŠ4ÖÖ£¬ĖłŅŌA²»ÕżČ·£»1 molĪģ¶žČ©Óė×ćĮæµÄŅų°±ČÜŅŗ·“Ó¦£¬×ī¶ąæɵĆ4 molµ„ÖŹŅų£¬ĖłŅŌB²»ÕżČ·£»Īģ¶žČ©ŗ¬ÓŠČ©»łÓŠĒ滹ŌŠŌ£¬ÄÜŹ¹ĖįŠŌKMnO4ČÜŅŗĶŹÉ«£¬ĖłŅŌC²»ÕżČ·£»Īģ¶žČ©ÓŠ4ÖÖĶ¬·ÖŅģ¹¹Ģ壬“ß»ÆŃõ»ÆµĆµ½µÄĪģ¶žĖįŅ²ÓŠ4ÖÖĶ¬·ÖŅģ¹¹Ģ壬ĖłŅŌDÕżČ·”£
“š°ø£ŗD
8£®(2007”¤ŗ£ÄĻ¾ķ)“ÓĢš³ČµÄ·¼ĻćÓĶÖŠæÉ·ÖĄėµĆµ½ČēĻĀ½į¹¹µÄ»ÆŗĻĪļ£ŗ”£
ĻÖÓŠŹŌ¼Į£ŗ¢ŁKMnO4ĖįŠŌČÜŅŗ£»¢ŚH2/Ni£»EµŚ¢Ł²½·“Ó¦________”¢A________________________________________________________________________”£
g(NH3)2OH£»¢ÜŠĀÖĘCu(OH)2£¬ÄÜÓėøĆ»ÆŗĻĪļÖŠĖłÓŠ¹ŁÄÜĶŶ¼·¢Éś·“Ó¦µÄŹŌ¼ĮÓŠ(””)
A£®¢Ł¢Ś”””” B.¢Ś¢Ū”””””” C.¢Ū¢Ü”””””””” D.¢Ł¢Ü
½āĪö£ŗøĆ»ÆŗĻĪļÖŠŗ¬ÓŠĮ½ÖÖ¹ŁÄÜĶÅ£ŗĢ¼Ģ¼Ė«¼üŗĶČ©»ł”£KMnO4ĖįŠŌČÜŅŗŹĒĒæŃõ»Æ¼Į£¬ÄÜŃõ»ÆĢ¼Ģ¼Ė«¼ü£¬Ņ²ÄÜŃõ»ÆČ©»ł£»Ģ¼Ģ¼Ė«¼üŗĶČ©»ł¶¼ÄÜŗĶĒāĘų·¢Éś¼Ó³É·“Ó¦£¬¶ų¢Ū¢Ü¶¼Ö»ÄÜŗĶČ©»ł·“Ó¦”£
“š°ø£ŗA
7£®3 gÄ³Č©ŗĶ×ćĮæµÄŅų°±ČÜŅŗ·“Ó¦£¬½į¹ūĪö³ö43.2 g Ag£¬ŌņøĆČ©ĪŖ(””)
A£®¼×Č©”””””” B.ŅŅČ©”””””””” C.±ūČ©”””””””””” D.¶”Č©
 ½āĪö£ŗŅņ1
molŅ»ŌŖČ©Ķس£æÉŅŌµĆµ½2
mol Ag£¬ĻֵƵ½0.4
mol Ag£¬¹ŹČ©ĪŖ0.2
mol£¬øĆČ©Ź½ĮæĪŖ3/0.2£½15”£“ĖĢāĖĘŗõĪŽ½ā£¬µ«1
mol¼×Č©æÉŅŌµĆµ½4
mol Ag£¬¼“3 g(0.1 mol)¼×Č©æɵƵ½43.2 g(0.4
mol)Agӣ
½āĪö£ŗŅņ1
molŅ»ŌŖČ©Ķس£æÉŅŌµĆµ½2
mol Ag£¬ĻֵƵ½0.4
mol Ag£¬¹ŹČ©ĪŖ0.2
mol£¬øĆČ©Ź½ĮæĪŖ3/0.2£½15”£“ĖĢāĖĘŗõĪŽ½ā£¬µ«1
mol¼×Č©æÉŅŌµĆµ½4
mol Ag£¬¼“3 g(0.1 mol)¼×Č©æɵƵ½43.2 g(0.4
mol)Agӣ
“š°ø£ŗA
6£®Ä³·¼Ļć×åÓŠ»śĪļµÄ·Ö×ÓŹ½ĪŖC8H6O2£¬ĖüµÄ·Ö×Ó(³ż±½»·Ķā²»ŗ¬ĘäĖū»·)ÖŠ²»æÉÄÜÓŠ(””)
A£®Į½øöōĒ»ł”””””” B.Ņ»øöČ©»ł”””””” C.Į½øöČ©»ł”””””””””” D.Ņ»øöōČ»ł
½āĪö£ŗČē¹ū·Ö×ÓÖŠ³ż±½»·ĶāĪŽĘäĖū²»±„ŗĶ¼ü£¬Ōņ·Ö×ÓŹ½ĪŖC8H10O2£¬±Č½Ļ·Ö×ÓŹ½æÉÖŖ»¹²ī4øöH£¬ĖłŅŌ“ĖÓŠ»śĪļÖŠ³ż±½»·Ķā»¹Ó¦ÓŠ2øöC”¢2øöO£¬ŌŚÕāĖÄøöŌ×Ó¼ä±ŲŠėŠĪ³ÉŅ»øöCC»ņĮ½øöĖ«¼ü(CC”¢CO)£¬Čē¹ūŠĪ³ÉŅ»øöōČ»ł(-COOH)Ö»ŗ¬Ņ»øöCO£¬ÓąĻĀµÄŅ»øöCŌ×ÓĪŽ·ØŠĪ³ÉĖ«¼ü”£
“š°ø£ŗD
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com