
题目列表(包括答案和解析)
7.碳化硅这种结构类似于金刚石的晶体,其中碳原子和硅原子的位置是交替的。在下列三种晶体①金刚石;②晶体硅;③碳化硅中,它们的熔点从高到低的顺序是 ( )
A.①③② B.②③① C.③①② D.②①③
答案: 7.A 熔点高低取决于共价键强弱,共价键强弱又与各原子的原子半径有关,C的原子半径小于Si的原子半径
6.下列各晶体中,含有的化学键类型相同且晶体类型也相同的一组是 ( )

答案: 6.D 都是共价键,NaCl形成的是离子键;SiO2形成原子晶体,NaCl形成离子晶体,
都是共价键,NaCl形成的是离子键;SiO2形成原子晶体,NaCl形成离子晶体,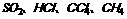 形成的都是分子晶体
形成的都是分子晶体
5.下列各组物质汽化或熔化时,所克服的粒子间作用力完全相同的是 ( )
A.碘的升华和干冰汽化 B.2氧化硅和干冰熔化
C.苯和硝酸钾熔化 D.食盐和冰熔化
答案: 5.A碘和干冰都是分子晶体,克服分子间作用力;B选项二氧化碳克服共价键;C选项硝酸钾克服的是离子键,苯克服分子间作用力;D选项食盐克服离子键
4.下列物质的晶体中不存在分子的是 ( )

答案: 4.AsiO2是原子晶体;构成晶体的粒子是原子
3.下列叙述中正确的是 ( )
A.离子晶体中肯定不含非极性共价键
B.原子晶体的熔点肯定高于其他晶体
C.由分子组成的物质其熔点一般较低
D.原子晶体中除去极性共价键外不可能存在其他类型的化学键
答案:3.C;A选项离子晶体中有时也含非极性共价键,例Na2O2;B选项SiO2的熔点为1 723℃,而钨(W)熔点为3 410℃;C选项分子晶体一般熔点较低; D选项金刚石晶体C-C间为非极性共价键
2.下列晶体由原子直接构成,且属于分子晶体的是 ( )
A.干冰 B.固态氖 C.白磷 D.三氯化铝
答案:2.B 氖(Ne)是单原子分手,是分子晶体,干冰、白磷、AlCl3是由分子构成的分子晶体
1.下列晶体中属于原子晶体的是 ( )
A.氖 B.食盐 C.干冰 D.金刚石
答案:1.D 根据原子晶体的组成特点及常见的性质判断
2.理解并掌握晶体类型与性质的关系,大致掌握晶体性质的比较思路和方法,例如物质熔沸点的比较。
(1)一般来说,异类晶体:原子晶体>离子晶体>分子晶体(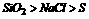 );
);
(2)同类晶体:
原子晶体的决定因素:共价键键能通过原子半径比较键长(C>Si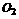 >SiC>Si)。
>SiC>Si)。
分子晶体的决定因素:①范氏力结构组成相似时,比较相对分子质量(Ch>CBr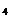 >CC
>CC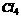 >C
>C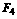 )。
)。
②相对分子质量相同,比较
注:分子晶体性质比较时,注意分子间有无氢键存在,有则首先考虑氢键的影响。
离子晶体的决定因素:静电引力的大小比较离子电荷、离子半径(MgO>Mg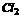 >NaCl>CsCl)。
>NaCl>CsCl)。
1.学习本节知识要充分利用模型了解典型晶体的空间结构,纠正平面结构的错觉,培养空间想像能力。空间想像能力较差的学生开始可借助模型分析,慢慢地再放开模型想像。理解晶体结构的共同点,晶体质点(原子、分子、离子)排列有规则,隔一定的距离重复出现,有明显的周期性;要注意与周期律、物质结构知识内容相联系,要善于利用数学工具掌握计数规则,灵活应用分析方法,如何借助已学过的典型晶体结构(如氯化钠晶体等)为模型进行联想、类比和迁移,培养知识的迁移能力和理论联系实际的应用能力。
(1)离子晶体:离子半径越小,离子电荷数越大,离子键越强,晶体熔、沸点就越高,如KF>KCI> KBr,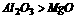 。
。
(2)分子晶体:组成和结构相似的分子晶体,相对分子质量越大,分子间作用力越强,熔、沸点越高,如
 。
。
注:①分子晶体性质比较时,注意分子间有无氢键存在,有则首先考虑氢键的影响;
②在同分异构体中,一般支链越多,熔、沸点越低,如沸点正戊烷>异戊烷>新戊烷;同分异构体
的芳香烃及其衍生物其熔、沸点高低顺序是邻>间>对位化合物。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com