
题目列表(包括答案和解析)
21.(12分)(1)控制变量是科学研究中的重要研究方法,其基本思路是,在实验研究中人为只改变一个因素(调节变量),其他因素保持相同,观察测定因调节变量改变而改变的因素(因变量),从而分析得到研究结论.中学化学中应用控制变量的方法研究问题的例子很多.请分析或设计:
①在研究浓度对化学反应速率的影响时,教材安排了利用Na2S2O3与H2SO4反应的一组对照实验(Na2S2O3+H2SO4
 Na2SO4+S↓+SO2↑+H2O)
Na2SO4+S↓+SO2↑+H2O)
|
烧杯编号 |
加3% Na2S2O3溶液体积(mL) |
加H2O体积(mL) |
加(体积之比为1∶20)H2SO4溶液体积(mL) |
所需时间(s) |
|
1 |
5 |
5 |
2 |
|
|
2 |
7 |
3 |
2 |
|
|
3 |
10 |
0 |
2 |
|
在三个烧杯(底部有黑色“十”字标记)内分别加入表中所示体积的三种液体,搅拌并开始计时,到出现浑浊使烧杯底部“十”字看不见时停止计时.比较所需时间,得出浓度对化学反应速率影响的结论.实验中,温度和反应体系中硫酸浓度是保持相同的因素,调节变量是________,因变量是________.
②运用控制变量原理设计实验,利用纯碱溶液探究温度对盐的水解的影响,简述实验方法:______________________________________________________________________________________.
(2)373 K时,H2PO与OH-发生如下反应:
H2PO+OH-
 HPO+H2O
HPO+H2O
反应结果如下表所示:
|
H2PO起始浓度(mol/L) |
0.10 |
0.50 |
0.50 |
|
OH-起始浓度(mol/L) |
1.00 |
1.00 |
4.00 |
|
反应速率[mol/(L·s)] |
3.2×10-5 |
1.60×10-4 |
2.56×10-3 |
如果用v=kcm(H2PO)·cn(OH-)表示反应速率(k为与浓度无关的常数)
①k=________, m=________, n=________.
②若c(H2PO)的起始浓度为0.20 mol/L, c(OH-)的起始浓度为1.50 mol/L,则反应速率v=____________.
解析:(1)实验改变的条件是Na2S2O3和水用量相对大小,故调节变量是Na2S2O3溶液的浓度,因变量是反应所需时间.利用控制变量原理设计实验探究温度对水解反应的影响,则控制变量是温度,因变量是水解程度大小,可用加入指示剂通过溶液颜色深浅来表示或用pH表示.
(2)①OH-的浓度均为1.00 mol/L时,
H2PO的浓度由0.10→0.50,浓度变为原来的5倍,反应速率由3.2×10-5→1.60×10-4,即反应速率变为原来的5倍,因此m=1;同理H2PO的浓度均为0.50 mol/L时,OH-的浓度由1.00→4.00,浓度变为原来的4倍,反应速率由1.60×10-4→2.56×10-3,即反应速率变为原来的16=42倍,因此n=2.
利用第一组数据有:3.2×10-6=k·(0.10)1×(1.00)2,所以k=3.2×10-4
②此时,v=3.2×10-4 mol/(L·s)×(0.20 mol/L)×(1.50mol/L)2=1.44×10-4 mol/(L·s)
答案:(1)①Na2S2O3溶液的浓度 所需时间
②取三支试管各放同浓度同体积的纯碱溶液,滴1-2滴酚酞试液,第一支不加热,第二支加热至t1℃,第三支加热至t2℃,观察三支试管中溶液的颜色深浅,温度越高,颜色越深,说明碱性越强,则水解程度越大(其他合理答案均给分,例如不同温度下测定同浓度同体积纯碱溶液的pH)
(2)①3.2×10-4 1 2
②1.44×10-4mol/(L·s)
20.(10分)物质在制取或配制成溶液时往往应用化学平衡的知识.
(1)钾是一种活泼的金属,工业上通常用金属钠和氯化钾在高温下反应制取.该反应为:Na(l)+KCl(l)
 NaCl(l)+K(g) ΔH>0,该反应的平衡常数可表示为:K=c(K),各物质的沸点与压强的关系见下表.
NaCl(l)+K(g) ΔH>0,该反应的平衡常数可表示为:K=c(K),各物质的沸点与压强的关系见下表.
|
压强(kPa) |
13.33 |
53.32 |
101.3 |
|
K的沸点(℃) |
590 |
710 |
770 |
|
Na的沸点(℃) |
700 |
830 |
890 |
|
KCl的沸点(℃) |
|
|
1437 |
|
NaCl的沸点(℃) |
|
|
1465 |
①在常压下金属钾转变为气态从反应混合物中分离的最低温度约为________,而反应的最高温度应低于________.
 ②常压下,当反应温度升至900℃时,该反应的平衡常数可表示为:K=________.
②常压下,当反应温度升至900℃时,该反应的平衡常数可表示为:K=________.
(2)实验室中配制碘水,往往是将I2溶于KI溶液中,这样就可以得到浓度较大的碘水,主要是因为发生了反应:I2(aq)+I-
 I
I
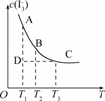
上述平衡体系中,I的物质的量浓度c(I)与温度T的关系如图所示(曲线上的任何一点都表示平衡状态).
①通过分析上图,该反应的正反应为________反应(填“吸热”或“放热”).
②在T1、D状态时,v正________v逆(填“>”“<”或“=”).
解析:(1)①由于钠的金属性比钾弱,所以要制取钾,应该利用影响化学平衡的条件,使平衡向正反应方向移动.在常压下金属钾转变为气态从反应混合物中分离的最低温度应等于钾的沸点,最高温度应低于钠的沸点.
②当温度升至900℃时,钠也为气态,故上述反应可表示为:Na(g)+KCl(l)
 NaCl(l)+K(g),故其平衡常数为K=.
NaCl(l)+K(g),故其平衡常数为K=.
(2)①由图可知,升高温度,c(I)降低,说明平衡逆向移动 ,则正反应为放热反应.
②T1、D状态时,还未达到平衡,而可逆反应最终都要达到平衡状态,所以必须增大c(I)才能达到平衡状态,即反应正向进行,v正>v逆;
答案:(1)①770℃ 890℃ ②
(2)①放热 ②>
19.(7分)在一体积为10 L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:
CO(g)+H2O(g)CO2(g)+H2(g) ΔH<0
(1)CO和H2O浓度变化如下图,则0-4 min的平均反应速率v(CO)=________mol/(L·min).
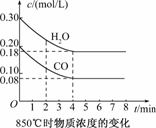
t1℃时物质浓度(mol/L)的变化
|
时间/min |
CO |
H2O |
CO2 |
H2 |
|
0 |
0.200 |
0.300 |
0 |
0 |
|
2 |
0.138 |
0.238 |
0.062 |
0.062 |
|
3 |
C1 |
c2 |
c3 |
c3 |
|
4 |
C1 |
c2 |
c3 |
c3 |
|
5 |
0.116 |
0.216 |
0.084 |
|
|
6 |
0.096 |
0.266 |
0.104 |
|
(2)t1℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表.
①表中3 min-4 min 之间反应处于________状态;c1________0.08 mol/L(填“>”“<”或“=”).
②反应在4 min-5 min间,平衡向逆方向移动,可能的原因是________(单选),表中5 min-6 min之间数值发生变化,可能的原因是________(单选).
a.增加水蒸气 b.降低温度
c.使用催化剂 d.增加氢气浓度
解析:(1)v(CO)=
=0.03 mol/(L·min).
(2)①0 min-2 min, c(CO)减小 0.062 mol/L,即平均速率为0.031 mol/(L·min),由于反应速率一般随反应的进行而减慢,所以2 min-3 min, c(CO)的减小值小于0.31 mol/L,因此c1>(0.138-0.031) mol/L>0.08 mol/L;
②由于降低温度平衡向右移动,所以4 min-5 min的条件变化不是b,由于c(CO2)减小,应是增加了H2浓度;第5 min-6 min, c(CO)减小,c(H2O)增大,c(CO2)增大,应是增加了水蒸气.
答案:(1)0.03 (2)①平衡 > ②d a
18.(7分)某温度下,密闭容器中充入1 mol N2和3 mol H2,使之反应合成NH3,平衡后,测得NH3的体积分数为n0,如果温度不变,只改变起始加入量,使之反应平衡后NH3的体积分数为n0,N2、H2、NH3的物质的量分别用x、y、z表示.
(1)恒温恒容条件下:
①若x=0, y=0,则z=________.
②若x=0.75 mol, 则y=________, z=________.
③x、y、z满足的一般条件是________.
(2)恒温恒压条件下,x、y、z满足的一般条件是
______________________________________.
解析:本题起始状态不同,但最终NH3的体积分数相同,即最终各平衡是等效的.恒温怛容条件下,“一边倒”后,对应的各物质的物质的量相等即可,例如“左倒”后,都是1 mol N2和3 mol H2,故①x=0, y=0,则z=2 mol;②若x=0.75 mol,则y=2.25 mol, z=0.5 mol;③“左倒”后,生成的N2为 mol,生成的H2为 mol,所以x+=1 mol, y+=3 mol.恒温恒压下,“一边倒”后,求得N2、H2物质的量之比为1∶3即可.
答案:(1)①2 mol ②2.25 mol 0.5 mol
③2x+z=2 mol, 2y+3z=6 mol
(2)x∶y=1∶3, z为任意值或x=y=0, z≥0.
17.(6分)在某一容积为2 L的密闭容器内,加入0.8 mol的H2和0.6 mol的I2,在一定的条件下发生如下反应:H2(g)+I2(g)
 2HI(g) ΔH<0
2HI(g) ΔH<0
反应中各物质的浓度随时间变化情况如图所示:
(1)该反应的化学平衡常数表达式为________.
(2)根据图所示数据,反应开始至达到平衡时,平均速率v(HI)为________.
(3)反应达到平衡后,第8分钟时:
 ①若升高温度,化学平衡常数K________(填写增大、减小或不变),HI浓度的变化正确的是________(用右图中a-c的编号回答).
①若升高温度,化学平衡常数K________(填写增大、减小或不变),HI浓度的变化正确的是________(用右图中a-c的编号回答).
②若加入I2,H2浓度的变化正确的是________(用右图中d-f的编号回答).
解析:(1)由平衡常数的定义可知反应的平衡常数表达式.
(2)由图可知3 min时达到平衡,v(HI)==0.167 mol/(L·min).
(3)①升高温度,平衡向左移动,c(HI)减小而c(H2)、c(I2)增大,所以K减小,c(HI)的变化符合图中的c;②若加入I2,平衡向右移动,c(H2)减小,应是图中的f.
答案:(1)K=
(2)0.167 mol/(L·min) (3)①减小 c ②f
16.在体积可变的密闭容器中,反应mA(g)+nB(s)
 pC(g)达到平衡后,压缩容器的体积,发现A的转化率随之降低.下列说法中,正确的是
pC(g)达到平衡后,压缩容器的体积,发现A的转化率随之降低.下列说法中,正确的是
( )
A.(m+n)必定小于p B.(m+n)必定大于p
C.m必定小于p D.m必定大于p
解析:压缩容器的体积相当于增大压强,平衡向气体体积缩小的方向移动,A的转化率降低,说明平衡逆向移动,所以逆向是气体体积缩小的方向,选项C正确.
答案:C
第Ⅱ卷 (非选择题,共52分)
15.将2 mol A和1 mol B充入某密闭容器中发生反应:2A(g)+B(g)
 xC(g),达到化学平衡后,C的体积分数为a.假设该反应的条件分别和下列各选项的条件相同,下列判断正确的是
xC(g),达到化学平衡后,C的体积分数为a.假设该反应的条件分别和下列各选项的条件相同,下列判断正确的是
( )
A.若在恒温恒压下,当x=1时,按1.5 mol A、1 mol C作为起始物质,达到平衡后,C的体积分数仍为a
B.若在恒温恒容下,当x=2时,将2 mol C作起始物质,达到平衡后,C的体积分数仍为a
C.若在恒温恒压下,当x=3时,1 mol A、1 mol B、6 mol C作起始物质,达到平衡后,C的体积分数仍为a
D.若在恒温恒容下,按0.6 mol A、0.3 mol B、1.4 mol C作起始物质,达到平衡后,C的体积分数仍为a,则x只能等于2
解析:将选项A和C中的C的物质的量转化后所得A、B的物质的量之比均与题干中两物质的物质的量之比不等,故A、C错误;将B项中C的物质的量转化后所得A、B的物质的量与题干中对应A、B的物质的量相等,B正确;D项中,因A、B的物质的量之比与题干中反应化学计量数之比相等,若x=3,即反应前后气体分子数目不变时,转化后所得A、B物质的量之比为2∶1,此时仍与由2 mol A和1 mol B构成的体系等效,体积分数同样保持不变,因此当x=3时符合题意,x=2不符合题意,D错.
答案:B
14.(2009·广东高三模拟)下图所示是在恒温下某化学反应的反应速率随时间变化的示意图.下列说法不符合该示意图的是
( )
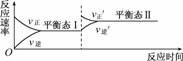
A.反应达到平衡时,正反应和逆反应速率相等
B.该反应达到平衡态Ⅰ以后,增大反应物的浓度,平衡发生移动,达到平衡态Ⅱ
C.反应达到平衡态Ⅰ以后,减小反应物浓度,平衡发生移动,达到平衡态Ⅱ
D.同一种反应物在平衡态Ⅰ和平衡态Ⅱ时浓度不相等
解析:A项,任一可逆反应达平衡时,v正、v逆均相等;B项,由图示可知反应达平衡后某时刻v正忽然增加,这一瞬间v逆不变,故应是增大了反应物的浓度;B项对,C不符合图像;D项,平衡态Ⅱ时反应物浓度应大于平衡态Ⅰ的浓度.
答案:C
13.反应2A(g)+B(g)
 xC(g)+2D(s),在一定条件下的2 L容器中,1 mol A与0.5
mol B反应达到平衡时A为0.3 mol/L,在1 L容器中1 mol A与0.5
mol B在相同温度下反应达到平衡时A为0.5 mol/L,则x值最合适为
xC(g)+2D(s),在一定条件下的2 L容器中,1 mol A与0.5
mol B反应达到平衡时A为0.3 mol/L,在1 L容器中1 mol A与0.5
mol B在相同温度下反应达到平衡时A为0.5 mol/L,则x值最合适为
( )
A.2 B.1
C.大于2 D.小于3
解析:假设在缩小容器体积(加压)的过程中平衡不移动,则在1 L容器中反应达平衡时A的浓度应该为0.6 mol/L,而实际上是0.5 mol/L,说明在加压过程中平衡向正反应方向移动,即有 2+1>x,故x<3.
答案:D
12.合成氨工业对国民经济和社会发展具有重要的意义,对于密闭容器中的反应:N2(g)+3H2(g)  2NH3(g),在637 K、30
MPa下n(NH3)和n(H2)随时间变化的关系如图所示.下列叙述正确的是
2NH3(g),在637 K、30
MPa下n(NH3)和n(H2)随时间变化的关系如图所示.下列叙述正确的是
( )
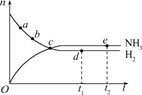
A.点a的正反应速率比点b的大
B.点c处反应达到平衡
C.点d(t1时刻)和点e(t2时刻)处n(N2)不一样
D.其他条件不变,773 K下反应至t1时刻,n(H2)比图中d点的值大
解析:由题意n(H2)随时间的变化曲线的斜率知在a点n(H2)的变化量大于b点n(H2)的变化量,即a点的正反应速率大于b点.虽然c点时n(H2)=n(NH3),但二者的物质的量仍在随时间发生变化,故c点并没有达到平衡,B不正确.由于在t1、t2时刻反应已达平衡,故两时刻n(N2)一样多,C不正确.由于合成氨的反应是一个放热反应,温度升高时,化学平衡向逆反应方向移动,则在其他条件不变时773 K下反应至t1时n(H2)比图中d的值大.故本题答案为A、D.
答案:AD
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com