
题目列表(包括答案和解析)
9.常温下,pH=11的氨水和pH=1的盐酸等体积混合后(不考虑混合后溶液体积的变化),恰好完全反应,则下列说法不正确的是
( )
A.弱碱的浓度大于强酸的浓度
B.反应后的溶液呈酸性
C.原氨水中有1%的含氮粒子为NH
D.反应后的溶液中NH、NH3·H2O与NH3三种粒子的平衡浓度之和为0.05 mol/L
解析:氨水与盐酸等体积混合后,恰好完全反应,此两者浓度相等;混合后溶质是NH4Cl,应呈酸性;原氨水的浓度为0.1 mol/L,电离出10-3 mol/L NH,故NH占1%;体积扩大为原来的2倍后,根据原子守恒,含氮元素的三种粒子平衡浓度之和为0.05 mol/L.
答案:A
8.在一定体积pH=12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液pH=11.若反应后溶液的体积等于Ba(OH)2溶液与NaHSO4溶液的体积之和,则Ba(OH)2溶液与NaHSO4溶液的体积比是
( )
A.1∶9 B.1∶1
C.1∶2 D.1∶4
解析:设Ba(OH)2溶液的体积为V1,NaHSO4溶液的体积为V2,浓度为c2,则由Ba2++SO===BaSO4↓有:
×10-2 mol/L·V1=V2·c2 ①
又由于混合后溶液的pH=11,得:
=10-3mol/L ②
解①②可得:V1∶V2=1∶4.
答案:D
7.已知甲酸钠(HCOONa)溶液呈碱性.室温下用c(H+)相同、体积相同的盐酸与甲酸(HCOOH)溶液分别进行如下实验,相关叙述正确的是
( )
A.加水稀释,两溶液中的氢离子数目都不变
B.用等浓度NaOH溶液中和,盐酸比甲酸消耗的碱液少
C.跟等质量铝粉反应,盐酸比甲酸的起始反应速率快
D.跟过量的锌粒反应,盐酸比甲酸产生氢气的量多
解析:由题知甲酸是弱酸,A项,加水稀释,由于甲酸中存在电离平衡,平衡向电离方向移动,则甲酸溶液中H+数目增多,A错;B项,甲酸是弱酸,盐酸是强酸,c(H+)相同时,甲酸浓度远大于盐酸浓度,等体积时,盐酸消耗NaOH少,B对;C项,起始时c(H+)相同,则反应速率相等,C错;D项,由B项分析知应是甲酸产生H2量多,D错.
答案:B
6.用标准盐酸滴定未知浓度的NaOH溶液时,若测定结果偏高,则产生误差的原因可能是
( )
A.滴定时,装NaOH溶液的锥形瓶未用NaOH溶液润洗
B.酸式滴定管用蒸馏水洗后,未用盐酸润洗
C.滴定前,酸式滴定管尖嘴处有气泡,而在滴定后气泡消失
D.滴定前以仰视的姿势读取了酸式滴定管的读数,滴定后读数正确
解析:A项对滴定结果无影响;B项标准盐酸被解释,用量增多,结果偏高;C项此种情况导致消耗盐酸偏多,测量结果偏高;D项此种情况导致盐酸体积偏小,测量结果偏低.
答案:BC
5.(2009·淄博模拟)已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.0×10-16.下列关于不溶物之间转化的说法中错误的是
( )
A.AgCl不溶于水,不能转化为AgI
B.两种不溶物的Ksp相差越大,不溶物就越容易转化为更难溶的不溶物
C.AgI比AgCl更难溶于水,所以AgCl可以转化为AgI
D.常温下,AgCl若要在NaI溶液中开始转化为AgI,则NaI的浓度必须不低于×10-11mol/L
解析:不溶于水不是绝对的不溶,而是溶解度小于0.1 g.尽管AgCl溶解的很少,但由于AgI比AgCl更难溶于水,溶液中微量的Ag+在I-浓度足够大的溶液中,可以转化为AgI,而使AgCl的溶解平衡向产生Ag+的方向移动,导致AgCl溶解,所以A错误.根据·c(I-)=1.0×10-16可计算得:c(I-)=×10-11 mol/L,D正确.
答案:A
4.(2009·天津滨海新区高三联考)下列叙述中不正确的是
( )
A.一定浓度的醋酸钠溶液可使酚酞溶液变红,其原因是发生了如下反应:CH3COO-+H2O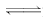
 CH3COOH+OH- ,使得溶液中的c(OH-)>c(H+)
CH3COOH+OH- ,使得溶液中的c(OH-)>c(H+)
B.在常温下,10 mL 0.02 mol/L HCl溶液与10 mL 0.02 mol/L Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=12
C.在0.1 mol/L NH4Cl溶液中:c(H+)+c(NH)=c(Cl-)+c(OH-)
D.将0.2 mol/L的盐酸与0.1 mol/L的NaAlO2溶液等体积混合,其溶液中离子浓度由小到大的顺序为:c(OH-)<c(Al3+)<c(H+)<c(Na+)<c(Cl-)
解析:A项,CH3COONa溶液呈碱性,正是因为CH3COO-水解,所以A项正确.B项,混合后c(OH-)==0.01 mol/L,故pH=12,B对.C项,电荷守恒,正确.D项,假设各为1 L溶液,混合后生成产物有Al(OH)3沉淀、AlCl3和NaCl,则溶液中c(Al3+)>c(H+),故D错.
答案:D
3.(2009·江苏南京质检)下列判断正确的是
( )
A.酸性溶液中Fe3+、Al3+、NO能大量共存
B.AlCl3溶液蒸干后得到的固体是AlCl3
C.在0.1 mol/L CH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+)
D.pH=3的醋酸溶液跟pH=11的氢氧化钡溶液等体积混合后,溶液pH=7
解析:B项,由于Al3+的水解,HCl具有挥发性,所以AlCl3溶液蒸干后得到Al(OH)3,灼烧后变为Al2O3;D项,混合后CH3COOH有剩余,溶液显酸性;C项为质子守恒.
答案:AC
2.对氨水溶液中存在的电离平衡NH3·H2O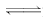 NH+OH-,下列叙述正确的是
NH+OH-,下列叙述正确的是
( )
A.加水后,溶液中n(OH-)增大
B.加入少量浓盐酸,溶液中c(OH-)增大
C.加入少量浓NaOH溶液,电离平衡向正反应方向移动
D.加入少量NH4Cl固体,溶液中c(NH)减小
解析:加水稀释,电离平衡向右移动,n(OH-)增大,A正确;加入盐酸中和OH-,虽平衡向右移动,但c(OH-)减小,B错误;加入浓NaOH溶液,使c(OH-)增大,电离平衡逆向移动,C错误;加入少量NH4Cl固体,溶液中c(NH)增大,D错误.
答案:A
1.H2S溶液中,在采取措施使pH增大的同时,则c(S2-)的变化情况是
( )
A.增大 B.减小
C.不变 D.可能增大,也可能减小
解析:在H2S溶液中存在H2S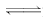 H++HS-,
HS-
H++HS-,
HS-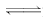 H++S2-.当加碱时,以上两平衡都右移,pH增大,则c(S2-)增大;当通入SO2时,发生SO2+2H2S===3S↓+H2O平衡左移,pH增大,但c(S2-)减小.
H++S2-.当加碱时,以上两平衡都右移,pH增大,则c(S2-)增大;当通入SO2时,发生SO2+2H2S===3S↓+H2O平衡左移,pH增大,但c(S2-)减小.
答案:D
13.(1)在下面元素周期表中全部是金属元素的区域为____.
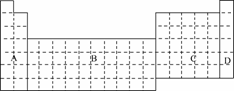
a.A b.B
c.C d.D
(2)有人认为形成化合物最多的元素不是ⅣA族的碳元素,而是另一种短周期元素,请你根据学过的化学知识判断这一元素是________.
(3)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜;乙元素原子核外M电子层与K电子层上的电子数相等.
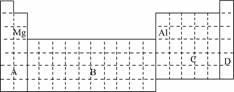
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置.
②甲、乙两元素相比较,金属性较强的是________(填名称),可以验证该结论的实验是
________.
a.将在空气中放置已久的这两种元素的块状单质分别放入热水中
b.将这两种元素的单质粉末分别和同浓度的盐酸反应
c.将这两种元素的单质粉末分别和热水作用,并滴入酚酞试剂
d.比较这两种元素的气态氢化物的稳定性
解析:(1)据元素周期表、元素周期律知识可知:A区为金属元素、非金属元素共存区;B区为过渡元素,全部为金属元素;C区为金属元素、非金属元素共存区;D区为0族元素或稀有气体元素.
(2)碳、氢两种元素均可形成无机物、有机物,且碳、氢是形成有机物的主要元素,但是在无机物中,碳形成的化合物不如氢形成的化合物多.
(3)据题意可知:甲为Al元素,乙为Mg元素;同周期元素随原子序数的递增,金属性逐渐减弱,故Mg的金属性较强,验证该结论的依据是判断元素金属性强弱的规律:金属单质与H2O或酸反应放出H2的难易程度.
答案:(1)b (2)H (3)①见下表中 ②镁 ③bc
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com