
题目列表(包括答案和解析)
9.关于IA族和ⅡA族元素的下列说法中正确的是 ( )
A.同一周期中,IA族单质的熔点比ⅡA族的高
B.浓度都是0.01mol几时,氢氧化钾溶液的pH比氢氧化钡的小
C.氧化钠的熔点比氧化镁的高
D.加热时,碳酸钠比碳酸镁易分解
答案:9.B A选项同一周期,Na熔点低于Mg熔点;B选项一般c(OH-)越大,pH-越大,而同浓度KOH比Ba(OH)2的c(OH‑)小;C选项Na2o熔点低于MgO熔点;D选项Na2O受热更易分解
8.下列性质适合于分子晶体的是 ( )
A.熔点1 070℃,易溶于水,水溶液能导电
B.熔点10.31℃,液态不导电,水溶液能导电
C.能溶于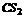 ,熔点112.8℃,沸点444.6℃
,熔点112.8℃,沸点444.6℃
D.熔点97.81℃,质软、导电,密度0.97g/
答案:8.BC 对比各类晶体的物理性质去判断
7.下列化学式表示物质分子组成的是 ( )
A.NaCl B.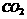 C.Cu D.
C.Cu D. 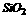
答案:7.B A选项NaCI是由Na+、C1-按一定比例组成;C选项Cu形成金属晶体内含Cu2+和自由电子;D选项SiO2由Si原子和O原子构成
6.下列说法一定正确的是 ( )
A.其水溶液导电的一定是离子晶体 B.熔融态导电的一定是离子晶体
C.固态导电的一定是金属晶体 D.固态不导电,熔融态导电的一定是离子晶体
答案:6.D A选项HCI的水溶液可以导电;B选项金属熔融态也可导电,C选项石墨可以导电
5.将SiCl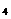 与过量的液氨反应可生成化合物
与过量的液氨反应可生成化合物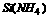 , 将该化合物在无氧条件下高温灼烧,可得到氮化硅(
, 将该化合物在无氧条件下高温灼烧,可得到氮化硅(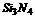 )固体。氧化硅是一种新型的耐高温、耐磨材料,在工业上有广泛的应用。则氮化硅所属的晶体类型是 ( )
)固体。氧化硅是一种新型的耐高温、耐磨材料,在工业上有广泛的应用。则氮化硅所属的晶体类型是 ( )
A.原子晶体 B.分子晶体 C.离子晶体 D.金属晶体
答案:5.A
4.关于晶体的下列说法正确的是 ( )
A.在晶体中只要有阴离子就一定有阳离子
B.在晶体中只要有阳离子就一定有阴离子
C.原子晶体的熔点一定比金属晶体的高
D.分子晶体的熔点--定比金属晶体的低
答案:4.A B选项金属晶体内有金属阳离子,但无阴离子;C选项原子晶体如Si02熔点1 723℃,钨熔点为3 410℃;D选项分子晶体12熔点为113.5℃,而汞熔点为-38.87℃
3.下列各组物质中,按熔点由低到高排列正确的是 ( )

答案:3.B 一般来说,异类晶体:原子晶体>离子晶体>分子晶体的熔、沸点;金属原子半径越小,最外层电子数越多,则金属离子与自由电子之间的相互作用越强,熔、沸点越高
2.在自然界中能以游离态存在的元素是下列中的 ( )
A.磷 B.硅 C.钠 D.金
答案:2.D 根据元素的活动性判断
1.金属的下列性质中,不能用金属晶体结构加以解释的是 ( )
A.易导电 B.易导热 C.有延展性 D.易锈蚀
答案:1.D 金属腐蚀大多数发生的是屯化学腐蚀,是由于能导电的杂质不如该金属活泼,也有的是接触腐蚀性气体或电解质溶液导致的,与金属晶体结构无关
2.结合金属结构的特点,把握住“自由电子”这一关键,进而掌握金属晶体的特性,并能用之解释金属能导电、导热、有良好延展性的原因。潜能开发 [例1]下列叙述中正确的是 A.分子晶体中一定存在共价键 B.离子晶体中一定含金属元素 C.原子晶体一定不存在离子 D.晶体中有阳离子必含有阴离子
思路分析
A中由稀有气体分子构成的分子晶体中不含共价键;B中铵盐晶体虽然是离子晶体但不含金属元素;D在金属晶体中只有金属阳离子和自由电子,不含有阴离子;只有C正确,在原子晶体中原子与原子间只有共价键。
[答案]C
[例2]下列有关金属元素特征的叙述中正确的是 ( )
A.金属元素的原子只有还原性,离子只有氧化性
B.金属元素在化合物中一定显正价
C.金属元素在不同化合物中的化合价均不同 ]
D.金属单质在常温下都是金属晶体
思维诊断
本题涉及几种晶体组成的粒子及化学键,并对各类晶体中存在的特例进行了考查,故我们对每个选项应逐一分析,找出可能出现的特例并加以排除,才能准确作答。
A一些有可变化合价的元素如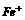 既有氧化性又有还原性;C金属在不同化合物中化合价可以相同;D金属汞在常温下是液态,不属于晶体,只有B正确。
既有氧化性又有还原性;C金属在不同化合物中化合价可以相同;D金属汞在常温下是液态,不属于晶体,只有B正确。
[答案]B
思维诊断
对于判断正误的习题一定要抓住每个选项中的关键词语,结合我们对化学概念的理解然后得出正确的结论。
知能达标训练
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com