
题目列表(包括答案和解析)
12.在60g体中,含有Si--O键的物质的量为 ( )
A.1 mol A.2 mol C.3 mol D.4 mol
答案: 12.D 60gSiO2为lmol,1 molSiO2含有4molSi--O键
11.有关晶体的下列说法中正确的是 ( )
A.晶体中分子间作用力越大,分子越稳定
B.原子晶体中共价键越强,熔点越高
C.冰熔化时水分子中共价键发生断裂
D.氯化钠熔化时离子键未被破坏
答案: 11.B
10.在石墨晶体里,每一层由无数个正六边形构成,同一层内每个碳原子与相邻的三个碳原子以C--C键结合,则石墨晶体中碳原子数与C--C键数之比为 ( )
A.1:1 B.2:l C.2:3 D.3:2
答案: 10.C 石墨晶体中,每个碳原子与3个碳原子形成C--C,而在每个键中的贡献只有一半,所以C原子个数与C--C键数之比为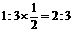
9.下列含有非极性键的离子晶体是 ( )
①醋酸钠 ②氢氧化钾 ③过氧化钠 ④金刚石 ⑤乙醇 ⑥氯化钙
A.①②③⑥ B.①③ C.①③④⑤ D.①②⑥
答案: 9.BC H3COONa中C--C间为非极性键且是离子晶体,Na2O2中有非极性键
8.水的沸点是100℃,硫化氢的分子结构跟水相似,但它的沸点却很低,是-60.7℃,引起这种差异的主要原因是 ( )
A.分子间作用力 B.共价键 C.氢键 D.相对分子质量
答案:8.C 考虑H2O可形成氢键
7. 的分子结构与
的分子结构与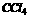 类似,对其做出如下推断:①
类似,对其做出如下推断:① 晶体是分子晶体;②常温常压
晶体是分子晶体;②常温常压 不是气体;③
不是气体;③ 分子是由极性键构成的非极性分子;④
分子是由极性键构成的非极性分子;④ 熔点高于
熔点高于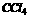 。其中正确的是 ( )
。其中正确的是 ( )
A.只有① B.只有①② C.只有②③ D.①②③④
答案: 7.D 根据CCl4性质可知SiCl4性质
6.IA族元素的原子与最外层有7个电子的原子结合,可以形成 ( )
A.离子晶体 B.原子晶体 C.分子晶体 D.无法确定
答案: 6.A、C IA元素有氢元素和碱金属,Vifa元素为卤族元素,故可形成分子晶体或离子晶体
5.碳有三种同素异形体,金刚石、石墨、足球烯(Cs。),其中足球烯是分子晶体。据此推测,下列叙述正确的是 ( )
A.足球烯不可以发生加成反应
B.三者和氧气反应的最终产物不同
C.足球烯在苯中的溶解度比在乙醇中的溶解度大
D.石墨、足球烯均可作为生产耐高温润滑剂的原料
答案: 5.C、D A选项足球烯有双键可发生加成反应;B选项三者和氧气反应最终产物都是CO2;C选项足球烯在苯中溶解度大;D选项石墨、足球烯均可作为生产耐高温润滑剂的原料
4.氮化硅是一种新合成的结构材料,它是一种超硬、耐磨、耐高温的物质。下列各组物质熔化时,所克服的粒子间作用力与氮化硅熔化时所克服的作用力相同的是 ( )
A.硝石和金刚石 B.晶体硅和水晶
C.冰和干冰 D.萘和碘
答案: 4.B 通过分析氮化硅性质得知它应属于原子晶体,熔化时应克服共价键
3.金刚石和石墨两种晶体中,每个最小的碳环里所包含的碳原子数 ( )
A.前者多 B.后者多 C.相等 D.无法确定
答案: 3.C根据模型结构特点,每个最小的碳环里所包含的碳原子数相等,都为6个
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com