
18£®(12·Ö)(08Äê½ËƠ»¯Ñ§¡¤21A)
̉ÑÖªA¡¢B¡¢C¡¢D¡¢E¶¼ÊÇÖÜÆÚ±íÖĐÇ°ËÄÖÜÆÚµÄÔªËØ£¬ËüĂǵĺ˵çºÉÊưA£¼B£¼C£¼D£¼E¡£ÆäÖĐA¡¢B¡¢CÊÇͬ̉»ÖÜÆڵķǽđÊôÔªËØ¡£»¯ºÏÎïDCµÄ¾§̀åΪÀë×Ó¾§̀壬DµÄ¶₫¼ÛÑôÀë×ÓÓëCµÄ̉ơÀë×Ó¾ßÓĐÏàͬµÄµç×Ó²ă½á¹¹¡£AC2Ϊ·Ç¼«ĐÔ·Ö×Ó¡£B¡¢CµÄÇ⻯ÎïµÄ·Đµă±ÈËüĂÇͬ×åÏàÁÚÖÜÆÚÔªËØÇ⻯ÎïµÄ·Đµă¸ß¡£EµÄÔ×ÓĐ̣ÊưΪ24£¬ECl3ÄÜÓëB¡¢CµÄÇ⻯ÎïĐγÉÁùÅäλµÄÅäºÏÎÇ̉Á½ÖÖÅä̀åµÄÎïÖʵÄÁ¿Ö®±ÈΪ2¡Ă1£¬Èư¸öÂÈÀë×ÓλÓÚÍâ½ç¡£Çë¸ù¾ỬÔÉÏÇé¿ö£¬»Ø´đÏÂÁĐÎỀ⣺(´đ̀âʱ£¬A¡¢B¡¢C¡¢D¡¢EÓĂËù¶ÔÓ¦µÄÔªËØ·ûºÅ±íʾ)
(1)A¡¢B¡¢CµÄµÚ̉»µçÀëÄÜÓÉĐ¡µ½´óµÄ˳Đ̣Ϊ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
(2)BµÄÇ⻯ÎïµÄ·Ö×Ó¿Ơ¼ä¹¹ĐÍÊÇ¡¡¡¡¡¡¡¡¡¡¡¡ ¡£ÆäÖĐĐÄÔ×Ó²ÉÈ¡¡¡¡¡¡¡¡¡¡¡ ÔÓ»¯¡£
(3)Đ´³ö»¯ºÏÎïAC2µÄµç×Óʽ¡¡¡¡¡¡¡¡¡¡¡¡ £»̉»ÖÖÓÉB¡¢C×é³ÉµÄ»¯ºÏÎïÓëAC2»¥ÎªµÈµç×Ó̀壬Æ仯ѧʽΪ¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
(4)EµÄºËÍâµç×ÓÅŲ¼Ê½ÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡ £¬ECl3ĐγɵÄÅäºÏÎïµÄ»¯Ñ§Ê½Îª¡¡¡¡¡¡¡¡ ¡£
(5)BµÄ×î¸ß¼ÛÑơ»¯Îï¶ÔÓ¦µÄË®»¯ÎïµÄÏ¡ÈÜ̉ºÓëDµÄµ¥ÖÊ·´Ó¦Ê±£¬B±»»¹Ôµ½×îµÍ¼Û£¬¸Ă·´Ó¦µÄ»¯Ñ§·½³̀ʽÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
´đ°¸£º(12·Ö)
(1)C£¼O£¼N¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (2)Èư½Ç׶ĐΡ¡¡¡¡¡¡¡ sp3
(3)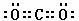 ¡¡¡¡ N2O
¡¡¡¡ N2O
(4)1s22s22p63s23p63d54s1(»̣[Ar] 3d54s1)¡¡¡¡¡¡ [Cr(NH3)4(H2O)2]Cl3
(5)4Mg+10HNO3=4Mg(NO3)2+NH4NO3+3H2O
½âÎö£ºA:»¯ºÏÎïDCµÄ¾§̀åΪÀë×Ó¾§̀壬DµÄ¶₫¼ÛÑôÀë×ÓÓëCµÄ̉ơÀë×Ó¾ßÓĐÏàͬµÄµç×Ó²ă½á¹¹£¬ÍÆÖªCΪÑơÔªËØ£¬DÎªĂ¾ÔªËØ£¬AC2Ϊ·Ç¼«ĐÔ·ÖӦΪ¶₫Ñơ»¯̀¼£¬AΪ̀¼ÔªËØ¡£B¡¢CµÄÇ⻯ÎïµÄ·Đµă±ÈËüĂÇͬ×åÏàÁÚÖÜÆÚÔªËØÇ⻯ÎïµÄ·Đµă¸ß£¬ÍƳöBµªÔªËØ£¬NH3·Ö×Ó¿Ơ¼ä¹¹ĐÍÊÇÈư½Ç׶ĐΣ¬µªÔ×Ósp3ÔÓ»¯£¬EµÄÔ×ÓĐ̣ÊưΪ24£¬ECl3ÄÜÓëB¡¢CµÄÇ⻯ÎïĐγÉÁùÅäλµÄÅäºÏÎÇ̉Á½ÖÖÅä̀åµÄÎïÖʵÄÁ¿Ö®±ÈΪ2¡Ă1£¬Èư¸öÂÈÀë×ÓλÓÚÍâ½ç£¬EΪ¸ơÔªËØ£¬¶₫Ñơ»¯̀¼·Ö×ÓÓ¦Âú×ă8µç×ÓÎȶ῭¬¡£
17£®(8·Ö)(08Äêɽ¶«Àí×Û¡¤32)[»¯Ñ§--ÎïÖʽṹÓëĐÔÖÊ]
µªÊǵØÇ̣Éϼ«Îª·á¸»µÄÔªËØ¡£
(1)Li3N¾§̀åÖеª̉ÔN3-´æÔÚ£¬»ù̀¬N3-µÄµç×ÓÅŲ¼Ê½Îª___________¡£
(2) N
 NµÄ¼üÄÜΪ942 kJ¡¤mol-1£¬N-Nµ¥¼üµÄ¼üÄÜΪ247 kJ¡¤mol-1£¬¼ÆËă˵Ă÷N2ÖеÄ___________¼ü±È____________¼üÎȶ¨(̀î¡°¦̉¡±»̣¡°¦Đ¡±)¡£
NµÄ¼üÄÜΪ942 kJ¡¤mol-1£¬N-Nµ¥¼üµÄ¼üÄÜΪ247 kJ¡¤mol-1£¬¼ÆËă˵Ă÷N2ÖеÄ___________¼ü±È____________¼üÎȶ¨(̀î¡°¦̉¡±»̣¡°¦Đ¡±)¡£
(3)(CH3)3NH+ºÍAlCl4-¿ÉĐγÉÀë×Ó̉º̀å¡£Àë×Ó̉º̀åÓÉ̉ơ¡¢ÑôÀë×Ó×é³É£¬ÈÛµăµÍÓÚ100¡æ£¬Æä»Ó·¢ĐỔ»°ă±ÈÓĐ»úÈܼÁ__________(̀î¡°´ó¡±»̣¡°Đ¡¡±)£¬¿ÉÓĂ×÷__________(̀î´úºÅ)¡£
¡¡ a£®Öúȼ¼Á
 ¡¡ b£®¡°ẦÉ«¡±ÈܼÁ
¡¡ b£®¡°ẦÉ«¡±ÈܼÁ
¡¡ c£®¸´ºÏ²ÄÁÏ
¡¡ d£®¾øÈȲÄÁÏ
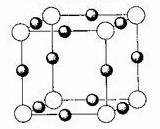
(4)X+ÖĐËùÓеç×ÓƠưºĂ³äÂúK¡¢L¡¢MÈư¸öµç×Ó²ă£¬ËüÓëN3£Đγɵľ§̀å½á¹¹ÈçͼËùʾ¡£XµÄÔªËØ·ûºÅÊÇ_____________£¬Óëͬ̉»¸öN3-ÏàÁ¬µÄX+ÓĐ__________¸ö¡£
´đ°¸£º
(1)1s22s22p6¡¡¡¡ ¡¡(2)¦Đ¡¡¡¡ ¦̉¡¡ (3)Đ¡¡¡ b¡¡¡¡ (4)Cu¡¡ 6
½âÎö£º»ù̀¬N3-µÄµç×Ó10¸ö£¬̉Ñ´ïÎȶ¨×´̀¬£¬¹ÊΪ1s22s22p6£¬¼ÆËă¿ÉÖª£¬N¡ÔNÖĐµÄ¦Đ¼üµÄ¼üÄÜΪ942 kJ¡¤mol-1¼ơÈ¥N£Nµ¥¼üµÄ¼üÄÜ247 kJ¡¤mol-1 £¬̣̉´Ë¦Đ¼ü±È¦̉¼üÎȶ¨¡£Àë×Ó̉º̀åÓÉ̉ơ¡¢ÑôÀë×Ó×é³É£¬Æä»Ó·¢ĐÔ½ÏĐ¡£¬Ç̉Î̃ÎÛȾ¡£X+ÖĐËùÓеç×ÓƠưºĂ³äÂúKLMÈư¸öµç×Ó²ă£¬Ó¦º¬ÓĐ28¸öµç×Ó£¬ỘXÔ×Óδ29¸öµç×Ó£¬XµÄÔªËØ·ûºÅÊÇCu£¬X+ ºÍN3-×é³É±ÈÀưΪ3£º1£¬¸ù¾Ư¾§̀å½á¹¹Í¼ËùʾºÚµăΪX+£¬°×µăΪN3-£¬Óëͬ̉»¸öN3-ÏàÁ¬µÄX+ÓĐ6¸ö¡£
16£®(11·Ö)(08Ä꺣ÄÏ»¯Ñ§¡¤25)ËÄÖÖÔªËØX¡¢Y¡¢Z¡¢WλÓÚÔªËØÖÜÆÚ±íµÄÇ°ËÄÖÜÆÚ£¬̉ÑÖªËüĂǵĺ˵çºÉÊửÀ´ÎÔö¼Ó£¬Ç̉ºËµçºÉÊưÖ®ºÍΪ51£»YÔ×ÓµÄL²ăp¹́µÀÖĐÓĐ2¸öµç×Ó£»ZÓëYÔ×ӵļ۲ăµç×ÓÊưÏàͬ£»WÔ×ÓµÄL²ăµç×ÓÊưÓë×îÍâ²ăµç×ÓÊưÖ®±ÈΪ4©U1£¬Æäd¹́µÀÖеĵç×ÓÊưÓë×îÍâ²ăµç×ÓÊưÖ®±ÈΪ5©U1¡£
(1)Y¡¢Z¿É·Ö±đÓëXĐγÉÖ»º¬̉»¸öÖĐĐÄÔ×ӵĹ²¼Û»¯ºÏÎïa¡¢b£¬ËüĂǵķÖ×Óʽ·Ö±đÊÇ¡¡¡¡¡¡ ¡¢¡¡¡¡¡¡ £»ÔÓ»¯¹́µÀ·Ö±đÊÇ¡¡¡¡¡¡ ¡¢¡¡¡¡¡¡ _£»a·Ö×ÓµÄÁ¢̀å½á¹¹ÊÇ¡¡¡¡¡¡ ¡£
(2)YµÄ×î¸ß¼ÛÑơ»¯ÎïºÍZµÄ×î¸ß¼ÛÑơ»¯ÎïµÄ¾§̀åÀàĐÍ·Ö±đÊÇ¡¡¡¡¡¡ ¾§̀å¡¢¡¡¡¡¡¡ ¾§̀å¡£
(3)XµÄÑơ»¯ÎïÓëYµÄÑơ»¯ÎïÖĐ£¬·Ö×Ó¼«ĐÔ½ÏĐ¡µÄÊÇ(̀î·Ö×Óʽ)¡¡¡¡¡¡ ¡£
(4)YÓëZ±È½Ï£¬µç¸ºĐԽϴóµÄ¡¡¡¡¡¡ £¬Æä+2¼ÛÀë×ӵĺËÍâµç×ÓÅŲ¼Ê½ÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
´đ°¸£º(11·Ö)(1)CH4¡¡ SiH4¡¡ sp3¡¡ sp3¡¡ ƠưËÄĂæ̀å¡¡ (2)·Ö×Ó¡¡ Ô×Ó¡¡ (3)CO2
(4)C¡¡ (5)Zn¡¡ 1s22s22p63s23p63d10
½âÎö£ºÓÉ¡°YÔ×ÓµÄL²ăp¹́µÀÖĐÓĐ2¸öµç×Ó¡±¿ÉÖªYÔ×ӵĵç×ÓÅŲ¼Ê½ÊÇ1s22s22p2£¬Îª̀¼ÔªËØ£»ÓÉ¡°ZÓëYÔ×ӵļ۲ăµç×ÓÊưÏàͬ¡±¿ÉÖªZÓë̀¼ÔªËØͬÖ÷×壬ÓỌ̈̉ZλÓÚÔªËØÖÜÆÚ±íµÄÇ°ËÄÖÜÆÚÇ̉ºËµçºÉÊư´óÓÚY£¬Ëù̉ÔZ¿ÉÄÜΪ¹èÔªËØ(14ºÅ)»̣ƠàÔªËØ(32ºÅ)£¬ÈôZΪƠàÔªËØ£¬ỘËÄÖÖÔªËصĺ˵çºÉÊưÖ®ºÍ´óÓÚ51(̣̉WµÄºËµçºÉÊư±ÈZµÄ»¹̉ª´ó)£¬¼´ZÖ»ÄÜΪ¹èÔªËØ£»ÓÉ¡°WÔ×ÓµÄL²ăµç×ÓÊưÓë×îÍâ²ăµç×ÓÊưÖ®±ÈΪ4©U1¡±¿ÉÖªWµÄ×îÍâ²ăµç×ÓÊưΪ2£¬ÓÉ¡°d¹́µÀÖеĵç×ÓÊưÓë×îÍâ²ăµç×ÓÊưÖ®±ÈΪ5©U1¡±¿ÉÖªd¹́µÀÖеĵç×ÓÊưΪ10£¬Ëù̉ÔWÔ×ӵĵç×ÓÅŲ¼Ê½ÊÇ1s22s22p63s23p63d104s2£¬¼´WÎªĐ¿ÔªËØ£»ÓỌ̈̉ËÄÖÖÔªËصĺ˵çºÉÊưÖ®ºÍΪ51£¬Ëù̉ÔXÔªËصĺ˵çºÉÊưΪ1£¬ÊÇÇâÔªËØ¡£
15£®(10·Ö)(08Äê¹ă¶«»¯Ñ§¡¤27)Ă¾¡¢ÍµÈ½đÊôÀë×ÓÊÇÈË̀åÄÚ¶àÖÖøµÄ¸¨̣̉×Ó¡£¹¤̉µÉÏ´Óº£Ë®ÖĐ̀áÈ¡Ă¾Ê±£¬ÏÈÖƱ¸Î̃Ë®ÂÈ»¯Ă¾£¬È»ºó½«ÆäÈÛÈÚµç½â£¬µĂµ½½đÊôĂ¾¡£
(1)̉ÔMgCl2ΪÔÁÏÓĂÈÛÈÚÑεç½â·¨ÖƱ¸Ă¾Ê±£¬³£¼ÓÈëNaCl¡¢KCl»̣CaCl2µÈ½đÊôÂÈ»¯ÎÆäÖ÷̉ª×÷ÓĂ³ưÁ˽µµÍÈÛµăÖ®Í⻹ÓĐ¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
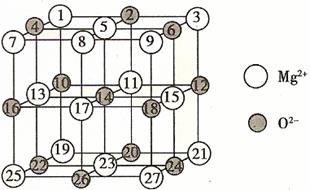
(2)̉ÑÖªMgOµÄ¾§̀å½á¹¹ÊôÓÚNaClĐÍ¡£Ä³Í¬Ñ§»³öµÄMgO¾§°û½á¹¹Ê¾̉âͼÈçÏÂͼËùʾ£¬Çë¸ÄƠưͼÖĐ´íÎ󣺡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
(3)ÓĂĂ¾·Û¡¢¼î½đÊôÑμ°¼îÍÁ½đÊôÑεȿÉ̉Ô×ö³ÉÑæ»đ¡£È¼·Åʱ£¬Ñæ»đ·¢³öÎåÑƠÁùÉ«µÄ¹â£¬ÇëÓĂÔ×ӽṹµÄ֪ʶ½âÊÍ·¢¹âµÄỘ̉£º¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
(4)MgÊǵÚÈưÖÜÆÚÔªËØ£¬¸ĂÖÜÆÚ²¿·ÖÔªËØ·ú»¯ÎïµÄÈÛµă¼ûÏÂ±í£º
|
Ñơ»¯Îï |
NaF |
MgF2 |
SiF4 |
|
ÈÛµă/K |
1266 |
1534 |
183 |
½âÊͱíÖĐ·ú»¯ÎïÈÛµă²î̉́µÄỘ̉£º¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
(5)È˹¤Ä£ÄâÊǵ±Ç°ÑĐ¾¿µÄÈÈµă¡£ÓĐÑĐ¾¿±íĂ÷£¬»¯ºÏÎïX¿ÉÓĂÓÚÑĐ¾¿Ä£Äâø£¬µ±Æä½áºÏ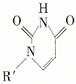 »̣Cu(I)(I±íʾ»¯ºÏ¼ÛΪ+1)ʱ£¬·Ö±đĐγÉaºÍb£º
»̣Cu(I)(I±íʾ»¯ºÏ¼ÛΪ+1)ʱ£¬·Ö±đĐγÉaºÍb£º
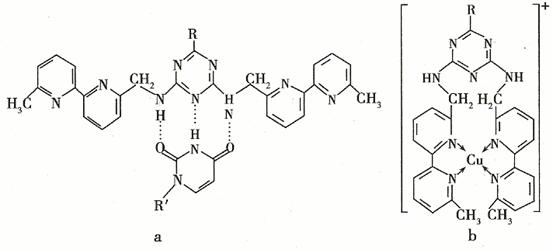
¢ÙaÖĐÁ¬½ÓÏàÁÚº¬NÔÓ»·µÄ̀¼̀¼¼ü¿É̉ÔĐưת£¬ËµĂ÷¸Ằ¼̀¼¼ü¾ßÓĐ¡¡¡¡¡¡¡¡ ¼üµÄ̀ØĐÔ¡£
¢Ú΢Á£¼äµÄÏ໥×÷ÓĂ°üÀ¨»¯Ñ§¼üºÍ·Ö×Ó¼äÏ໥×÷ÓĂ£¬±È½ÏaºÍbÖĐ΢Á£¼äÏ໥×÷ÓĂÁ¦µÄ²î̉́¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
´đ°¸£º(10·Ö)(ÎïÖʽṹѡ×ö̀â)
(1)Ôö´óÀë×ÓŨ¶È£¬´Ó¶øÔö´óÈÛÈÚÑεĵ¼µçĐÔ
(2)¢àӦΪºÚÉ«
(3)Ô×ÓºËÍâµç×Ó°´̉»¶¨¹́µÀ˳Đ̣ÅÅÁĐ£¬¹́µÀÀëºËÔ½Ô¶£¬ÄÜÁ¿Ô½¸ß¡£È¼ÉƠʱ£¬µç×Ó»ñµĂÄÜÁ¿£¬´ÓÄÜÁ¿½ÏµÍµÄ¹́µÀԾǨµ½ÄÜÁ¿½Ï¸ßµÄÁí̉»̀ơ¹́µÀ¡£Ô¾Ç¨µ½Đ¹́µÀµÄµç×Ó´¦ÔÚ̉»ÖÖ²»Îȶ¨µÄ×´̀¬£¬ËüËæ¼´¾Í»á̀ø»ØÔÀ´µÄµØÄÜÁ¿¹́µÀ£¬²¢Ị̈Íâ½çÊÍ·ÅÄÜÁ¿(¹âÄÜ)
(4)NaFÓëMgF2ΪÀë×Ó¾§̀壬SiF4Ϊ·Ö×Ó¾§̀壬Ëù̉ÔNaFÓëMgF2Ô¶±ÈSiF4ÈÛµẳª¸ß¡£ÓỌ̈̉ΪMg2+µÄ°ë¾¶Đ¡ÓÚNa+µÄ°ë¾¶£¬Ëù̉ÔMgF2µÄÀë×Ó¼üÇ¿¶È´óÓÚNaFµÄÀë×Ó¼üÇ¿¶È£¬¹ÊMaF2µÄÈÛµă´óÓÚNaF¡£
(5)¢Ù¦̉¼ü¡¡ ¢ÚaÖĐ´æÔÚÇâ¼üºÍ·¶µÂ»ªÁ¦£¬bÖĐ´æÔÚÅäλ¼ü
½âÎö£º(1)¡¡ ̉ÔMgCl2ΪÔÁÏÓĂÈÛÈÚÑεç½â·¨ÖƱ¸Mgʱ£¬³£¼ÓÈëNaCl¡¢KCl¡¢»̣CaCl2µÈ½đÊôÂÈ»¯ÎÆäÖ÷̉ª×÷ÓĂ³ưÁ˽µµÍÈÛµăÖ®Í⻹ÓĐ£ºÔö´óÀë×ÓŨ¶È£¬´Ó¶øÔö´óÈÛÈÚÑεĵ¼µçĐÔ¡£
(2)¡¡ Çë¸üƠưͼÖĐ´íÎ󣺢àӦΪºÚÉ«¡£
(3)¡¡ ÇëÓĂÔ×ӽṹµÄ֪ʶ½âÊÍ·¢¹âµÄỘ̉£ºÔ×ÓºËÍâµç×Ó°´̉»¶¨¹́µÀ˳Đ̣ÅÅÁĐ£¬¹́µÀÀëºËÔ½Ô¶£¬ÄÜÁ¿Ô½¸ß¡£È¼ÉƠʱ£¬µç×Ó»ñµĂÄÜÁ¿£¬´ÓÄÚ²à¹́µÀԾǨµ½Íâ²àµÄÁí̉»̀ơ¹́µÀ¡£Ô¾Ç¨µ½Đ¹́µÀµÄµç×Ó´¦ÔÚ̉»ÖÖ²»Îȶ¨µÄ×´̀¬£¬ËüËæ¼´¾Í»á̀ø»ØÔÀ´¹́µÀ£¬²¢Ị̈Íâ½çÊÍ·ÅÄÜÁ¿(¹âÄÜ)¡£
(4)¡¡ ½âÊͱíÖĐ·ú»¯ÎïÈÛµă²î̉́µÄỘ̉£ºNaFÓëMgF2ΪÀë×Ó¾§̀壬SiF4Ϊ·Ö×Ó¾§̀壬Ëù̉ÔNaFÓëMgF2Ô¶±ÈSiF4ÈÛµẳª¸ß¡£ÓỌ̈̉ΪMg2+µÄ°ë¾¶Đ¡ÓÚNa+µÄ°ë¾¶£¬Ëù̉ÔMgF2µÄÀë×Ó¼üÇ¿¶È´óÓÚNaFµÄÀë×Ó¼üÇ¿¶È£¬¹ÊMaF2µÄÈÛµă´óÓÚNaF¡£
(5)¡¡ ¢ÙaÖĐÁ¬½ÓÏàÁÚº¬NÔÓ»·µÄ̀¼̀¼¼ü¿É̉ÔĐưת£¬ËµĂ÷¸Ằ¼̀¼¼ü¾ßÓĐ£º¦̉¼üµÄ̀ØĐÔ¡£
¢Ú΢Á£¼äµÄÏ໥×÷ÓĂ°üÀ¨»¯Ñ§¼üºÍ·Ö×Ó¼äÏ໥×÷ÓĂ£¬±È½ÏaºÍbÖĐ΢Á£¼äÏ໥×÷ÓĂµÄ²î̉́£ºaÖĐ΢Á£¼äµÄÏ໥×÷ÓĂΪÇâ¼ü£¬bÖĐ΢Á£¼äµÄÏ໥×÷ÓĂΪÅäλ¹²¼Û¼ü¡£¡¡
35£®£Û»¯Ñ§--Ñ¡Đ̃ÎïÖʽṹÓëĐÔÖÊ£Ư(15·Ö)
(1)S¡¡ C
(2)VĐΡ¡ Ö±ÏßĐΡ¡ SO2¡¡ ̣̉ΪCO2ÊǷǼ«ĐÔ·Ö×Ó£¬SO2ºÍH2O¶¼ÊǼ«ĐÔ·Ö×Ó£¬¸ù¾Ư¡°ÏàËÆÏàÈÜ¡±ÔÀí£¬SO2ÔÚH2OÖеÄÈܽâ¶È½Ï´ó
(3)Cr¡¡ ËÄ¡¡ 1s22s22p63s23p63d54s1¡¡¡¡¡¡¡¡ +6
(4)F-H¡F¡¡ F-H¡O¡¡ O-H¡F¡¡¡¡ O-H¡O
½âÎö£º¸ù¾Ưµç×ӵĺËÍâÅŲ¼¹æÂÉ£¬ÄÜÁ¿×îµÍÔÀí£¬Ç̉XÔ×ÓºËÍâµÄM²ăÖĐÖ»ÓĐÁ½¶Ô³É¶Ôµç×Ó£¬¹ÊXΪẠ́ÔªËØ£¬YÔ×ÓºËÍâµÄL²ăµç×ÓÊưÊÇK²ăµÄÁ½±¶£¬¹²ÓĐ6¸öµç×Ó£¬YΪ̀¼ÔªËØ£¬ZÊǵؿÇÄÚº¬Á¿(ÖÊÁ¿·ÖÊư)×î¸ßµÄÔªËØΪÑơÔªËØ£¬QµÄºËµçºÉÊưÊÇXÓëZµÄºËµçºÉÊưÖ®ºÍ£¬QµÄºËµçºÉÊưΪ24£¬ÊǸơÔªËØ£¬ÔÚÔªËØÖÜÆÚ±íµÄ¸÷ÔªËØÖĐµç¸ºĐÔ×î´óµÄÊÇ·úÔªËØ¡£XZ2ÓëYZ2·Ö×ÓΪSO2¡¢CO2£¬ SO2ºÍH2O¶¼ÊǼ«ĐÔ·Ö×Ó£¬¸ù¾Ư¡°ÏàËÆÏàÈÜ¡±ÔÀí£¬SO2ÔÚH2OÖеÄÈܽâ¶È½Ï´ó¡£Ç̉H̉×ÓëO¡¢ F¡¢NĐγÉÇâ¼ü¡£
14£®[»¯Ñ§--Ñ¡Đ̃ÎïÖʽṹÓëĐÔÖÊ](15·Ö)(08ÄêÄ₫ÏÄÀí×Û¡¤35)
X¡¢Y¡¢Z¡¢Q¡¢EÎåÖÖÔªËØÖĐ£¬XÔ×ÓºËÍâµÄM²ăÖĐÖ»ÓĐÁ½¶Ô³É¶Ôµç×Ó£¬YÔ×ÓºËÍâµÄL²ăµç×ÓÊưÊÇK²ăµÄÁ½±¶£¬ZÊǵؿÇÄÚº¬Á¿(ÖÊÁ¿·ÖÊư)×î¸ßµÄÔªËØ£¬QµÄºËµçºÉÊưÊÇXÓëZµÄºËµçºÉÊưÖ®ºÍ£¬EÔÚÔªËØÖÜÆÚ±íµÄ¸÷ÔªËØÖĐµç¸ºĐÔ×î´ó¡£Çë»Ø´đÏÂÁĐÎỀ⣺
(1)X¡¢YµÄÔªËØ·ûºÅ̉À´ÎΪ¡¡¡¡¡¡¡¡¡¡ ¡¢¡¡¡¡¡¡¡¡¡¡ £»
(2)XZ2ÓëYZ2·Ö×ÓµÄÁ¢̀å½á¹¹·Ö±đÊÇ¡¡¡¡¡¡¡¡¡¡ ºÍ¡¡¡¡¡¡¡¡¡¡ £¬Ïàͬ̀ơ¼₫ÏÂÁ½ƠßÔÚË®ÖеÄÈܽâ¶È½Ï´óµÄÊÇ¡¡¡¡¡¡¡¡¡¡ (Đ´·Ö×Óʽ)£¬ÀíÓÉÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ £»
(3)QµÄÔªËØ·ûºÅÊÇ¡¡¡¡¡¡¡¡ £¬ËüÊôÓÚµÚ¡¡¡¡¡¡ ÖÜÆÚ£¬ËüµÄºËÍâµç×ÓÅŲ¼Ê½Îª¡¡¡¡¡¡¡¡¡¡ £¬ÔÚĐγɻ¯ºÏÎïʱËüµÄ×î¸ß»¯ºÏ¼ÛΪ¡¡¡¡¡¡¡¡¡¡¡¡¡¡ £»
(4)ÓĂÇâ¼ü±íÊ¾Ê½Đ´³öEµÄÇ⻯ÎïÈÜ̉ºÖĐ´æÔÚµÄËùÓĐÇâ¼ü¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
13£®(07Äêɽ¶«Àí×Û¡¤32)(8·Ö)[»¯Ñ§£ÎïÖʽṹÓëĐÔÖÊ]
ÇëÍê³ÉÏÂÁи÷̀⣺
(1)Ç°ËÄÖÜÆÚÔªËØÖĐ£¬»ù̀¬Ô×ÓÖĐδ³É¶Ôµç×ÓÓëÆäËùÔÚÖÜÆÚÊưÏàͬµÄÔªËØÓĐ¡¡¡¡ ÖÖ¡£
(2)µÚ¢óA¡¢¢ơAÔÔªËØ×é³ÉµÄ»¯ºÏÎïGaN¡¢GaP¡¢GaAsµÈÊÇÈ˹¤ºÏ³ÉµÄĐÂĐÍ°ëµ¼̀å²ÄÁÏ£¬Æ侧̀å½á¹¹Óëµ¥¾§¹èÏàËÆ¡£GaÔ×ӵĵç×ÓÅŲ¼Ê½Îª¡¡¡¡¡¡¡¡¡¡¡¡ ¡£ÔÚGaN¾§̀åÖĐ£¬Ă¿¸öGaÔ×ÓÓë¡¡¡¡¡¡ ¸öNÔ×ÓÏàÁ¬£¬Óëͬ̉»¸öGaÔ×ÓÏàÁ¬µÄNÔ×Ó¹¹³ÉµÄ¿Ơ¼ä¹¹ĐÍΪ¡¡¡¡¡¡¡¡¡¡ ¡£ÔÚËÄ´ó¾§̀åÀàĐÍÖĐ£¬GaNÊôÓÚ¡¡¡¡¡¡¡¡ ¾§̀å¡£
(3)ÔÚ¼«ĐÔ·Ö×ÓNCl3ÖĐ£¬NÔ×ӵĻ¯ºÏÎïΪ¨D3£¬ClÔ×ӵĻ¯ºÏ¼ÛΪ+1£¬ÇëÍƲâNCl3Ë®½âµÄÖ÷̉ª²úÎïÊÇ¡¡¡¡¡¡¡¡¡¡¡¡ (̀ѧʽ)¡£
¡¡ ´đ°¸£º(1)5
¡¡ (2)1s22s22p63s23p63d104s24p1(»̣[Ar]3d104s24p1)¡¡ 4¡¡ ƠưËÄĂæ̀å¡¡ Ô×Ó
¡¡ (3)HClO¡¡ NH3¡¤H2O
¡¡ ½âÎö£º(1)µÚËÄÖÜÆÚÖĐ£¬»ù̀¬Ô×ÓÖĐδ³É¶Ôµç×ÓÊưÓëÆäÖÜÆÚÊưÏàͬµÄÔªËØ°üÀ¨£ºµÚ1ÖÜÆÚµÄÇâ¡¢µÚ¶₫ÖÜÆÚµÄ̀¼ºÍÑơ¡¢µÚÈưÖÜÆÚµÄÁס¢µÚËÄÖÜÆÚµÄ̀ú£¬¹²5ÖÖ¡£
¡¡ (2)GaÔÚÔªËØÖÜÆÚ±íÖĐÊǵÚËÄÖÜÆÚ¡¢µÚ¢óA×壬Ô×ÓĐ̣ÊưÊÇ31£¬¼´ÆäÔ×ÓºËÍâµç×ÓÊưÊÇ31£¬¸ù¾ƯºËÍâµç×ÓµÄÅŲ¼¹æÂÉ¿É̉ÔĐ´³ö¸ĂÔ×ӵĵç×ÓÅŲ¼Ê½Îª£º1s22s22p63s23p63d104s24p1»̣[Ar]3d104s24p1¡£̣̉ΪGaN¾§̀å½á¹¹Óëµ¥¾§¹èÏàËÆ£¬¿ÉÖªGaN¾§̀åÊÇÔ×Ó¾§̀壬¾§̀å½á¹¹Îª¿Ơ¼äÍø×´½á¹¹£¬Ă¿¸öGaÔ×ÓÓëËĸöNÏàÁ¬£¬ƠâËĸöNÔ×Ó¹¹³ÉµÄ¿Ơ¼ä¹¹ĐÍÊÇƠưËÄĂæ̀åĐÍ¡£
¡¡ (3)Ë®½â·´Ó¦Ç°ºó¸÷ÔªËصĻ¯ºÏ¼Û²»±ä£¬ÓÉ̀ẩâÖªNCl3ÖĐNµÄ»¯ºÏ¼ÛΪ-3¼Û£¬ClµÄ»¯ºÏ¼ÛΪ+1¼Û£¬ỘÔÚNCl3Ë®½âµÄ²úÎïÖĐNµÄ»¯ºÏ¼Û̉²ÊÇ-3¼Û£¬ClµÄ»¯ºÏ¼ÛÊÇ+1¼Û£¬·ÖÎö¿ÉÖªÆäË®½â²úÎïÊÇHClOºÍNH3 ¡¤H2O ¡£
12£®(07ÄêÄ₫ÏÄÀí×Û¡¤31B)[»¯Ñ§-Ñ¡Đ̃ÎïÖʽṹÓëĐÔÖÊ]
¡¡ ̉ÑÖªA¡¢B¡¢C¡¢DºÍE 5ÖÖ·Ö×ÓËùº¬Ô×ÓÊưÄ¿̉À´ÎΪ1¡¢2¡¢3¡¢4ºÍ6£¬Ç̉¶¼º¬ÓĐ18¸öµç×Ó¡£ÓÖÖªB¡¢CºÍDÊÇÓÉÁ½ÖÖÔªËصÄÔ×Ó×é³É¡£Çë»Ø´đ£º
(1)×é³ÉA·Ö×ÓµÄÔ×ӵĺËÍâµç×ÓÅŲ¼Ê½ÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡ £»
(2)BºÍCµÄ·Ö×Óʽ·Ö±đÊÇ¡¡¡¡¡¡¡¡ ºÍ¡¡¡¡¡¡¡¡ £»C·Ö×ÓµÄÁ¢̀å½á¹¹³Ê¡¡¡¡¡¡¡¡ ĐÍ£¬¸Ă·Ö×ÓÊôÓÚ¡¡¡¡¡¡¡¡ ·Ö×Ó(̀î¡°¼«ĐÔ¡±»̣¡°·Ç¼«ĐÔ¡±)£»
(3)ÈôỊ̈DµÄÏ¡ÈÜ̉ºÖĐ¼ÓÈëÉÙÁ¿¶₫Ñơ»¯Ằ£¬ÓĐÎ̃É«Æø̀åÉú³É¡£ỘDµÄ·Ö×ÓʽÊÇ¡¡¡¡¡¡¡¡ £¬¸Ă·´Ó¦µÄ»¯Ñ§·½³̀ʽΪ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ £»
(4)Èô½«1mol EÔÚÑơÆøÖĐÍêȫȼÉƠ£¬Ö»Éú³É1mol CO2ºÍ2molH2O£¬ỘEµÄ·Ö×ÓʽÊÇ¡¡¡¡¡¡¡¡ ¡£
´đ°¸£º(1)1s22s22p63s23p6¡¡ (2)HCl¡¡ H2S¡¡ V¡¡
¼«ĐÔ¡¡¡¡¡¡ (3)H2O2¡¡ 2H2O2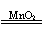
 2H2O+O2¡ü(4)CH4O
2H2O+O2¡ü(4)CH4O
½âÎö£º(1)̣̉AÓĐ18¸öµç×ÓÇ̉Ö»ÓĐ1¸öÔ×Ó£¬Ëù̉ÔAΪ18ºÅÔªËØAr£¬°´ƠƠºËÍâµç×ÓÅŲ¼¹æÂÉ¿É̉ÔĐ´³öÆäµç×ÓÅŲ¼Ê½Îª1s22s22p63s23p6 ¡£
(2)B¡¢CÁ½·Ö×Ó¾ùÓĐ2ÖÖÔªËØ×é³ÉµÄ£¬ÊÇ·Ö±đº¬ÓĐ2ºÍ3¸öÔ×ÓµÄ18µç×ӵķÖ×Ó£¬Ëù̉ÔBΪHCl£¬CΪH2S£¬H2SµÄ½á¹¹ÓëË®·Ö×ӵĽṹÏàËƾùΪ¡°V¡±Đ͵ļ«ĐÔ·Ö×Ó¡£
(3)̣̉ΪD·Ö×ÓÖĐº¬ÓĐ4¸öÔ×Ó¡¢2ÖÖÔªËØ¡¢18¸öµç×Ó£¬Ç̉ÔÚÈÜ̉ºÖĐ¼ÓÈëMnO2ºóÉú³ÉÎ̃É«Æø̀壬Ëù̉ÔDΪH2O2
¡£·´Ó¦µÄ»¯Ñ§·½³̀ʽΪ2H2O2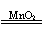
 2H2O+O2¡ü¡£
2H2O+O2¡ü¡£
(4)̣̉Ϊ1mol EÔÚÑơÆøÖĐÍêȫȼÉƠ£¬Ö»Éú³É1mol CO2ºÍ2molH2O£¬Ëù̉Ô1¸öE·Ö×ÓÖĐº¬ÓĐ1¸öCÔ×ÓºÍ4¸öHÔ×Ó¡£ÓỌ̈̉ΪE·Ö×ÓÖĐº¬ÓĐ6¸öÔ×ÓÇ̉Ϊ18µç×Ó·Ö×Ó£¬̣̉´ËEÖĐº¬ÓеÄÁí̉»¸öÔ×ÓΪOÔ×Ó¡£̣̉´ËEµÄ»¯Ñ§Ê½ÎªCH4O¡£
11£®(07Äê¹ă¶«»¯Ñ§¡¤29)(10·Ö)
C¡¢S¡¢O¡¢SeÊÇͬ×åÔªËØ£¬¸Ă×åÔªËص¥Öʼ°Æ仯ºÏÎïÔÚ²ÄÁÏ¡¢̉½̉©µÈ·½ĂæÓĐÖØ̉ªÓ¦ÓĂ¡£Çë»Ø´đÏÂÁĐÎỀ⣺
(1)GeµÄÔ×ÓºËÍâµç×ÓÅŲ¼Ê½Îª
(2)C¡¢Si¡¢SaÈưÖÖÔªËصĵ¥ÖÊÖĐ£¬Äܹ»ĐγɽđÊô¾§̀åµÄÊÇ
(3)°´̉ªÇóÖ¸³öÏÂÁĐÑơ»¯ÎïµÄ¿Ơ¼ä¹¹ĐÍ¡¢³É¼ü·½Ê½»̣ĐÔÖÊ
¢ÙCO2·Ö×ӵĿƠ¼ä¹¹Đͼ°̀¼ÑơÖ®¼äµÄ³É¼ü·½Ê½¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ £»
¢ÚSO2¾§̀åµÄ¿Ơ¼ä¹¹Đͼ°¹èÑơÖ®¼äµÄ³É¼ü·½Ê½¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ £»
¢Û̉ÑÖªSnO2ÊÇÀë×Ó¾§̀å£¬Đ´³öÆäÖ÷̉ªÎïÀíĐÔÖÊ¡¡¡¡¡¡¡¡¡¡¡¡ (Đ´³ö2̀ơ¼´¿É)
(4)CO¿É̉Ժͺܶà½đÊôĐγÉÅäºÏÎÈçNi(CO)2£¬NiÓëCOÖ®¼äµÄ¼üĐÍΪ
(5)̀¼Ñơ¼üµÄº́ÍâÉ́ËơƠñ¶¯ÆµÂÊÓë¼üµÄÇ¿¶È³ÉƠư±È£¬̉ÑÖªNi(CO)4ÖĐ̀¼Ñơ¼üµÄÉ́ËơƠñ¶¯ÆµÂÊΪ2060cm£3£¬CO·Ö×ÓÖĐ̀¼Ñơ¼üµÄÉ́ËơƠñ¶¯ÆµÂÊΪ2143cm£2£¬ỘNi(CO)ÖĐ̀¼Ñơ¼üµÄÇ¿¶È±ÈCO·Ö×ÓÖĐ̀¼Ñơ¼üµÄÇ¿¶È¡¡¡¡ (̀î×Öĸ)
A£®Ç¿¡¡¡¡
B£®Èơ¡¡¡¡
C£®ÏàµÈ¡¡¡¡
D£®Î̃·¨ÅжÏ
´đ°¸£º(10·Ö)
(1)1s22s22p63s23p63d104s24p2
(2)Sn
(3)¢ÙÖ±ÏßĐÍ¡¡ ¹²¼Û¼ü(»̣¦Á¼üÓë¦Đ¼ü)¢ÚSi=Oͨ¹ư¹²¼Û¼üĐγÉËÄĂæ̀å½á¹¹£¬ËÄĂæ̀åÖ®¼äͨ¹ư¹²¼Û¼üĐγɿƠ¼äÍø×´½á¹¹¹²¼Û¼ü(»̣¦Á¼ü)¢ÛÈÛÈÚʱÄܵ¼µç¡¢½Ï¸ßµÄÈÛµă
(4)Åäλ¼ü
(5)B
½âÎö£º¿¼²éѧÉú¶ÔÔ×ӽṹºÍÔ×ÓºËÍâµç×ÓÅŲ¼µÄÁ˽⣬¶Ô³£¼ûÎïÖÊ¿Ơ¼ä¹¹Đͺͻ¯Ñ§¼üÓëÎïÖÊĐÔÖʵÄÁ˽⣬̉Ô¼°¶ÔÔ×Ó¾§̀å¡¢½đÊô¾§̀å¡¢¼̣µ¥ÅäºÏÎïµÄ½á¹¹µÄÁ˽âºÍ¶ÔÀë×Ó¼üĐγɵÄÀí½â£¬¿¼²éѧÉúµÄ¹éÄÉÍÆÀíÄÜÁ¦¡¢ĐÅϢǨ̉ÆÄÜÁ¦¼°Æä×ÛºÏÓ¦ÓĂÄÜÁ¦¡£
10£®(11·Ö)(2007º£ÄÏ¡¤25)A¡¢B¡¢C¡¢D¡¢E´ú±í5ÖÖÔªËØ¡£Çë̀î¿Ơ£º
(1)AÔªËØ»ù̀¬Ô×ÓµÄ×îÍâ²ăÓĐ3¸öδ³É¶Ôµç×Ó£¬´ÎÍâ²ăÓĐ2¸öµç×Ó£¬ÆäÔªËØ·ûºÅΪ¡¡¡¡¡¡¡¡¡¡ ¡¡ £»
(2)BÔªËصĸº̉»¼ÛÀë×ÓºÍCÔªËصÄƠử»¼ÛÀë×ӵĵç×Ó²ă½á¹¹¶¼Óëë²Ïàͬ£¬BµÄÔªËØ·ûºÅΪ¡¡¡¡¡¡¡¡¡¡¡¡ £¬CµÄÔªËØ·ûºÅΪ¡¡¡¡¡¡¡¡¡¡ ¡¡ £»
(3)DÔªËصÄƠưÈư¼ÛÀë×ÓµÄ3dÑDzăΪ°ë³äÂú£¬DµÄÔªËØ·ûºÅΪ¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡£¬Æä»ù̀¬Ô×ӵĵç×ÓÅŲ¼Ê½Îª¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡ ¡£
(4)EÔªËØ»ù̀¬Ô×ÓµÄM²ăÈ«³äÂú£¬N²ăĂ»ÓĐ³É¶Ôµç×Ó£¬Ö»ÓĐ̉»¸öδ³É¶Ôµç×Ó£¬EµÄÔªËØ·ûºÅΪ¡¡¡¡¡¡¡¡¡¡ ¡¡ £¬Æä»ù̀¬Ô×ӵĵç×ÓÅŲ¼Ê½Îª¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
¡¡´đ°¸£º(1)N(2)Cl¡¡ K(3)Fe¡¡ 1s22s22p63s23p63d64s2
(4)¡¡ Cu¡¡ 1s22s22p63s23p63d104s1
¿¼µă£º±¾̀⿼²éÁ˳£¼ûÔªËØÖÖÀàÍƶÏ̉Ô¼°Ô×ӽṹ¡£
½âÎö£º(1)AÔªËØÔ×ÓºËÍâ¹²ÓĐ5¸öµç×Ó£¬ỘºËÄÚΪ5¸öÖÊ×Ó£¬̣̉´ËΪN¡£(2)B¡¢C·Ö±đΪ17¡¢19ºÅÔªËؼ´Cl¡¢K¡£(3)D3+µÄµç×ÓÅŲ¼Ê½Îª1s22s22p63s23p63d5£¬¿ÉÖªDΪ26ºÅÔªËØ£¬¼´Fe£¬̣̉´ËÆä»ù̀¬Ô×ӵĵç×ÓÅŲ¼Ê½Îª1s22s22p63s23p63d64s2¡£(4)EÔªËØÔ×ÓºËÍâ¹²ÓĐ29¸öµç×Ó£¬¼´µÚ29ºÅÔªËØΪCu£¬µç×ÓÅŲ¼Ê½Îª1s22s22p63s23p63d104s1¡£
¹ú¼ÊÑ§Đ£ÓÅÑ¡ - Á·Ï°²áÁбí - ÊỒâÁбí
º₫±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨Æ½̀¨ | ÍøÉÏÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | µçĐÅƠ©Æ¾Ù±¨×¨Çø | ÉæÀúÊ·ĐéÎ̃Ö÷̉åÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com