
16.(09山东卷28)运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义。
 (1)合成氨反应反应N2(g)+3H2(g)
(1)合成氨反应反应N2(g)+3H2(g) 2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡 移动(填“向左”“向右”或“不”);,使用催化剂 反应的ΔH(填“增大”“减小”或“不改变”)。
2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡 移动(填“向左”“向右”或“不”);,使用催化剂 反应的ΔH(填“增大”“减小”或“不改变”)。
 (2)O2 (g)= O+2(g)+e-
(2)O2 (g)= O+2(g)+e-  H1= 1175.7 kJ·mol-1
H1= 1175.7 kJ·mol-1
 PtF6(g)+ e-1
PtF6(g)+ e-1  PtF6-(g)
PtF6-(g)  H2= - 771.1 kJ·mol-1
H2= - 771.1 kJ·mol-1
 O2+PtF6-(s)=O2+(g)+PtF6-
O2+PtF6-(s)=O2+(g)+PtF6-
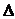 H3=482.2 kJ·mol-1
H3=482.2 kJ·mol-1
 则反应O2(g)+ PtF6 (g) = O2+PtF6-
(s)的
则反应O2(g)+ PtF6 (g) = O2+PtF6-
(s)的 H=_____________ kJ·mol-1。
H=_____________ kJ·mol-1。
 (3)在25℃下,向浓度均为0.1 mol·L-1的MgCL2和CuCl2混合溶液中逐滴加入氨水,先生成__________沉淀(填化学式),生成该沉淀的离子方程式为____________。已知25℃时Ksp[Mg(OH)2]=1.8×10-11,KsP[Cu(OH)2]=2.2×10-20。
(3)在25℃下,向浓度均为0.1 mol·L-1的MgCL2和CuCl2混合溶液中逐滴加入氨水,先生成__________沉淀(填化学式),生成该沉淀的离子方程式为____________。已知25℃时Ksp[Mg(OH)2]=1.8×10-11,KsP[Cu(OH)2]=2.2×10-20。
 (4)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH4*)=c(Cl-),则溶液显_____________性(填“酸”“碱”或“中”);用含a的代数式表示NH3·H2O的电离常数Kb=__________。
(4)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH4*)=c(Cl-),则溶液显_____________性(填“酸”“碱”或“中”);用含a的代数式表示NH3·H2O的电离常数Kb=__________。
 [解析](1)在恒压条件下加入氩气,则容积增大,导致原平衡中各物质的浓度同等比例减小,所以平衡向气体体积增大的方向即向左移动;催化剂仅是改变化学反应速率,不会影响焓变21世纪教育网
[解析](1)在恒压条件下加入氩气,则容积增大,导致原平衡中各物质的浓度同等比例减小,所以平衡向气体体积增大的方向即向左移动;催化剂仅是改变化学反应速率,不会影响焓变21世纪教育网
(2)根据盖斯定律,将化学方程式①+②-③叠加。
(3)Cu(OH)2 的Ksp小于Mg(OH)2的,所以离子的浓度商首先大于Cu(OH)2 的而先沉淀;由于氨水是弱碱,书写离子方程式时不能拆开21世纪教育网
(4)由溶液的电荷守恒可得: c(H*)+c(NH4*)=c(Cl-)+c(OH-),已知c(NH4*)=c(Cl-),则有c(H*)=c(OH-),溶液显中性;电离常数只与温度有关,则此时NH3·H2O的电离常数
Kb=[c(NH4*)·c(OH-)]/c(NH3·H2O)= (0.01 mol·L-1·10-7mol·L-1)/(amol·L-1-0.01 mol·L-1)= 10-9/( (a-0.01)mol·L-1.
 [答案](1)向左 不改变
(2)-77.6
[答案](1)向左 不改变
(2)-77.6
(3)Cu(OH)2 Cu2++2NH3·H2O=Cu(OH)2 ↓+2NH4+
 (4)中 Kb=10-9/(
(a-0.01)mol·L-1.
(4)中 Kb=10-9/(
(a-0.01)mol·L-1.
[考点分析]本题考查学生盖斯定律的应用能力和电离常数的计算。
15.(09全国卷Ⅰ28)s下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极。
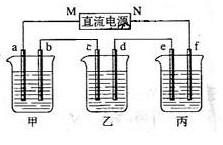
(1)接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加。据此回答问题:
①电源的N端为 极; ②电极b上发生的电极反应为 ;
③列式计算电极b上生成的气体在标准状态下的体积: ;
④电极c的质量变化是 g;
⑤电解前后各溶液的酸、碱性大小是否发生变化,简述其原因:
甲溶液 ;
乙溶液 ;
丙溶液 ;
(2)如果电解过程中铜全部析出,此时电解能否继续进行,为什么?
[解析](1)①乙中C电极质量增加,则c处发生的反应为:Cu2++2e-=Cu,即C处为阴极,由此可推出b为阳极,a为阴极,M为负极,N为正极。丙中为K2SO4,相当于电解水,设电解的水的质量为xg。由电解前后溶质质量相等有,100×10%=(100-x)×10.47%,得x=4.5g,故为0.25mol。由方程式2H2+O2
 2H2O可知,生成2molH2O,转移4mol电子,所以整个反应中转化0.5mol电子,而整个电路是串联的,故每个烧杯中的电极上转移电子数是相等的。②甲中为NaOH,相当于电解H2O,阳极b处为阴离子OH-放电,即4OH--4e-=2H2O + O2↑。③转移0.5mol电子,则生成O2为0.5/4=0.125mol,标况下的体积为0.125×22.4=2.8L。④Cu2++2e-=Cu,转移0.5mol电子,则生成的m(Cu)=0.5/2 ×64 =16g。⑤甲中相当于电解水,故NaOH的浓度增大,pH变大。乙中阴极为Cu2+放电,阳极为OH-放电,所以H+增多,故pH减小。丙中为电解水,对于K2SO4而言,其pH几乎不变。(2)铜全部析出,可以继续电解H2SO4,有电解液即可电解。
2H2O可知,生成2molH2O,转移4mol电子,所以整个反应中转化0.5mol电子,而整个电路是串联的,故每个烧杯中的电极上转移电子数是相等的。②甲中为NaOH,相当于电解H2O,阳极b处为阴离子OH-放电,即4OH--4e-=2H2O + O2↑。③转移0.5mol电子,则生成O2为0.5/4=0.125mol,标况下的体积为0.125×22.4=2.8L。④Cu2++2e-=Cu,转移0.5mol电子,则生成的m(Cu)=0.5/2 ×64 =16g。⑤甲中相当于电解水,故NaOH的浓度增大,pH变大。乙中阴极为Cu2+放电,阳极为OH-放电,所以H+增多,故pH减小。丙中为电解水,对于K2SO4而言,其pH几乎不变。(2)铜全部析出,可以继续电解H2SO4,有电解液即可电解。
[答案](1)①正极 ②4OH--4e-=2H2O + O2↑。③2.8L ④16g ⑤甲增大,因为相当于电解水;乙减小,OH-放电, H+增多。丙不变,相当于电解水。
(2)可以 因为CuSO4溶液已转变为H2SO4溶液,反应也就变为水的电解反应
考点分析:本题以电化学知识点为背景,考查学生质量守恒的应用、电子得失守恒的应用能力21世纪教育网
14. (上海市2009届高三年级上学期十四校联考)根据有关信息:21世纪教育网
2SO2(g)+O2(g) 2SO3(g)+196.7KJ;某种硝酸钙晶体可表示为Ca(NO3)2·8H2O;25℃时NaHCO3的溶解度为9.6g/100g水;空气中氧气的体积分数为21%,判断下列有关数据正确的是
A.室温下,配制2.5mol/L的NaHCO3溶液
B.爆炸最强烈的坑道气中甲烷的体积分数为10.5%
C.用1molSO2气体与足量氧气反应放出的热量为98.35KJ
D.与CaO作用直接制Ca(NO3)2·8H2O所用硝酸的质量分数为50%
[解析]25℃时NaHCO3的溶解度为9.6g/100g水,则n(NaHCO3)mol/0.1L=9.6/106mol÷0.1L<1mol/L,A错;10.5:89.5×21%=1:1.8,CH4+2O2=CO2+2H2O,B错;C错,因为1molSO2气体不能完全反应;50/(63×2):[50/18+50/(63×2)]=1:8,D正确;
[答案]D
[考点分析]本题考查学生通过溶解度计算物质的量浓度、体积分数、热量、质量分数的能力21世纪教育网
13. (08四川理综13)在a L Al2(SO4)3和(NH4)2SO4的混合溶液中加入b mol BaCl2,恰好使溶液中的SO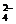 离子完全沉淀;如加入足量强碱并加热可得到c mol NH3气,则原溶液中的Al3+离子浓度(mol/L)为
( )
离子完全沉淀;如加入足量强碱并加热可得到c mol NH3气,则原溶液中的Al3+离子浓度(mol/L)为
( )
A.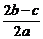 B.
B. C.
C. D.
D.
[解析]由于产生c mol NH3,则必定有NH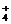 c mol,使SO
c mol,使SO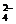 完全沉淀需Ba2+ b
mol,因此SO
完全沉淀需Ba2+ b
mol,因此SO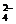 有b mol。根据电荷守恒:2 c (SO
有b mol。根据电荷守恒:2 c (SO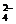 )= c (NH
)= c (NH )+3c (Al3+),则3c (Al3+)=
)+3c (Al3+),则3c (Al3+)=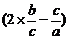 mol/L
mol/L
c(Al3+)= mol/L
mol/L
[答案]C
[考点分析]本题考查溶液中离子浓度的计算。
2.7 g,n(H2O)=0.15 mol,可知有机物样品平均分子式中n(C)∶n(H)=1∶3,由含氧衍生物分子式分析:若是纯净物,则分子式必为C2H6Ox,排除B、C;由3.1 g完全燃烧生成7.1 g CO2和H2O可知耗O2为4 g,代入乙二醇检验,恰好符合,A正确,乙二醇分子式可以改写为C2H2(H2O)2,D中甲醇可改写为CH2(H2O)、丙三醇可改写为C3H2(H2O)3,由分子式可知甲醇和丙三醇按1∶1比例混合后平均分子式恰好为C2H2(H2O)2,故符合题意。
[答案]AD
[考点分析]本题考查学生通过有机物的燃烧确认有机物化学式的计算能力。
12. (08江苏14)某有机物样品3.1 g完全燃烧,燃烧后的混合物通入过量的澄清石灰水,石灰水共增重7.1 g,经过滤得到10 g沉淀。该有机样品可能是 ( )
A.乙二醇 B.乙醇 C.乙醛 D.甲醇和丙三醇的混合物
[解析]由10 g CaCO3沉淀可知燃烧生成0.1 mol CO2(4.4 g),生成m (H2O)=7.1 g-4.4 g=
11.(09宁夏卷 13)在一定温度下,反应1/2H2(g)+ 1/2X2(g)
13)在一定温度下,反应1/2H2(g)+ 1/2X2(g) 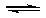 HX(g)的平衡常数为10。若将1.0mol的HX(g)通入体积为1.0L的密闭容器中,在该温度时HX(g)的最大分解率接近于
HX(g)的平衡常数为10。若将1.0mol的HX(g)通入体积为1.0L的密闭容器中,在该温度时HX(g)的最大分解率接近于
 A.5%
B.17%
C.25%
D.33%
A.5%
B.17%
C.25%
D.33%

 [解析]1/2H2(g)+
1/2X2(g)
[解析]1/2H2(g)+
1/2X2(g) 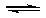 HX(g)的平衡常数K1为10,那么HX(g)
HX(g)的平衡常数K1为10,那么HX(g) 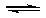 1/2H2(g)+ 1/2X2(g)
的平衡常数K2为1/10, 2HX(g)
1/2H2(g)+ 1/2X2(g)
的平衡常数K2为1/10, 2HX(g) 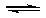 H2(g)+ X2(g) 的平衡常数K3为(1/10)2=0.01.设HX(g)分解xmol/L,有, 2HX(g)
H2(g)+ X2(g) 的平衡常数K3为(1/10)2=0.01.设HX(g)分解xmol/L,有, 2HX(g) 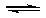 H2(g)+ X2(g)
H2(g)+ X2(g)
 1
0 0
1
0 0
 x
x x
x
x x
 1-x
x x
1-x
x x
 K3= x·x/(1-x)
2= 0.01 ,得到x=0.17,所以, 该温度时HX(g)的最大分解率接近于B. 17%
K3= x·x/(1-x)
2= 0.01 ,得到x=0.17,所以, 该温度时HX(g)的最大分解率接近于B. 17%
 [答案]B
[答案]B
[考点分析]本题考查学生借助于平衡常数计算物质转化率的能力。
10.(09江苏卷 4) 用NA表示阿伏加德罗常数的值。下列叙述正确的是w .
4) 用NA表示阿伏加德罗常数的值。下列叙述正确的是w .
 A.25℃时,PH=13的1.0L Ba(OH)2溶液中含有的
A.25℃时,PH=13的1.0L Ba(OH)2溶液中含有的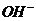 数目为0.2NA
数目为0.2NA
 B.标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA
B.标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA
 C.室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA
C.室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA
 D.标准状况下,22.4L 甲醇中含有的氧原子数为1.0NA
D.标准状况下,22.4L 甲醇中含有的氧原子数为1.0NA
[解析]A.PH=13也就是意味着 ,则
,则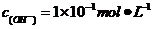 ,所以
,所以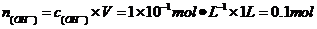 ,所以
,所以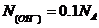 ;
;
B.发生的化学反应方程式为 (该反应为歧化反应),
(该反应为歧化反应), ,那么转移电子的数目应该为
,那么转移电子的数目应该为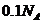 ;
;
C.乙烯和丁烯的最简式都是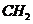 ,则
,则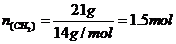 ,所以
,所以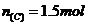 ,
, ;
;
D.标准状况下,甲醇为液态,那么甲醇的物质的量就不是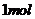 ,则所含有的氧原子个数也不为
,则所含有的氧原子个数也不为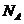 21世纪教育网
21世纪教育网
[答案]C
[考点分析]本题借助于阿伏伽德罗常数的计算考查溶液中离子数、转移电子数、混合气体中原子个数以及气体摩尔体积的应用21世纪教育网
9.(09全国卷Ⅱ 11) 已知:2H2(g)+ O2(g)=2H2O(l) ΔH= -571.6KJ· mol-1
11) 已知:2H2(g)+ O2(g)=2H2O(l) ΔH= -571.6KJ· mol-1

 CH4(g)+ 2O2(g)=CO2(g)+2H2O(l) ΔH= -890KJ· mol-1
CH4(g)+ 2O2(g)=CO2(g)+2H2O(l) ΔH= -890KJ· mol-1

 现有H2与CH4的混合气体112L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3695KJ,则原混合气体中H2与CH4的物质的量之比是
现有H2与CH4的混合气体112L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3695KJ,则原混合气体中H2与CH4的物质的量之比是

 A.1∶1 B.1∶3
A.1∶1 B.1∶3 
 C.1∶4
D.2∶3
C.1∶4
D.2∶3
[解析]设H2、CH4的物质的量分别为x、ymol。则x + y =5,571.6x/2 + 890y = 3695,解得x=1.25mol; y=3.75mol,两者比为1:3,故选B项。
[答案]B
[考点分析]本题考查化学反应中能量变化的计算。
8.(09全国卷Ⅰ9)现有乙酸和两种链状单烯烃混合物,其中氧的质量分数为a,则碳的质量分数是
A.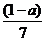 B.
B. C.
C.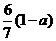 D.
D.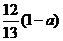
[解析]乙酸的化学式为C2H4O2,而单烯烃的通式为CnH2n,从化学式可以发现两者中,C与H之间的数目比为1:2,质量比为6:1,碳氢的质量分数一共为1-a,其中碳占 。
。
[答案]C
[考点分析]本题考查有机物中元素质量分素的计算。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com