
题目列表(包括答案和解析)
28.(12分)有关元素A、B、C、D的信息如下:
|
元
素 |
有关信息 |
|
A |
最高价氧化物对应的水化物(甲)能与其气态氢化物(乙)反应生成盐 |
|
B |
地壳中含量最高的元素,A与B可形成一种质量比为 7:12的化合物(丙) |
|
C |
单质曾用于焊接钢轨 |
|
D |
单质是生活中常见金属,其制品在自然环境中被腐蚀呈现红棕色 |
请回答下列问题:
(1)用C单质来焊接钢轨的化学方程式是 。
(2)有关C与D元素,下列说法正确的是 (填序号)。
①C或D的高价盐均可用做净水剂
②用C或D单质做成的槽车,都可用来运输甲的稀溶液
③C、D的单质与稀硫酸组成的原电池,C电极发生氧化反应
④C的合金可用来做车船材料和门窗等
(3)B的一种氢化物在碱性溶液中可与丙反应,生成物中A元素只显其最高价态,该反应的离子方程式是 。
(4)现取1 mol·L-1 100 mL的C的氯化物溶液,向其中加入1 mol·L-1氢氧化钠溶液产生了3.9 g的沉淀,则加入的氢氧化钠溶液体积可能是 mL。
 (5)已知:2AB2(g)
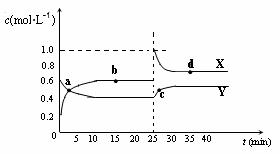
(5)已知:2AB2(g) A2B4(g);△H<0。在恒温恒容条件下,将一定量AB2和A2B4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如右图所示。
A2B4(g);△H<0。在恒温恒容条件下,将一定量AB2和A2B4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如右图所示。
①a、b、c、d四个点中,化学反应处于平衡状态的是 点。
②a、b、c、d四个点中所表示的反应体系中,气体颜色由深到浅的顺序是 (填字母)。
15.下列表格中的各种情况,可以用下面的图像曲线表示的是
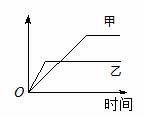
|
|
反应 |
纵坐标 |
甲 |
乙 |
|
A |
相同质量的氨,在同一容器中 2NH3 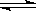 N2
+ 3H2 N2
+ 3H2 |
氨气的转化率 |
500℃ |
400℃ |
|
B |
等质量钾、钠分别与足量水反应 |
H2质量 |
钠 |
钾 |
|
C |
在体积可变的恒压容器中,体积比1:3的N2、H2, N2 + 3H2 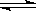 2NH3 2NH3 |
氨气的浓度 |
活性高的 催化剂 |
活性一般的 催化剂 |
|
D |
2
molSO2和1 molO2,在相同温度下2SO2 + O2 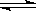 2SO3 2SO3 |
SO3物质的量 |
2个大气压 |
10个大气压 |
14.下列各项中的两个量,其比值一定为2:1的是
A.液面在“0”刻度时,50 mL碱式滴定管和25 mL碱式滴定管所盛溶液的体积
B.相同温度下,pH = 1和pH = 2的硫酸溶液中的c(H+)
C.在过氧化钠固体中,阳离子和阴离子的个数
D.加热条件下,浓硫酸与碳反应中,参加反应的硫酸与被还原的硫酸的个数
13.在25 ℃时,将两个铂电极插入一定量饱和Na2SO4溶液中进行电解,通电一段时间后,在阳极上放出a mol气体,同时有w g Na2SO4·10H2O晶体析出。若温度不变,此时剩余溶液中溶质的质量分数为
12.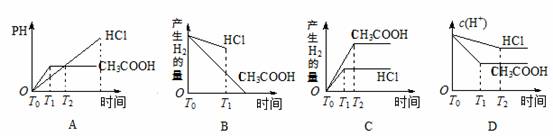 在体积都为1L,pH都等于2的盐酸和醋酸溶液中,投入0.65 g锌粒,则图示比较符合客观事实的是
在体积都为1L,pH都等于2的盐酸和醋酸溶液中,投入0.65 g锌粒,则图示比较符合客观事实的是
11.下列叙述中正确的是
A.通常情况下,乙烯、乙醇、乙酸、乙酸乙酯都易发生取代反应
B.橡胶、蛋白质和纤维素都是天然高分子化合物
C.碘水和新制的Cu(OH)2悬浊液都可以鉴别葡萄糖溶液和淀粉溶液
D.将绕成螺旋状的铜丝插入酒精中,加热酒精可实现乙醇的催化氧化
10.设NA表示阿伏加德罗常数的值,下列叙述中正确的是
A.1 L0.1 mol·L-1的CH3COONa溶液中CH3COO-的总数是0.1NA
B.常温常压下,1.6 gO2和O3混合气体中质子总数为0.8NA
C.一定条件下,2 molSO2和1 molO2发生反应,转移的电子总数一定是2NA
D.1L0.1mol·L-1的葡萄糖溶液中分子总数为0.1NA
9.下列有关环境问题的叙述正确的是
A.赤潮、白色污染、绿色食品都与相关物质的颜色有关
B.5·12汶川大地震发生后,灾区急需大量消毒剂,其中SO2可用于环境消毒
C.利用太阳能等清洁能源代替化石燃料,有利于节约能源,保护环境
D.我国禁止汽车使用含铅汽油,其主要原因是铅资源短缺
1.化学在环境监测中越来越显示其重要作用,水体受还原性物质(主要是有机物)污染的程度常用化学需氧量(COD)来衡量。COD是指在一定条件下,用强氧化剂处理一定体积水样时所消耗的强氧化剂相当于氧气的质量,单位用mg/L表示。
重铬酸钾法是指在强酸性溶液中,用一定量的重铬酸钾氧化(以Ag+作催化剂)水样中的还原性物质,其本身被还原为Cr3+,过量的重铬酸钾以试亚铁灵作指示剂、用硫酸亚铁铵溶液回滴,根据相关试剂的用量即可求出水样的化学需氧量(COD)。
请回答下列问题:
(1)当水样中含有浓度较高的Cl-时,常需加入HgSO4溶液,则HgSO4的作用及可能原因是 。
(2)滴定时硫酸亚铁铵溶液需盛放在 (填“酸”或“碱”)式滴定管中。
(3)国家《生活饮用水标准检验法(GB5750-85)》中酚类的检测下限为0.002 mg/L。某水源受化工厂污染,酚含量达0.282 mg/L,该污染的水样中酚(以苯酚氧化成CO2
计算)引起的化学需氧量(COD)为 mg/L。
(4)某化工园区有两家企业排放出的废水中,某次COD测量值高达2100 mg/L,这两家企业最有可能是 。(填字母)
a.制糖厂 b.水泥厂 c.电镀厂 d.造纸厂
(5)现有某废水样品10.00 mL,先加入10 mL蒸馏水,然后加入10.00 mL 0.04000 mol/L K2Cr2O7溶液、3 mL 1%硫酸-硫酸银溶液、17 mL硫酸汞溶液,加热反应2 h。在试亚铁灵指示剂存在下用0.1000 mol/L Fe(NH4)2(SO4)2溶液滴定多余的K2Cr2O7,共用去Fe(NH4)2(SO4)2溶液12.00 mL。试计算该水样的化学需氧量(COD)。
14.某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度均相同)。
|
|
50 mL盐酸 |
50 mL盐酸 |
50 mL盐酸 |
|
m(混合物) |
9.2
g |
15.7
g |
27.6
g |
|
V(CO2)(标准状况) |
2.24
L |
3.36
L |
3.36
L |
下列分析与推理错误的是
A.加入混合物9.2 g时,盐酸为过量
B.盐酸的物质的量浓度为3.0 mol/L
C.15.7 g混合物恰好与盐酸完全反应
D.根据表中数据不能计算出混合物中NaHCO3的质量分数
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com