
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
22ЃЎЯТСаЫЕЗЈе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁЁЁ AЃЎ0.2molЁЄL-1ЕФДзЫсФЦШмвКжаЃЌc(Na+)ЃНc(CH3COO- )
ЁЁЁЁЁЁЁЁ BЃЎЪвЮТЯТЃЌpHЃН3бЮЫсКЭpHЃН11ЕФАБЫЎЕШЬхЛ§ЛьКЯКѓЕФШмвКpHаЁгк7
ЁЁЁЁЁЁЁЁ CЃЎЯђТШЛЏФЦШмвКжаЕЮМгЯЁЯѕЫсЕУЕНpHЃН5ЕФЛьКЯШмвКжаЃЌc(Na+)ЃНc(Cl-)
ЁЁЁЁЁЁЁЁ DЃЎ0.1molЁЄL-1ЕФЬМЫсФЦШмвКжаЃЌc(H+)Ѓc(OH-)ЃНc(CO32-)+c(H2CO3)
21ЃЎЖдгкЬхЛ§ЯрЭЌЕФЂй(NH4)2SO4ЁЂЂкNH4HSO4ЁЂЂлH2SO4ШмвКЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ(ЁЁЁЁ )
ЁЁЁЁЁЁЁЁ AЃЎШмвКЕФpHЯрЭЌЪБЃЌ3жжШмвКЮяжЪЕФСПХЈЖШДѓаЁЫГађЪЧЂлЃОЂкЃОЂй
ЁЁЁЁЁЁЁЁ BЃЎШмвКЕФpHЯрЭЌЪБЃЌНЋ3жжШмвКЯЁЪЭЯрЭЌБЖЪ§ЃЌpHБфЛЏзюДѓЕФЪЧЂй
ЁЁЁЁЁЁЁЁ CЃЎШмвКЕФpHЯрЭЌЪБЃЌгЩЫЎЕчРыГіЕФc(H+)ДѓаЁЫГађЪЧЂлЃОЂкЃОЂй
ЁЁЁЁЁЁЁЁ DЃЎШє3жжШмвКЕФЮяжЪЕФСПХЈЖШЖМЯрЭЌЃЌдђШмвКЕФpHДѓаЁЫГађЪЧЂйЃОЂкЃОЂл
20ЃЎИпЬњЕчГиЪЧвЛжжаТаЭПЩГфЕчЕчГиЃЌгыЦеЭЈИпФмЕчГиЯрБШЃЌИУЕчГиФмГЄЪБМфБЃГжЮШЖЈЕФЗХЕчЕчбЙЁЃИпЬњЕчГиЕФзмЗДгІЮЊЃК
3Zn + 2K2FeO4 ЁЁ+ 8H2O 3Zn(OH)2 + 2Fe(OH)3 ЁЁ+ 4KOH ЁЃЯТСаа№ЪіВЛе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
3Zn(OH)2 + 2Fe(OH)3 ЁЁ+ 4KOH ЁЃЯТСаа№ЪіВЛе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁЁЁ AЃЎЗХЕчЪБаПзіИКМЋЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁЁЁ BЃЎГфЕчЪБЧтбѕЛЏЬњБЛбѕЛЏ
ЁЁЁЁЁЁЁЁ CЃЎГфЕчЪБЕчГиЕФе§МЋКЭЕчдДЕФе§МЋЯрСЌЁЁЁЁЁЁ
ЁЁЁЁЁЁЁЁ DЃЎЗХЕчЪБУПзЊвЦ3 mole-ЃЌга2mol FeO42-БЛЛЙд
19ЃЎЪвЮТЯТЃЌвЛдЊЫсHAШмвКгывЛдЊМюBOHШмвКЕШЬхЛ§ЛьКЯЃЌЯТСагаЙиХаЖЯе§ШЗЕФЪЧ(ЁЁЁЁ )
ЁЁЁЁЁЁЁЁ AЃЎШєЛьКЯКѓЫљЕУШмвКГЪжаадЃЌдђHAПЯЖЈЪЧЧПЫсЁЂBOHПЯЖЈЪЧЧПМю
ЁЁЁЁЁЁЁЁ BЃЎШєЛьКЯЧАЫсЁЂМюpHжЎКЭЕШгк14ЃЌЛьКЯКѓЫљЕУШмвКГЪМюадЃЌдђBOHПЯЖЈЪЧШѕМю
ЁЁЁЁЁЁЁЁ CЃЎШєЛьКЯЧАЫсЁЂМюЮяжЪЕФСПХЈЖШЯрЭЌЃЌЛьКЯКѓЫљЕУШмвКГЪЫсадЃЌдђHAПЯЖЈЪЧШѕЫс
ЁЁЁЁЁЁЁЁ DЃЎШєЛьКЯКѓЫљЕУШмвКГЪЫсадЃЌдђЛьКЯШмвКжаРызгХЈЖШвЛЖЈТњзу
ЁЁЁЁ ЁЁЁЁc(B+)ЃОc(A-)ЃОc(H+)ЃОc(OHЃ)
18ЃЎ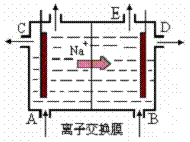 гвЭМЮЊбєРызгНЛЛЛФЄЗЈЕчНтБЅКЭЪГбЮЫЎдРэЪОвтЭМЁЃ
гвЭМЮЊбєРызгНЛЛЛФЄЗЈЕчНтБЅКЭЪГбЮЫЎдРэЪОвтЭМЁЃ
ЯТСаЫЕЗЈВЛе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁЁЁ AЃЎДгEПквнГіЕФЦјЬхЪЧCl2
ЁЁЁЁЁЁЁЁ BЃЎДгBПкМгШыКЌЩйСПNaOHЕФЫЎШмвКвддіЧПЕМЕчад
ЁЁЁЁЁЁЁЁ CЃЎБъзМзДПіЯТУПЩњГЩ22.4 LCl2ЃЌБуВњЩњ2 mol NaOH
ЁЁЁЁЁЁЁЁ DЃЎДжбЮЫЎжаКЌCa2+ЁЂMg2+ЁЂFe3+ЁЂSO42ЃЕШРызгЃЌ
ОЋжЦЪБЯШМгNa2CO3ШмвК
17ЃЎвбжЊ0.1molЁЁLЃ1ЕФЖўдЊЫсH2AШмвКЕФpH=4.0ЃЌдђЯТСаЫЕЗЈжае§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁЁЁ AЃЎдкNa2AЁЂNaHAСНШмвКжаЃЌЖМКЌга5жжРызгЃЌЧвжжРрЯрЭЌ
ЁЁЁЁЁЁЁЁ BЃЎHA-ЫЎНтЕФРызгЗНГЬЪНЮЊЃКHA-+H2O H3O++A2-
H3O++A2-
ЁЁЁЁЁЁЁЁ CЃЎдкNaHAШмвКжавЛЖЈгаЃК c(OHЃ)=c(HA-)+ 2c(H2A)+ c(H+)-c(Na+)
ЁЁЁЁЁЁЁЁ DЃЎдкNa2AШмвКжавЛЖЈгаЃКc(Na+)>c(A2-)> c(H+)>c(OHЃ)
16ЃЎЮЊжЄУїФГПЩШмадвЛдЊЫс(HX)ЪЧШѕЫсЃЌФГЭЌбЇЩшМЦСЫШчЯТЪЕбщЗНАИЁЃЦфжаВЛКЯРэЕФЪЧ(ЁЁЁЁ )
ЁЁЁЁЁЁЁЁ AЃЎЪвЮТЯТЃЌВт0.1 mol/L HXШмвКЕФpHЃЌШєpHЃО1ЃЌжЄУїHXЪЧШѕЫс
ЁЁЁЁЁЁЁЁ BЃЎЪвЮТЯТЃЌНЋЕШХЈЖШЕШЬхЛ§ЕФбЮЫсКЭNaXШмвКЛьКЯЃЌШєЛьКЯШмвКpHЃМ7ЃЌжЄУїHXЪЧ
ШѕЫс
ЁЁЁЁЁЁЁЁ CЃЎЪвЮТЯТЃЌВт1 mol/L NaXШмвКЕФpHЃЌШєpHЃО7ЃЌжЄУїHXЪЧШѕЫс
ЁЁЁЁЁЁЁЁ DЃЎдкЯрЭЌЬѕМўЯТЃЌЖд0.1 mol/LЕФбЮЫсКЭ0.1 mol/LЕФHXШмвКНјааЕМЕчадЪЕбщЃЌШєHXШмвКЕЦХнНЯАЕЃЌжЄУїHXЮЊШѕЫс
15ЃЎЯТСаЙигкЕчНтжЪШмвКЕФа№Ъіе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁЁЁ AЃЎГЃЮТЯТЃЌpHЃН7ЕФNH4ClгыАБЫЎЕФЛьКЯШмвКжаРызгХЈЖШДѓаЁЫГађЮЊ
c(ClЃ)ЃОc(NH4+)ЃОc(H+)ЃОc(OHЃ)
ЁЁЁЁЁЁЁЁ BЃЎНЋpHЃН4ЕФДзЫсШмвКЯЁЪЭКѓЃЌШмвКжаЫљгаРызгЕФХЈЖШОљНЕЕЭ
ЁЁЁЁЁЁЁЁ CЃЎжаКЭpHгыЬхЛ§ОљЯрЭЌЕФбЮЫсКЭДзЫсШмвКЃЌЯћКФNaOHЕФЮяжЪЕФСПЯрЭЌ
ЁЁЁЁ DЃЎГЃЮТЯТЃЌЭЌХЈЖШЕФNa2SгыNaHSШмвКЯрБШЃЌNa2SШмвКpHДѓ
13ЃЎНігУвЛжжЪдМСМјБ№ШчЯТЮяжЪЃКБНЁЂCCl4ЁЂNaIШмвКЁЂNaClШмвКЁЂNa2SO3ШмвКЃЌЯТСаЪдМСжаВЛФмбЁгУЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁЁЁ AЃЎфхЫЎЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁ BЃЎFeCl3ШмвКЁЁЁЁ
ЁЁЁЁЁЁЁЁ CЃЎЫсадKMnO4ШмвКЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁ DЃЎAgNO3ШмвК
 ЁЁ
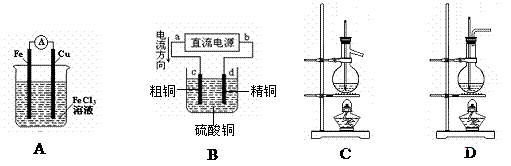
14ЃЎРћгУЯТСазАжУ(ВПЗжвЧЦївбЪЁТд)ЃЌВЛФмЫГРћЭъГЩЖдгІЪЕбщЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁ
14ЃЎРћгУЯТСазАжУ(ВПЗжвЧЦївбЪЁТд)ЃЌВЛФмЫГРћЭъГЩЖдгІЪЕбщЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁЁЁ AЃЎдЕчГи ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎОЋСЖЭЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎЪЏгЭЕФЗжСѓЁЁ ЁЁЁЁЁЁ DЃЎЪЕбщЪвжЦввЯЉ
12ЃЎУРЙњПЦбЇМвЗЂБэТлЮФЃЌаћВМЗЂЯжСЫТСЕФЁАГЌМЖдзгЁБНсЙЙ--A1 13КЭA114ЁЃвбжЊет
ЁАГЌМЖдзгЁБзюЭтВуЕчзгЪ§жЎКЭЮЊ40ИіДІгкЯрЖдЮШЖЈзДЬЌЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧ(ЁЁЁЁ )
ЁЁ ЁЁЁЁ AЃЎAll3КЭA114ЛЅЮЊЭЌЮЛЫи
ЁЁ ЁЁЁЁ BЃЎAll3ГЌдзгжаAlдзгМфЭЈЙ§РызгМќНсКЯ
ЁЁ ЁЁЁЁ CЃЎA114зюЭтВуЕчзгЪ§жЎКЭЮЊ42ЃЌгыЕкIIAзхдЊЫиЕФаджЪЯрЫЦ
ЁЁ ЁЁЁЁ DЃЎAll3КЭA114ЖМОпгаНЯЧПЕФЛЙдадШнвзЪЇШЅЕчзгЩњГЩбєРызг
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com