
Р§2. Шє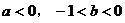 ЃЌдђ(ЁЁЁЁ )
ЃЌдђ(ЁЁЁЁ )
A. 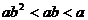
B. 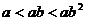
C. 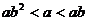
D. 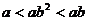
НтЃКШЁ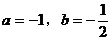 ЃЌКмШнвзЕУЕНД№АИЮЊDЁЃ
ЃЌКмШнвзЕУЕНД№АИЮЊDЁЃ
ЕуВІЃКЬиР§ЗЈОЭЪЧгУЗћКЯвбжЊЬѕМўЕФЬиР§ЛђПМТЧЬиЪтЧщПіЁЂЬиЪтЮЛжУЃЌМьбщбЁдёжЇЛђЛЏМђвбжЊЬѕМўЃЌЕУГіД№АИЁЃЕБвбжЊЬѕМўжагаЗЖЮЇЪБПЩПМТЧЪЙгУЬиР§ЗЈЁЃ
Р§1. Шє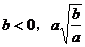 гавтвхЃЌдђ
гавтвхЃЌдђ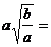 (ЁЁЁЁ )ЁЃ
(ЁЁЁЁ )ЁЃ
A. 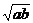 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ B.
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ B.

C. 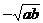 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ D.
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ D.
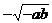
НтЃКИљОнЬтЩшЃЌзЂвтЕН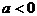 ЃЌжБНгЛЏМђдЪНЃЌПЩЕУ
ЃЌжБНгЛЏМђдЪНЃЌПЩЕУ ЁЃ
ЁЃ
бЁCЁЃ
ЕуВІЃКжБНгЗЈОЭЪЧжБНгДгЬѕМўГіЗЂЃЌЭЈЙ§КЯРэдЫЫуКЭбЯУмЭЦРэЃЌзюКѓЭЦГіе§ШЗЕФНсЙћЃЌдйЖдеебЁдёжЇНтД№ЕФвЛжжНтЬтЫМТЗЁЃ
29. (13Зж)
(1) (ЁЁ ЁЁЁЁ)(2)ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
(3)ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
(4)ЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃЌЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
28.(11Зж)
(1)______________________ЁЁЁЁЁЁ _ _ЁЃ (2)______________ЁЁЁЁ ____ЁЃ
(3)K=___________ ____ЃЌ _____ _____ЗДгІ (4)_________ЁЁЁЁ _ЁЁЁЁЁЁ __
27.(12Зж)(1)дзгНсЙЙЪОвтЭМЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃЛ
ЭтЮЇЕчзгХХВМЪНЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
(2)ЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁ(гУЛЏбЇЪНБэЪО)ЃЛЁЁЁЁЁЁ ИіІвМќКЭЁЁЁЁЁЁ ИіІаМќЁЃ
(3)ЛЏбЇЪНЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЃЌЁЁЁЁЁЁ дгЛЏЗНЪНгыХфЮЛЬхвдЁЁ ЁЁЁЁЁЁМќЯрНсКЯЁЃ
26.(10Зж)ЂХдЊЫиУћГЦЃК CЁЁ ЁЁЁЁЁЁ
ЂЦаЮГЩЙ§ГЬЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЂЧНсЙЙЪНЃКЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЃЛЕчзгЪНЃКЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЂШПеМфЙЙаЭЃКЁЁЁЁЁЁ ЁЁЁЁЁЁЃЌЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁ(ЬюЁАМЋадЗжзгЁБЛђЁАЗЧМЋадЗжзгЁБ)
(5)гЩДѓЕНаЁЕФЫГађЮЊЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ(гУдЊЫиЗћКХБэЪО)ЁЃ
25. (6Зж)
ЁЁЂХЁЁЁЁЁЁ ЃЛ ЂЦЁЁЁЁЁЁ ЃЛЁЁ ЂЧЁЁЁЁЁЁ ЃЛ ЂШЁЁЁЁЁЁ ЃЛЂЩЁЁЁЁЁЁ ЁЃ
29. (13Зж)
(1)ЯТСагаЙиОЇЬхЕФа№ЪіжаДэЮѓЕФЪЧ(ЁЁ )
AЃЎЪЏгЂОЇЬхжаЕФЙшдзгвдsp2дгЛЏЗНЪНгыжмЮЇЕФбѕдзгаЮГЩЙВМлМќ
BЃЎТШЛЏФЦОЇЬхжаУПИіNa+ЛђCl-жмЮЇНєСкЕФга6ИіCl- ЛђNa+ЁЁ ЁЁЁЁЁЁЁЁЁЁ
CЃЎдкCsClОЇЬхжаУПИіCs+ жмЮЇНєСкЕФга8ИіCl-ЃЌЖјКЭУПИіCl-ЕШОрРыНєСкЕФвВга8ИіCs+ЁЁЁЁ
DЃЎдкУцаФСЂЗНУмЖбЛ§ЕФН№ЪєОЇЬхжаЃЌУПИіН№ЪєдзгжмЮЇНєСкЕФга4ИіН№Ъєдзг
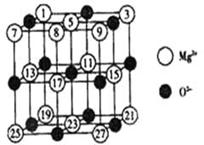 (2)вбжЊMgOЕФОЇЬхНсЙЙЪєгкNaClаЭЁЃФГЭЌбЇ
(2)вбжЊMgOЕФОЇЬхНсЙЙЪєгкNaClаЭЁЃФГЭЌбЇ
ЛГіЕФMgOОЇАћНсЙЙЪОвтЭМШчЯТЭМЫљЪОЃЌЧыИФе§ЭМ
жаДэЮѓЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(гУЮФзжБэЪі)
(3)ЕкШ§жмЦкВПЗждЊЫиЗњЛЏЮяЕФШлЕуМћЯТБэЃК
|
ЗњЛЏЮя |
NaF |
MgF2 |
SiF4 |
|
ШлЕу/K |
1266 |
1534 |
183 |
НтЪЭБэжаЗњЛЏЮяШлЕуВювьЕФдвђЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(4)ШЫЙЄФЃФтЪЧЕБЧАбаОПЕФШШЕуЁЃгабаОПБэУїЃЌЛЏКЯЮяXПЩгУгкбаОПФЃФтУИЃЌЕБЦфНсКЯ
ЁЁ ЛђCu(I)(IБэЪОЛЏКЯМлЮЊ+1)ЪБЃЌЗжБ№аЮГЩaКЭbЃК
ЛђCu(I)(IБэЪОЛЏКЯМлЮЊ+1)ЪБЃЌЗжБ№аЮГЩaКЭbЃК
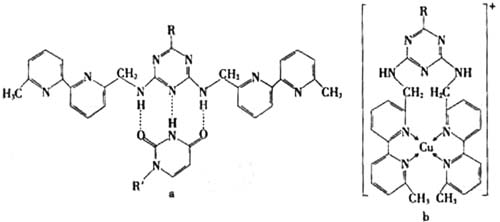
ЗжЮіaКЭbжаЮЂСЃМфЕФЯрЛЅзїгУ(АќРЈЛЏбЇМќКЭЗжзгМфЯрЛЅзїгУ)ЕФВювьЃЌЪджИГі
ЦфВЛЭЌЕуЃК
aжаКЌЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЃЌbжаКЌЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ(гУЁАЧтМќЁБЁЂЁАХфЮЛМќЁБЁЂЁАМЋадМќЁБЁЂЁАЗЧМЋадМќЁБЕШЬюПе)
ЛЏбЇД№ЬтПЈ(ЦНааАр)
28.(11Зж)дкШнЛ§ЮЊ1LЕФУмБеШнЦїжаЃЌНјааШчЯТЗДгІЃКA(g)+2B(g)  C(g)+D(g)ЃЌдкВЛЭЌЮТЖШЯТЃЌDЕФЮяжЪЕФСПn(D)КЭЪБМфtЕФЙиЯЕШчЭМЁЃЧыЛиД№ЯТСаЮЪЬтЃК
C(g)+D(g)ЃЌдкВЛЭЌЮТЖШЯТЃЌDЕФЮяжЪЕФСПn(D)КЭЪБМфtЕФЙиЯЕШчЭМЁЃЧыЛиД№ЯТСаЮЪЬтЃК
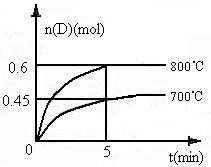 (1)700ЁцЪБЃЌ0-5minФкЃЌвдBБэЪОЕФЦНОљЗДгІЫй
(1)700ЁцЪБЃЌ0-5minФкЃЌвдBБэЪОЕФЦНОљЗДгІЫй
ТЪЮЊ____________________________ЁЃ
(2)ФмХаЖЯИУЗДгІЪЧЗёДяЕНЛЏбЇЦНКтзДЬЌЕФвРОнЪЧ
(ЖрбЁПлЗж)__________________ЁЃ
A.ШнЦїжабЙЧПВЛБфЁЁ ЁЁB.ЛьКЯЦјЬхжаc(A)ВЛБф
C.2vе§(B)=vФц(D)ЁЁ ЁЁЁЁD.c(A)= c (C)
(3)ШєзюГѕМгШы1.0molAКЭ2.2molBЃЌРћгУЭМжаЪ§ОнМЦЫу800ЁцЪБЕФЦНКтГЃЪ§
K=_______________ЃЌИУЗДгІЮЊ__________ЗДгІ(ЬюЁАЮќШШЁБЛђЁАЗХШШЁБ)ЁЃ
(4)800ЁцЪБЃЌФГЪБПЬВтЕУЬхЯЕжаИїЮяжЪЕФЮяжЪЕФСПХЈЖШШчЯТЃКc(A)=0.06molЁЄLЃ1ЃЌc(B)=0.50molЁЄLЃ1,c(C)=0.20molЁЄLЃ1ЃЌc(D)=0.018molЁЄLЃ1ЃЌдђДЫЪБИУЗДгІНЋ______________(ЬюЁАЯђгввЦЖЏЁБЁЂЁАЯђзѓвЦЖЏЁБЛђЁАДІгкЦНКтзДЬЌЁБ)ЁЃ
27.(12Зж)гаAЁЂBЁЂCЁЂDЁЂEЮхжждЊЫиЃЌЦфжаAЁЂBЁЂCЁЂDЮЊЖЬжмЦкдЊЫиЃЌAдЊЫиЕФжмЦкЪ§ЁЂжїзхЪ§ЁЂдзгађЪ§ЯрЭЌЃЛBдзгКЫЭтга3жжФмСПВЛЭЌЕФдзгЙьЕРЧвУПжжЙьЕРжаЕФЕчзгЪ§ЯрЭЌЃЛCдзгЕФМлЕчзгЙЙаЭЮЊns n np n+1ЃЌDдЊЫиЕФдзгзюЭтВуЕчзгЪ§БШДЮЭтВуЕчзгЪ§Щй2ИіЃЌDЕФвѕРызггыEЕФбєРызгЕчзгВуНсЙЙЯрЭЌЃЌDКЭEПЩаЮГЩЛЏКЯЮяE2DЁЃ
(1)ЩЯЪідЊЫижаЃЌEдЊЫиЕФдзгНсЙЙЪОвтЭМЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
DдЊЫиЕФЭтЮЇЕчзгХХВМЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
(2)ЯТСаЗжзгНсЙЙЭМжаЕФ КЭ
КЭ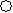 БэЪОЩЯЪідЊЫиЕФдзгжаГ§ШЅзюЭтВуЕчзгЕФЪЃгрВПЗжЃЌ аЁКкЕуБэЪОУЛгааЮГЩЙВМлМќЕФзюЭтВуЕчзгЃЌЖЬЯпБэЪОЙВМлМќЁЃ
БэЪОЩЯЪідЊЫиЕФдзгжаГ§ШЅзюЭтВуЕчзгЕФЪЃгрВПЗжЃЌ аЁКкЕуБэЪОУЛгааЮГЩЙВМлМќЕФзюЭтВуЕчзгЃЌЖЬЯпБэЪОЙВМлМќЁЃ
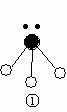 ЁЁЁЁЁЁ
ЁЁЁЁЁЁ 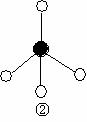 ЁЁЁЁЁЁ
ЁЁЁЁЁЁ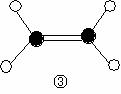 ЁЁЁЁЁЁ
ЁЁЁЁЁЁ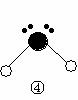
дђдквдЩЯЗжзгжаЃЌжааФдзгВЩгУsp3дгЛЏаЮГЩЛЏбЇМќЕФЗЧМЋадЗжзгЪЧЁЁЁЁЁЁЁЁЁЁЁЁ (гУЛЏбЇЪНБэЪО)ЃЛ дкЂлЕФЗжзгжагаЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ИіІвМќКЭЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ИіІаМќЁЃ
(3)AgNO3 ШмвКгызуСПCЕФЧтЛЏЮяЫЎШмвКЗДгІЩњГЩЕФХфКЯЮяЃЌЦфЛЏбЇЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌИУХфКЯЮяжааФдзгЭЈЙ§ЁЁЁЁЁЁ дгЛЏЗНЪНгыХфЮЛЬхвд
ЁЁ ЁЁЁЁЁЁМќЯрНсКЯЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com