
题目列表(包括答案和解析)
4.使5.6 L CO2气体迅速通过Na2O2固体后得到4.48 L气体(标准状况),这4.48 L气体的质量为( )
A.8.8 g B.6.4 g C.8.2 g D.6.2 g
解析:根据Na2O2与CO2反应的方程式,利用差量法进行计算:
2Na2O2+2CO2===2Na2CO3+O2 ΔV
2×22.4 L 22.4 L
V(CO2) (5.6-4.48) L
反应消耗CO2的体积V(CO2)=2ΔV=2×1.12 L=2.24 L
则生成O2的体积V(O2)=V(CO2)=1.12 L
气体总质量:m=m(CO2)+m(O2)=×44 g/mol+×32 g/mol=8.2 g。
答案:C
3.下列判断正确的是( )
A.可用水来确定某Na2O粉末中是否含有Na2O2
B.可用CO2来确定某Na2O粉末中是否含有Na2O2
C.可利用在空气中加热的方法除去Na2O中的Na2O2
D.将足量的Na2O2、Na2O分别加到酚酞试液中,最终溶液均为红色
解析:CO2、H2O与Na2O2、Na2O均能反应,但与Na2O2反应时能产生气体,不过因氧气是无色无味的气体且CO2也是气体,故CO2和Na2O2的反应无明显的现象产生,水与Na2O2反应则会产生气泡而有明显的现象,故A项正确而B项错误;在空气中加热Na2O2与Na2O的混合物,后者会转化为前者,故C项错误;D项中两种氧化物加到酚酞试液中后,均先与试液中的水反应生成碱而使试液先变为红色,但因Na2O2具有漂白性,最后又会将变成红色的溶液漂白,故D项错误。
答案:A
2. 过氧化钠能与水反应,某同学在学习了这一反应后提出了以下说法,你认为正确的是( )
A.Na2O2是氧化剂,H2O是还原剂
B.Na2O2既作氧化剂,又作还原剂
C.氧化剂和还原剂的质量比为1∶1
D.在2Na2O2+2H2O===4NaOH+O2↑的反应中,转移的电子数为4e-
解析:在Na2O2与H2O反应中,Na2O2中O为-1价,其中有一部分升高到0价,有一部分降低到-2价,H2O中元素化合价未变。1 mol Na2O2在反应中转移电子为1 mol。
答案:BC
1.2.1g平均分子质量为7.2的CO与H2组成的混合气体与足量的O2充分燃烧后,立即通入足量的Na2O2固体中,固体的质量增加( )
A.2.1 g B.3.6 g C.7.2 g D.无法确定
解析:本题涉及的反应方程式有:
①2CO+O22CO2
②2Na2O2+2CO2===2Na2CO3+O2
③2H2+O22H2O
④2Na2O2+2H2O===4NaOH+O2↑
将①②叠加得:
⑤Na2O2+CO===Na2CO3
将③④叠加得:
⑥Na2O2+H2===2NaOH
综合分析知,增加的质量为CO和H2的质量和。
答案:A
21. (2009·滨州10月模拟)(1)已知液氨中存在着平衡2NH3 NH+NH。科学家在液氨中加入氢氧化铯(CsOH)和特殊的吸水剂,使液氨中的NH生成N4分子,请写出液氨与氢氧化铯反应的化学方程式:
。
NH+NH。科学家在液氨中加入氢氧化铯(CsOH)和特殊的吸水剂,使液氨中的NH生成N4分子,请写出液氨与氢氧化铯反应的化学方程式:
。
(2)含有一定量(NH4)2SO4和NH3·H2O的水溶液称为“缓冲溶液”,在此溶液中加入少量的强碱或强酸时,溶液的pH几乎不变,这可由下列离子方程式来说明:
加酸时:NH3·H2O+H+ NH+H2O
NH+H2O
加碱时:NH+OH- NH3·H2O
NH3·H2O
由于(NH4)2SO4和NH3·H2O的大量存在,加少量酸或碱时,溶液中c(H+)与c(OH-)基本保持不变。
含有一定的NaH2PO4和Na2HPO4的溶液,也具有缓冲作用,写出此溶液中加入少量强酸或强碱时发生的离子反应方程式:
加酸时: ;
加碱时: 。
解析:(1)已知氨水中存在着电离平衡2NH3 NH+NH,加入CsOH会生成CsNH2,从而释放出更多的NH和OH-,在特殊的吸水剂条件下,这两种离子生成N4、H2和H2O,故可得总反应方程式为:8NH3+4CsOH===N4+4CsNH2+6H2↑+4H2O。
NH+NH,加入CsOH会生成CsNH2,从而释放出更多的NH和OH-,在特殊的吸水剂条件下,这两种离子生成N4、H2和H2O,故可得总反应方程式为:8NH3+4CsOH===N4+4CsNH2+6H2↑+4H2O。
(2)依据信息提示:加H+时HPO结合H+生成H2PO;加OH-时H2PO结合OH-生成HPO,从而使溶液的pH保持相对稳定,故称为缓冲溶液。
答案:(1)8NH3+4CsOH===N4+4CsNH2+6H2↑+4H2O
(2)HPO+H+ H2PO
H2PO
H2PO+OH- HPO+H2O
HPO+H2O
20.人体胃液中含有胃酸(0.2%-0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内。当胃酸过多时就会出现“咯酸水”、“烧心”、“胃部隐隐作痛”等症状,严重时会降低食欲,引起消化不良等。当胃酸过多时,医生通常用“小苏打片”、“胃舒平”给病人治疗(小苏打片的成分是碳酸氢钠,胃舒平中则含有氢氧化铝)。
(1)写出用“小苏打片”治疗胃酸过多时反应的离子方程式: 。
(2)有人用土法治疗胃酸过多病,方法是:将鸡蛋皮洗净、烤焦、磨细服用。据说这种疗法效果还不错。请用学过的知识分析其中的化学道理。
。
(3)如果病人同时患有胃溃疡,此时最好服用胃舒平,反应的离子方程式为: 。
(4)氢氧化钠也能中和胃酸,可以服用少量氢氧化钠来治疗胃酸过多病吗? 。
(5)写出NaOH溶液分别与“小苏打”、“胃舒平”溶液反应的离子方程式: 。
解析:用化学知识解释、解决生活、社会问题很好地体现了新课程的STSE理念,是今后高考的命题趋势。在给定的新情境下,按题目要求能够熟练地写出离子方程式。NaHCO3、Al(OH)3都既与强酸反应,又与强碱反应,Al(OH)3和HCO在离子方程式中不可拆写。
答案:(1)HCO+H+===CO2↑+H2O (2)鸡蛋皮中含CaCO3,洗净是为了除杂物,烤焦主要是杀菌、消毒,服用后CaCO3与HCl反应起到了降低HCl浓度的作用。CaCO3+2H+===Ca2++CO2↑+H2O (3)Al(OH)3+3H+===Al3++3H2O (4)不能,NaOH虽然能中和胃酸,但它有强腐蚀性,故不能服用NaOH治疗胃酸过多病。 (5)OH-+HCO===H2O+CO, OH-+Al(OH)3===[Al(OH)4]-
19.(原创)实验室为自然科学(化学)兴趣小组的同学准备了四种红色溶液,它们分别可能是KMnO4酸性溶液、滴有酚酞的NaOH溶液、滴有石蕊的稀硫酸和品红溶液。另外还提供了常见的仪器和药品。为了培养同学们的创新精神和实践能力,老师规定只允许选用一种试剂对上述四种溶液加以鉴别。
(1)甲组同学选用了FeCl2溶液,试写出该组同学鉴别出NaOH溶液的有关离子方程式: 。
(2)乙组同学选用了Na2SO3溶液,他们第一步鉴别出来的溶液是AA,对应的现象分别是 。还需继续完成的实验是
(请简要写明操作步骤、现象和结论)。
(3)丙组同学选用了甲、乙两组另外的一种试剂,鉴别时较甲、乙两组在操作上更为简便,你认为他们选择的试剂可能是AA____。
解析:(1)检验Fe2+方法可利用Fe(OH)2的性质(白色絮状沉淀迅速变为灰绿色,最后变为红褐色)。
(3)丙组试剂的选择依据OH-+NHNH3↑+H2O,MnO具有氧化性可将S2-、SO氧化,因而可组成为(NH4)2SO3或NH4HSO3、(NH4)2S、NH4HS。
答案:(1)Fe2++2OH-===Fe(OH)2↓,4Fe(OH)2+O2+2H2O===4Fe(OH)3
(2)KMnO4酸性溶液;稀硫酸 红色退去;产生无色刺激性气味气体。(以下答题具有开放性,答案不唯一) 另取未鉴别出的两待测液,分别向其中滴加稀H2SO4,红色退去者为NaOH溶液,剩余为品红溶液。或:另取未鉴别出的两待测液,分别向其中滴加KMnO4酸性溶液,红色退尽者为品红溶液,余者为NaOH溶液。或:另取未鉴别出的两待测液,并以稀H2SO4和Na2SO3反应产生的SO2分别通入到两待测液中,红色退去,取退色溶液加热,重新变红者为品红溶液,余者为NaOH溶液
(3)(NH4)2SO3或NH4HSO3、(NH4)2S、NH4HS
18.现有含杂质的试剂,科学实验中,对物质的纯度有严格的要求,只用一种试剂即可除去下列各物质中的杂质(括号内为杂质),试写出所用试剂及有关反应的离子方程式。
(1)BaCl2(HCl) 选用试剂 ,
离子方程式 。
(2)CO2(SO2) 选用试剂 ,
离子方程式 。
(3)NaCl(Na2SO4) 选用试剂 ,
离子方程式 。
(4)FeCl2(FeCl3) 选用试剂 ,
离子方程式 。
(5)Na2CO3(NaHCO3) 选用试剂 ,
离子方程式 。
解析:根据杂质的性质选择合适的试剂,然后根据离子反应实质进行书写。
17.某无色溶液,其中可能存在的离子如下:Na+、Ag+、Ba2+、Al3+、[Al(OH)4]-、S2-、CO、SO、SO。现取该溶液进行有关实验,有如下结果,试回答有关问题
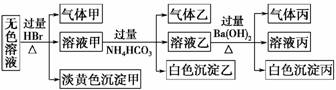
(1)沉淀甲是 ,生成沉淀甲的离子方程式为 。
(2)沉淀乙是 ,由溶液甲生成沉淀乙的离子方程式为 。
(3)沉淀丙是 ,如何用一化学实验来确定其成分? 。
(4)综合上述信息,溶液中可以肯定存在的离子有 。
解析:确定沉淀甲较为关键。若甲是AgBr,即溶液中含Ag+,则所有阴离子均不可能大量存在,转而分析的是S2-、SO与H+反应生成S,从而使思路畅通。
答案:(1)S 2S2-+SO+6H+===3S↓+3H2O
(2)Al(OH)3 Al3++3HCO===Al(OH)3↓+3CO2↑
(3)一定有BaCO3,还可能有BaSO4 向沉淀丙中加入过量的稀盐酸,若沉淀不能完全溶解,说明其中有BaSO4
(4)S2-、SO、[Al(OH)4]-、Na+
16.在某无色溶液里,只含有下列8种离子中的某几种:Na+、H+、Ag+、Mg2+、Cl-、OH-、HCO、NO。已知该溶液能跟铝粉反应,且放出的气体只有H2。试回答:
(1)若溶液和铝粉反应后有[Al(OH)4]-生成,则溶液中一定含有大量的 离子,
还可能含有大量的 离子。
(2)若溶液和铝粉反应后有Al3+生成,则原溶液中一定不含有大量的 离子。
解析:(1)溶液与铝粉反应生成[Al(OH)4]-,则溶液一定含有大量的OH-,所给离子中可与OH-大量共存的有Na+、Cl-和NO,但溶液中必须有阳离子存在,故Na+一定大量存在。
(2)溶液与铝粉反应产生Al3+,则溶液中一定含有大量的H+。与H+大量共存的离子有Na+、Mg2+、Cl-、NO,但因NO在酸性条件下有强氧化性,与金属反应不产生H2,故阴离子只能是Cl-。Ag+与Cl-不能大量共存,故溶液中一定不含有OH-、HCO、NO、Ag+。
答案:(1)OH-、Na+ Cl-、NO (2)OH-、HCO、NO、Ag+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com