
例1.求函数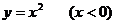 的反函数,并利用对称关系作出其反函数的图象.
的反函数,并利用对称关系作出其反函数的图象.
解:∵原函数的定义域是x<0,值域是y>0,
∴由y=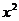 解出
解出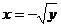 ,
,
∴函数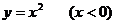 的反函数是
的反函数是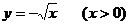 ,
,
作 y=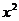 (x
(x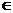 (-∞,0))的图象,再作该函数关于直线y=x的对称曲线,即为函数
(-∞,0))的图象,再作该函数关于直线y=x的对称曲线,即为函数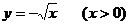 的图象(如图).
的图象(如图).
例2.求函数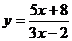 的值域.
的值域.
分析:灵活运用互为反函数的两个函数定义域和值域之间的关系.
解:∵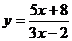 ∴
∴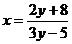 ∴ y≠
∴ y≠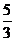
∴函数的值域为{y|y≠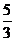 }
}
例3 已知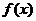 =
=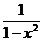 (x<-1),求
(x<-1),求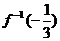 ;
;
解法1:⑴令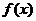 =y=
=y=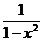 ,∴
,∴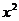 =
=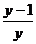 --①,∵x<-1,∴x=-
--①,∵x<-1,∴x=-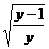 ;⑵∵x<-1,由①式知
;⑵∵x<-1,由①式知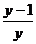 ≥1,∴y<0;
≥1,∴y<0;
⑶∴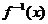 = -
= -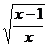 (x<0);⑷
(x<0);⑷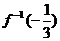 =-2.
=-2.
分析:由y=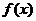 与y=
与y=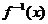 互为反函数的关系可知:当y=
互为反函数的关系可知:当y=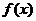 中的x=a时y=b,则在y=
中的x=a时y=b,则在y=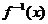 中,当x=b时y=a,本题要求
中,当x=b时y=a,本题要求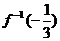 ,设其为u,说明在函数
,设其为u,说明在函数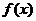 =y=
=y=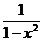 (x<-1)中,当y=
(x<-1)中,当y=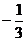 时,x=u,问题转化为知原来函数中的y=
时,x=u,问题转化为知原来函数中的y=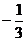 而求x.
而求x.
解法2:令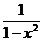 =
=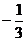 ,变形得
,变形得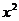 =1+3=4,又∵x<-1,∴x=-2.
=1+3=4,又∵x<-1,∴x=-2.
说明:解法2显然比解法1简捷得多,正确灵活地运用所学的有关概念,往往可以收到事半功倍的效果.
3.应用:⑴利用对称性作反函数的图像
若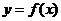 的图象已作出或比较好作,那么它的反函数
的图象已作出或比较好作,那么它的反函数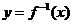 的图象可以由
的图象可以由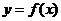 的图象关于直线y=x对称而得到;
的图象关于直线y=x对称而得到;
⑵求反函数的定义域求原函数的值域;
⑶反函数的单调性与原函数的单调性相同
2.证明结论(不要求掌握,根据实际情况处理)
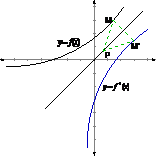 证明:设M(a,b)是
证明:设M(a,b)是 的图象上的任意一点,
的图象上的任意一点,
则当x=a时,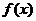 有唯一的值
有唯一的值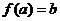 .
.
∵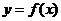 有反函数
有反函数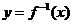 ,
,
∴当x=b时,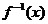 有唯一的值
有唯一的值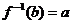 ,
,
即点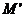 (b,a)在反函数
(b,a)在反函数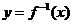 的图象上.
的图象上.
若a=b,则M,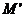 是直线y=x上的同一个点,它们关于直线y=x对称.
是直线y=x上的同一个点,它们关于直线y=x对称.
若a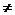 b,在直线y=x上任意取一点P(c,c),连结PM,P
b,在直线y=x上任意取一点P(c,c),连结PM,P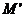 ,M
,M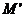
由两点间的距离公式得:
PM=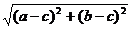 ,P
,P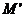 =
=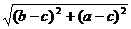 ,
,
∴PM=P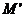 . ∴直线y=x是线段M
. ∴直线y=x是线段M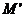 的垂直平分线,
的垂直平分线,
∴点M,
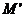 关于直线y=x对称.
关于直线y=x对称.
∵点M是y=f(x)的图象上的任意一点,
∴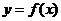 图象上任意一点关于直线y=x的对称点都在它的反函数
图象上任意一点关于直线y=x的对称点都在它的反函数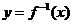 的图象上,由
的图象上,由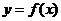 与
与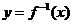 互为反函数可知,函数
互为反函数可知,函数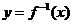 图象上任意一点关于直线y=x的对称点也都在它的反函数
图象上任意一点关于直线y=x的对称点也都在它的反函数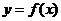 的图象上,
的图象上,
∴函数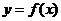 与
与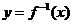 的图象关于直线y=x对称.
的图象关于直线y=x对称.
逆命题成立:若两个函数的图象关于直线y=x对称,则这两个函数一定是互为反函数.
1.探究互为反函数的函数的图像关系
观察讨论函数、反函数的图像,归纳结论:函数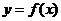 的图象和它的反函数
的图象和它的反函数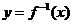 的图象关于直线
的图象关于直线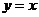 对称.
对称.
5.我们已经知道两个互为反函数的函数间有着必然的联系(在定义域、值域和对应法则方面). 函数图象是从“形”的方面反映这个函数的自变量x与因变量y之间的关系.因此,互为反函数的函数图象间也必然有一定的关系,今天通过观察如下图像研究-互为反函数的函数图象间的关系.
①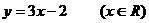 的反函数是
的反函数是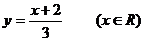

② 的反函数是
的反函数是

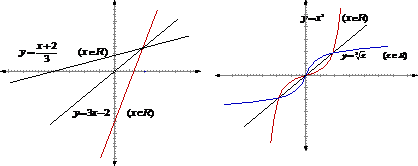
4. 在平面直角坐标系中,①点A(x,y)关于x轴的对称点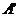 (x,-y);
(x,-y);
②点A(x,y)关于y轴的对称点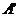 (-x,y);③点A(x,y)关于原点的对称点
(-x,y);③点A(x,y)关于原点的对称点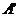 (-x,-y);④点A(x,y)关于y=x轴的对称点
(-x,-y);④点A(x,y)关于y=x轴的对称点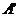 (?,?);
(?,?);
3.反函数的求法:一解、二换、三注明
2.互为反函数的两个函数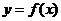 与
与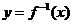 间的关系:
间的关系:
----定义域、值域相反,对应法则互逆;
1.反函数的定义;
2.附加隐含条件的应用规律
⑴溶液无色透明时,则溶液肯定无有色离子。如Cu2+(蓝色)、Fe3+(棕黄色)、Fe2+(浅绿色)、 (紫红色)等都有颜色,若无色溶液则说明这些离子不存在。
(紫红色)等都有颜色,若无色溶液则说明这些离子不存在。
⑵强碱性溶液中肯定不存在与 起反应的离子。
起反应的离子。
⑶强酸性溶液中肯定不存在与H+起反应的离子
⑷与水反应的离子,如O2-、N3-、P3-等在水溶液中不存在。
试题枚举
[例1]下列离子方程式正确的是
A.NaHSO3溶液与NaOH溶液反应:HSO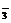 +OH-=SO
+OH-=SO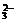 +H2O
+H2O
B.少量二氧化碳通入足量的NaOH溶液:CO2+OH-=
C.Fe与盐酸反应产生H2:2Fe+6H+=2Fe3++3H2↑
D.氨水和醋酸溶液混合NH3·H2O+CH3COOH=NH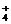 +CH3COO-+H2O
+CH3COO-+H2O
解析: 判断离子方程式的正误应注意①是否符合客观实际;②应该用化学式表示的(气体、沉淀、水、弱酸、弱碱、氧化物、单质等)是否写对,应该删掉的离子是否删去;③是否配平,电子转移是否合理.
据此检查各选项,A、D正确.B错,因少量的CO2通入足量的NaOH溶液中,应生成CO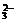 .
.
正确的写法为:CO2+2OH-=CO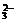 +H2O
+H2O
C错.因不符合客观实际,应生成Fe2+.
正确的写法为:Fe+2H+=Fe2++H2↑
答案: AD
[例2.]下列各组离子中,能在强酸溶液里大量共存,并且溶液呈无色透明的是
A.MnO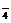 ,K+,Na+,SO
,K+,Na+,SO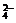 B.Na+,K+,HCO
B.Na+,K+,HCO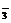 ,Cl-
,Cl-
C.Mg2+,NH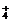 ,Cl-,NO
,Cl-,NO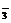 D.Ba2+,K+,S2-,SO
D.Ba2+,K+,S2-,SO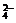
解析:对于离子能否共存问题:必须考虑两个问题,一看同组离子是否发生反应(复分解或氧化还原),二看是否满足题干要求.
有颜色离子:Fe3+,Fe2+,Cu2+,MnO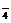 ……
……
强酸性(或强碱性),说明溶液中除离子组内各离子外,还应有H+或(OH-),典型的氧化性离子(如Fe3+,MnO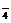 ,Cr2O
,Cr2O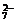 等)和典型的还原性离子(如Fe2+,S2-,I-,SO
等)和典型的还原性离子(如Fe2+,S2-,I-,SO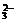 等)在溶液中会发生氧化还原反应.据以上分析得此题正确选项为C.
等)在溶液中会发生氧化还原反应.据以上分析得此题正确选项为C.
答案:C
[例3](1)向NaHSO4溶液中,逐滴加入Ba(OH)2溶液中至中性,请写出发生反应的离子方程式: 。
(2)在以上中性溶液中,继续滴加Ba(OH)2溶液,请写出此步反应的离子方程式 。
解析:题目要求NaHSO4溶液与Ba(OH)2溶液反应呈中性,也即要求写出的离子方程式属于下列反应 2NaHSO4 + Ba(OH)2 = 2H2O + Na2SO4 + BaSO4↓。则离子方程式为:2H+ + SO42- + Ba2+ + 2OH- = BaSO4 ↓ + 2H2O 。若向上述溶液中继续滴加B(OH)2,则有 Ba2+ + SO42- = BaSO4 ↓
答案:2H+ + SO42- + Ba2+ + 2OH- = BaSO4 ↓ + 2H2O
Ba2+ + SO42- = BaSO4 ↓
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com