
题目列表(包括答案和解析)
14.(1)H O Na S (2)SO3 H2O2 Na2O2 (3)NaHSO3 NaHSO4
13.⑴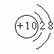 ⑵ NaOH 〉Mg(OH)2
⑵ NaOH 〉Mg(OH)2
⑶ NH3 + H2O  NH3·H2O
NH3·H2O  NH4+ + OH-
NH4+ + OH-
⑷ 分子晶体 ⑸ OH- ;H2O
1.D 2.AD 3.C 4.C 5.B 6.A 7.C 8.D 9.B 10.CD 11.C 12.C
讲析:1.电解质电离时共价键被破坏。 2.可根据元素的化合价来判断氧化物是否是酸酐。 3.本题重点抓住正离子N5+整体为+1价来分析。 5.据题给性质推断氮化硅为原子晶体。 6.根据构成晶体的粒子种类以及它们之间的相互作用的强弱不同来判断。 7.根据玻璃态的水不存在晶体结构,密度不变来判断。 9.由于晶体中每8个笼只有6个容纳了CH4分子,另外2个笼被游离H2O分子填充,由此得出8个笼中共有6个CH4
分子,46+2=48个H2O分子。 11.本题可根据排除法来判断,注意氢键存在于分子间,且气体物质分子之间无相互作用,不存在氢键。 12.n(Ca):n(Ti):n(O)=1:(8╳1/8):(12╳1/4)
3.⑴假定两刚性球间彼此相切,这才可将Li+与I-的距离看成是两离子半径之和。⑵ 0.214nm 0.088nm ⑶r+>0.060nm-0.068nm,说明将Li+和I-看成刚性球组实际不相切。因为电子之间相互排斥,致使两离子半径之和小于它们之间的理论距离。
 讲析:⑵根据NaCl的晶体结构即可建立如上图所示的“数学模型”。设图中大圆表示I-,其半径为r-,小圆为Li+,其半径为r+,则有如下关系:AC=2(r++r-),
讲析:⑵根据NaCl的晶体结构即可建立如上图所示的“数学模型”。设图中大圆表示I-,其半径为r-,小圆为Li+,其半径为r+,则有如下关系:AC=2(r++r-),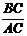 =sin45°,BC=2r-,根据上式解得r+/r-=0.414,又由假定知:r++r-=0.303nm,从而解得r+=0.088nm,r-=0.214nm
=sin45°,BC=2r-,根据上式解得r+/r-=0.414,又由假定知:r++r-=0.303nm,从而解得r+=0.088nm,r-=0.214nm
检测提高
1.B 2.BC
讲析:1.H2O2、Na2O2中均存在非极性键;SiO2等属于原子晶体的共价化合物熔点高;金属晶体中含金属阳离子,但不存在阴离子。 2.物质熔沸点的高低主要决定于微粒间作用力的大小,比较时首先要判断晶体类型,另外合金的熔点低于各成分金属。
15.Ti14C13
讲析:构成分子晶体的原子只属于一个分子,不与其它分子共用。
第10课时 (B卷)
纠错训练
14. (1)HF,‚HCl,ƒHI,„H2S,…NaOH,†NH3、MgO、NaHCO3
(2)NaCl、NaOH、NaHCO3;‚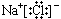
(3)CO2、SO2、H2O;‚SiO2
(4)CH4,‚H2O,ƒCH4,„MgO、SiO2
10.D 11.C 12.D 13.C
讲析:1.可以具有教强氢键的F、O、N,CH4中的C原子没有孤对电子,不存在氢键。 3.铵盐由非金属元素组成却存在共价键,H2O2存在非极性键。 5. 碳、氮原子结合成碳氮化合物是原子晶体。 6. 两个原硅酸分子相互作用而脱去一分子水的方式是:一个分子去OH原子团,另一个分子之去H。 7.解题的关键是判断晶体类型。 8.乙的化学式MY2,离子化合物不一定溶于水。 9.微粒间的作用为共价健,故属于共价化合物。 10. CO2原子晶体转化为分子晶体时发生了结构的变化,故为化学变化;但属于化合物,所以不互为同素异形体。 11.先根据AlCl3的物理性质推知为分子晶体,再判断它的其它性质和分子的极性。 12. MgCl2为离子晶体,水溶液能导电。 13. 该晶体中A、B、C三种原子的个数比是: (8╳1/8):(6╳1/2):1 = 1:3:1
1.D 2.C 3.B 4.BD 5.AC 6.D 7.C 8.BC 9.B
4.⑴ A:NH3 B:HCN C:CO(NH2)2 D:BF3
 ⑵
⑵ 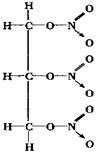
讲析:注意理清原子实和配位共价键的含义及表达。
新活题网站
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com