
题目列表(包括答案和解析)
15、(10分)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2,已知该反应中H2O2只发生如下过程:H2O2→ O2
(1)该反应中的还原剂是 。
(2)该反应中,发生还原反应的过程是 → 。
(3)写出该反应的化学方程式,并标出电子转移的方向和数目
。
(4)如反应转移了0.3mol电子,则产生的气体在标准状况下体积为 。
14、铜和镁的合金4.6g完全溶于浓硝酸,若反应中硝酸被还原只产生4480mL的NO2气体和336mL的N2O4气体(都已折算到标准状况),在反应后的溶液中,加入足量的氢氧化钠溶液,生成沉淀的质量为
A、9.02g B、8.51g C、8.26g D、7.04g
13、含有a mol FeBr2的溶液中,通入x mol Cl2。下列各项为通Cl2过程中,溶液内发生反应的离子方程式,其中不正确的是
A.x=0.4a, 2Fe2-+Cl2=2Fe3++2Cl-
B.x=0.6a, 2Br-+ Cl2=Br2+2Cl-
C.x=a, 2Fe2++2Br-+2Cl2=Br2+2Fe3++4Cl-
D.x=1.5a, 2Fe2++4Br-+3Cl2=2Br2+2Fe3++6Cl-
12、某铁的“氧化物”样品,用2.5mol/L硫酸140mL恰好完全溶解,所得溶液还能吸收标准状况下0.56L氯气,使其中Fe2+全部转化为Fe3+。该样品可能的化学式为
A、Fe2O3 B、Fe3O4 C、Fe4O5 D、Fe5O7
11、在一定体积pH=12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液pH=11。若反应后溶液的体积等于Ba(OH)2溶液与NaHSO4溶液的体积之和,则Ba(OH)2溶液与NaHSO4溶液的体积比是
A.1:9 B.1:1 C.1:2 D.1:4
10、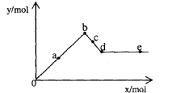 已知Ba(AlO2)2可溶于水。右图表示的是向A12(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加人Ba(OH)2的物质的量x的关系。下列有关叙述正确的是
已知Ba(AlO2)2可溶于水。右图表示的是向A12(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加人Ba(OH)2的物质的量x的关系。下列有关叙述正确的是
A.a-b时沉淀的物质的量:A1(OH)3比BaSO4多
B.c-d时溶液中离子的物质的量:AlO2-比Ba2+多
C.a-d时沉淀的物质的量:BaSO4可能小于A1(OH)3
D.d-e时溶液中离子的物质的量:Ba2+可能等于OH-
9、在下列给定条件的溶液中,一定能大量共存的离子组是
A.无色溶液中:Cu2+、K+、H+、NO3‑
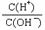 B.由水电离的C(H+)为10-13mol/L:Fe2+、NO3-、K+、Na+
B.由水电离的C(H+)为10-13mol/L:Fe2+、NO3-、K+、Na+
C. =1012的溶液中:NH4+、Ca2+、Cl-、K+
D.无色酚酞显红色:HS-、K+、HCO3-、AlO2-
8、下列离子方程式书写正确的是
A.过量的SO2通入NaOH溶液中:SO2+2OH-=SO32 -+H2O
B.Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-=2Fe2++I2
C.NaNO2溶液中加入酸性KMnO4溶液:2MnO4- +5NO2- +6H+ = 2Mn2++5NO3- +3H2O
D.NaHCO3溶液中加入过量的Ca(OH)2溶液: HCO3- +Ca2++OH-=CaCO3↓+H2O
7、某溶液加入铝能产生氢气。则下列各组离子在水溶液中可以大量共存的是
A.Fe2+、K+、Cl-、NO3- B.K+、Mg2+、Cl-、SO42-
C.Na+、Al3+、HCO3‑、SO42- D.NH4+、Na+、AlO2-、Cl-
6、 氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:
氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:
Al2O3+N2+3C 2AlN+3CO
下列叙述正确的是
A.在氮化铝的合成反应中,N2是还原剂,Al2O3是氧化剂
B.上述反应中每生成2mol AlN,N2得到3mol电子
C.氮化铝中氮元素的化合价为-3
D.氮化铝晶体属于分子晶体
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com