
题目列表(包括答案和解析)
416. 24mL0.0ml·L-1的Na23恰好与20mL0.02ml·L-1的2R27溶液完全反应,则R 元素在还原产物中的化合价为( )
元素在还原产物中的化合价为( )
A.0 B.+2 .+3 D.+6
41.将下列种物质:N2、Fe4、Fe(N3)3、HN3和Fe2(4)3分别填入下面对应的横线上___ ___+______→______+______+______+H2组成一个未配平的化学方程式,正确的顺序是( )
___+______→______+______+______+H2组成一个未配平的化学方程式,正确的顺序是( )
A.Fe4、Fe(N3)3; Fe2(4)3、HN3 、N2
B.HN3、Fe4; Fe2(4)3、Fe(N3)3、N2
.HN3、Fe2(4)3; Fe4、Fe(N3)3、N2
D.Fe2(4)3、N2; Fe4、HN3 、Fe(N3)3
414.被称之为“软电池”的纸质电池,采 用一个薄层纸片(在其一边镀锌,而在其另一边镀二氧化锰)作为传导体在纸内的离子“流过”水和氧化锌组成的电解液电池总反应为:
用一个薄层纸片(在其一边镀锌,而在其另一边镀二氧化锰)作为传导体在纸内的离子“流过”水和氧化锌组成的电解液电池总反应为:
Zn+2Mn2+H2=Zn+2Mn(H),下列说法正确的是( )
A.该电池的正极为锌
B.该电池反应中二氧化锰起催化剂作用
.当0.1mlZn完全溶解时,流经电解液的电子个数为1.204×1023
D.电池正极反应式为:2Mn2+2e-+H2=2Mn(H)+2H-
413. I是一种不溶于水的白色固体,它可以由反应:它可以由下列反应制得:22++4I-=2I↓+I2。现以石墨为阴极,以为阳极电解I溶液,通电前向电解液中加入少量酚酞和淀粉溶液。电解开始不久,阴极区溶液呈红色,而阳极区溶液呈蓝色。对阳极区溶液呈蓝色的正确解释是( )
A.2I--2e-=I2,碘遇淀粉变蓝
B.一2e-=2+, 2+的溶液显蓝色
.22++4I-=2I↓+I2,碘遇淀粉变蓝
D.4H--4e-=2H2+2 2将I-氧化为I2,碘遇淀粉变蓝
412.实验室常利用以下反应制取少量氨气:NaN2+NH41
Na1+N2↑+2H2关于该
反应的下列说法,正确的是 ( )
A.NaN2是氧化剂
B.每生成1mlN2时,转移电子的物质的量为6ml
.NH41中的氮元素被还原
D.N2既是氧化剂,又是还原剂
411.二氯化二硫(2l2)是广泛用于橡胶工业的硫化剂。已知它的结构式为l---l,易与水反应:22l2+2H2 4Hl+2↑+2↓。对该反应下列说法正确的是 ( )
A.2l2既作氧化剂又作还原剂
B.2l2只作氧化剂
.每生成1ml 2转移4ml电子
D.2l2只作还原剂
410.下列叙述中,正确的是( )
A、 含金属元素的离子不一定都是阳离子
B、 在氧化还原反应中,非金属单质一定是氧化剂
C、 某元素从化合态变为游离态时,该元素一定被还原
D、 金属阳离子被还原后不一定得到金属单质
409.对于反应H-+NH3=H2+NH2-的正确说法是( )
A.属于置换反应 B.H-是还原剂
.NH3是还原剂 D.H2既是氧化产物又是还原产物
408.为了测量水中有机物等还原性污染物的含量,通过把1L水样与强氧化剂完全作用时消耗氧化剂的量,折算成以氧气为氧化剂时的质量(2mg•L-1)来表示,称为该水样的化学耗氧量(D)。我国明文规定:D>00 mg•L-1的污水不得直接排放。 为了测定某工业废水的D,实验如下:量取废水样品20.00mL,加入0.100ml•L-1Mn410.00mL和少量稀H24,在一定条件下充分反应后,再用0.200 ml•L-1的草酸钠(Na224)溶液滴定过量的Mn4,达到滴定终点时消耗Na224溶液11.00mL。
(1)写出酸性介质中Mn4(被还原为Mn2+)与Na224(被氧化为2)反应的离子方程式 。
(2)计算该水样的D,写出计算过程 。
(3)如果每次取水样20.00mL,加入等体积的0.100 ml•L-1 Mn4酸性溶液;为简化计算,令滴定过量Mn4时,每消耗1.00mL Na224溶液,就相当于水样的D为10mg•L-1,该Na224溶液的物质的量浓度应配制为多少?
407.俗话说:“饭后一苹果,疾病远离我。”吃水果能帮助消化,当我们把苹果切开后不久,果肉上便会产生一层咖啡色的物质,好像生了“锈”一般,其原因是果肉里的酚在空气中转变为二醌,这些二醌很快聚合成为咖啡色的聚合物。
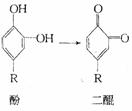
①这一变化(酚变为二醌)的反应类型为 (填序号)。
a.氧化反应 b.还原反应 .加成反应 d.取代反应
②若要避免苹果“生锈”,请你选择一种保存切开的苹果的方 法,
法,

 ,
,
其原因是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com